Хлорат магния (Mg(ClO3)2) представляет собой соединение, состоящее из ионов Mg2+ и ClO3-. Это водорастворимый и высокореактивный белый кристаллический порошок. Его можно использовать как окислитель при производстве фейерверков и как дезинфицирующее средство при очистке воды.
| Название ИЮПАК | Хлорат магния |
| Молекулярная формула | Mg(ClO3)2 |
| Количество CAS | 10326-21-3 |
| Синонимы | Диперхлорат магния, хлорат магния(II), гексагидрат хлората магния |
| ИнЧИ | InChI=1S/2ClHO3.Mg/c2 2-1(3)4;/h2 (H,2,3,4);/q;;+2/p-2 |
Свойства хлората магния
Формула хлората магния
Хлорат магния — химическое соединение формулы Mg(ClO3)2. Соединение состоит из одного иона магния (Mg2+) и двух ионов ClO3. Химическая формула гласит, что одна молекула хлората магния содержит два иона хлорида и шесть атомов кислорода.
Хлорат магния Молярная масса
Молярная масса Mg(ClO3)2 составляет 191,2 г/моль. Эта величина рассчитывается путем сложения атомных масс элементов, присутствующих в молекуле Mg(ClO3)2. Магний имеет молярную массу 24,31 г/моль, а хлор и кислород имеют молярную массу 35,45 г/моль и 16,00 г/моль соответственно. Умножая молярную массу каждого элемента на количество атомов этого элемента в молекуле и складывая их, мы получаем молярную массу соединения.
Температура кипения хлората магния
Mg(ClO3)2 разлагается, не достигнув температуры кипения. При нагревании Mg(ClO3)2 разлагается на хлорид магния, газообразный кислород и газообразный хлор. Следовательно, Mg(ClO3)2 не имеет температуры кипения.
Хлорат магния Температура плавления
Температура плавления Mg(ClO3)2 составляет 105°С. При этой температуре твердое соединение переходит в жидкую форму. Температура плавления Mg(ClO3)2 может варьироваться в зависимости от чистоты соединения и условий ее измерения.
Плотность хлората магния г/мл
Плотность Mg(ClO3)2 составляет 2,21 г/мл. Это означает, что один миллилитр Mg(ClO3)2 имеет массу 2,21 грамма. Плотность Mg(ClO3)2 можно использовать для расчета объема заданной массы соединения или массы заданного объема соединения.
Хлорат магния Молекулярный вес
Молекулярная масса Mg(ClO3)2 составляет 191,2 г/моль. Эта величина рассчитывается путем сложения атомных масс элементов, присутствующих в молекуле Mg(ClO3)2.
Структура хлората магния
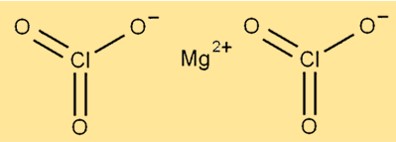
Структура Mg(ClO3)2 состоит из ионов магния, окруженных шестью атомами кислорода и двумя атомами хлора. Ион магния расположен в центре молекулы, а атомы кислорода и хлора расположены вокруг него. Соединение имеет кристаллическую структуру и имеет белый цвет.
Растворимость хлората магния
Mg(ClO3)2 растворим в воде, этаноле и ацетоне. Растворимость Mg(ClO3)2 в воде увеличивается с температурой. При комнатной температуре в 100 мл воды растворяется примерно 31 грамм Mg(ClO3)2. Растворимость Mg(ClO3)2 в других растворителях зависит от полярности растворителя.
| Появление | Белый кристаллический порошок |
| Удельный вес | 2,21 г/см3 |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 191,2 г/моль |
| Плотность | 2,21 г/мл |
| Точка плавления | 105°С |
| Точка кипения | Разлагается перед кипячением |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в воде, этаноле и ацетоне. |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | Непригодный |
| рН | Непригодный |
Безопасность и опасность хлората магния
Mg(ClO3)2 является сильным окислителем и может бурно реагировать с горючими материалами, вызывая пожары или взрывы. Он также может вызвать раздражение кожи, глаз и дыхательной системы при контакте или вдыхании. Поэтому при работе с Mg(ClO3)2 следует использовать соответствующие средства индивидуальной защиты, такие как перчатки и очки. Состав также следует хранить вдали от горючих материалов и источников тепла или возгорания. Кроме того, необходимо обеспечить достаточную вентиляцию для предотвращения вдыхания пыли или паров соединения. С Mg(ClO3)2 следует обращаться осторожно, чтобы избежать потенциальных опасностей.
| Символы опасности | Окислитель |
| Описание безопасности | Избегайте контакта с горючими материалами, надевайте перчатки и защитные очки, обеспечивайте достаточную вентиляцию. |
| Идентификационные номера ООН | ООН1475 |
| код ТН ВЭД | 2829.90.90 |
| Класс опасности | 5.1 |
| Группа упаковки | II |
| Токсичность | Может вызвать раздражение кожи, глаз и дыхательных путей; Может быть вреден при проглатывании |
Методы синтеза хлората магния
Для синтеза Mg(ClO3)2 можно использовать разные методы.
Распространенным методом является реакция гидроксида магния с хлорной кислотой. Реакция протекает следующим образом:
Mg(OH)2 + 2HClO3 → Mg(ClO3)2 + 2H2O
Другой метод — взаимодействие карбоната магния с хлорной кислотой. Реакция протекает следующим образом:
MgCO3 + 2HClO4 → Mg(ClO4)2 + CO2 + H2O
Третий метод включает электролиз хлорида магния в присутствии хлоратной соли, такой как хлорат натрия или калия. Реакция протекает следующим образом:
2MgCl2 + 2NaClO3 → Mg(ClO3)2 + 2NaCl
В этом методе в процессе электролиза используется магниевый анод и хлоратная соль в качестве окислителя.
Использование хлората магния
Mg(ClO3)2 находит различное применение в разных областях. Вот некоторые из его применений:
- Пиротехнические изделия: обычно используются в качестве окислителя в пиротехнических составах, таких как сигнальные ракеты, фейерверки и сигнальные устройства.
- Химический синтез: используется в качестве источника кислорода при синтезе различных химических веществ, включая фармацевтические препараты, красители и взрывчатые вещества.
- Отбеливатель: используется в качестве отбеливателя при производстве бумаги, целлюлозы и текстиля.
- Очистка воды: также используется в качестве средства очистки воды для удаления примесей и бактерий, присутствующих в воде.
- Лабораторный реагент: используется в качестве лабораторного реагента в различных методах аналитической химии.
- Сельское хозяйство: используется в качестве удобрения и кондиционера почвы для обеспечения растений магнием и кислородом.
- Нефтяная и газовая промышленность: Используется в качестве окислителя при буровзрывных работах в нефтегазовой промышленности.
Вопросы:
Вопрос: Какова формула хлората магния?
А: Mg(ClO3)2.
Вопрос: Сколько атомов содержится в 2,1 молях Mg(ClO3)2?
Ответ: В 2,1 молях Mg(ClO3)2 содержится 5,04 x 10^24 атомов.
Вопрос: На что распадается хлорат магния?
Ответ: Mg(ClO3)2 при нагревании может превращаться в хлорид магния, газообразный кислород и газообразный хлор.
Вопрос: Как распадается хлорат магния?
A: Mg(ClO3)2 при нагревании разлагается на хлорид магния и газообразный кислород.
Вопрос: Каково общее количество атомов кислорода, присутствующих в одной единице Mg(ClO3)2?
Ответ: В одной единице Mg(ClO3)2 содержится 6 атомов кислорода.
Вопрос: На что распадается Mg(ClO3)2?
Ответ: Mg(ClO3)2 при нагревании разлагается с образованием MgCl2 и O2.
Вопрос: Каково общее количество молей атомов кислорода, присутствующих в одном моле Mg(ClO3)2?
Ответ: В одном моле Mg(ClO3)2 содержится 6 молей атомов кислорода.
Вопрос: Какова масса Mg(ClO3)2 в граммах?
A: Формульная масса Mg(ClO3)2 в граммах равна 232,21 г/моль.
Вопрос: Является ли Mg(ClO3)2 ионным или молекулярным?
Ответ: Mg(ClO3)2 — ионное соединение.
