Сульфат магния (сульфат) или MgSo4 представляет собой химическое соединение, состоящее из магния, серы и кислорода. Его широко используют в медицине как слабительное, противосудорожное средство и для лечения дефицита магния.
| Название ИЮПАК | Сульфат магния |
| Молекулярная формула | MgSO4 |
| Количество CAS | 7487-88-9 |
| Синонимы | английская соль; английская соль; Горькая соль; Соль для ванны; английская соль; Сал английский; Гептагидрат сульфата магния |
| ИнЧИ | InChI=1S/Mg.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
Формула сульфата магния
Химическая формула сульфата магния – MgSO4. Эта формула указывает на то, что сульфат магния состоит из катиона магния (Mg2+) и сульфат-аниона (SO42-). Формула сульфата магния важна в химических расчетах, поскольку помогает определить количество вещества, необходимого для химической реакции.
Молярная масса MgSO4
Молярная масса сульфата магния составляет 120,366 г/моль. Это значение рассчитывается путем сложения атомных масс одного атома магния (24,305 г/моль), одного атома серы (32,066 г/моль) и четырех атомов кислорода (по 15,999 г/моль каждый). Молярная масса является важным параметром в химических расчетах, поскольку помогает определить количество вещества, необходимое для химической реакции.
Температура кипения сульфата магния
Температура кипения сульфата магния зависит от состояния соединения. Сульфат магния существует в двух формах: безводной и гептагидратной. Безводная форма имеет более высокую температуру кипения 1,124 ° C (2,055 ° F), а гептагидратная форма имеет более низкую температуру кипения 150 ° C (302 ° F). На температуру кипения сульфата магния могут влиять такие факторы, как давление и примеси.
Температура плавления сульфата магния
Температура плавления сульфата магния также зависит от состояния соединения. Безводная форма имеет более высокую температуру плавления — 1,124 ° C (2,055 ° F), тогда как гептагидратная форма имеет более низкую температуру плавления — 150 ° C (302 ° F). На температуру плавления сульфата магния также могут влиять такие факторы, как давление и примеси.
Плотность сульфата магния г/мл
Плотность сульфата магния варьируется в зависимости от состояния соединения. Безводная форма имеет плотность 2,66 г/см³, а гептагидратная форма — 1,68 г/см³. Плотность – это физическое свойство вещества, указывающее количество массы в единице объема. Плотность сульфата магния можно использовать для расчета объема вещества, необходимого для химической реакции.
Молекулярный вес сульфата магния
Молекулярная масса сульфата магния составляет 120,366 г/моль. Это значение рассчитывается путем сложения атомных масс одного атома магния (24,305 г/моль), одного атома серы (32,066 г/моль) и четырех атомов кислорода (по 15,999 г/моль каждый). Молекулярный вес является важным параметром в химических расчетах, поскольку он помогает определить количество вещества, необходимое для химической реакции.
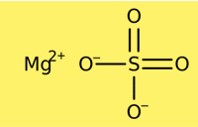
Структура сульфата магния
Сульфат магния имеет кристаллическую структуру. Безводная форма имеет ромбоэдрическую кристаллическую структуру, а гептагидратная форма имеет моноклинную кристаллическую структуру. Кристаллическая структура сульфата магния состоит из катионов магния и сульфат-анионов. Безводная форма содержит один катион магния и один сульфат-анион на клетку, тогда как гептагидратная форма содержит один катион магния и два сульфат-аниона на клетку.
| Появление | Белое кристаллическое твердое вещество |
| Удельный вес | 2,66 (безводный) 1,68 (гептагидрат) |
| Цвет | От бесцветного до белого |
| Запах | Без запаха |
| Молярная масса | 120 366 г/моль |
| Плотность | 2,66 г/см³ (безводный) 1,68 г/см³ (гептагидрат) |
| Точка плавления | 1124°С (безводный) 150°С (гептагидрат) |
| Точка кипения | 1124°С (безводный) 150°С (гептагидрат) |
| Мигающая точка | Непригодный |
| Растворимость в воде | 71,6 г/100 мл (20°С) |
| Растворимость | Растворим в воде и этаноле |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| ПКа | 9,99 |
| рН | 6,0 – 8,0 (5% раствор) |
Безопасность и опасность сульфата магния
Сульфат магния обычно считается безопасным при правильном обращении. Однако он может представлять определенную опасность, если с ним не обращаться осторожно. Воздействие пыли сульфата магния может вызвать раздражение глаз, кожи и дыхательных путей. Проглатывание или введение большого количества сульфата магния может вызвать диарею, спазмы желудка и обезвоживание. При работе с сульфатом магния важно носить защитное оборудование, такое как перчатки и очки, чтобы избежать раздражения кожи и глаз. В случае проглатывания или воздействия немедленно обратитесь за медицинской помощью. Сульфат магния следует хранить в сухом прохладном месте, вдали от источников тепла и несовместимых материалов.
| Символы опасности | Никто |
| Описание безопасности | S22 – Не дышать пылью; S24/25 – Избегать контакта с кожей и глазами; S36 – Носите подходящую защитную одежду; S26 – При попадании в глаза немедленно промыть большим количеством воды и обратиться к врачу; S45 – В случае несчастного случая или плохого самочувствия немедленно обратитесь к врачу (по возможности покажите врачу этикетку). |
| Идентификаторы сети | ООН3077 |
| код ТН ВЭД | 28332100 |
| Класс опасности | 9 |
| Группа упаковки | III |
| Токсичность | LD50 (перорально, крыса) > 3000 мг/кг; ЛД50 (кожная, крыса) > 2000 мг/кг |
Методы синтеза сульфата магния
Существуют различные методы синтеза сульфата магния (MgSO4).
Распространенным методом является взаимодействие оксида или гидроксида магния с серной кислотой. Процесс включает добавление оксида или гидроксида магния к серной кислоте при перемешивании до полного растворения смеси. Соберите кристаллы магния MgSO4, выпарив раствор, чтобы удалить лишнюю воду.
Другой подход заключается в медленном добавлении карбоната магния в серную кислоту при перемешивании до полного растворения. Чтобы получить кристаллы магния MgSO4, профильтруйте полученный раствор от всех примесей и выпарите его.
Проведите реакцию магния с серной кислотой и нагревайте смесь до завершения реакции, затем профильтруйте и выпарите полученный раствор, чтобы получить кристаллы магния MgSO4.
Получить магний MgSO4 можно также путем реакции хлорида магния с натрием MgSO4. Процесс включает добавление хлорида магния к раствору натрия MgSO4, перемешивание полученной смеси и нагревание ее до образования кристаллов магния MgSO4.
Использование сульфата магния
Сульфат магния (MgSO4) имеет множество применений в различных областях. Некоторые из его применений включают в себя:
- Медицинское использование: используется для лечения эклампсии и преэклампсии во время беременности, а также для предотвращения судорог у пациентов с тяжелой астмой или гипомагниемией. Он служит слабительным и слабительным средством.
- Сельское хозяйство: используется в качестве удобрения из-за высокого содержания магния и серы. Фермеры используют его для устранения дефицита магния в почвах.
- Пищевая промышленность и производство напитков: используется в качестве пивоваренной соли при производстве пива для регулирования химического состава воды и улучшения вкуса. Пищевая промышленность использует его в качестве коагулянта при производстве тофу.
- Промышленное применение: Используется в качестве осушителя и осушителя, а также в качестве антипирена. Различные отрасли промышленности используют его при производстве текстиля, бумаги и химикатов.
- Уход за собой: люди используют сульфат магния в солях для ванн и ваннах для ног из-за его заявленной пользы для здоровья, включая уменьшение мышечной боли и скованности.
- Другое использование: Используется в производстве пигментов, взрывчатых веществ и при очистке металлов.
Вопросы:
Вопрос: Какая основа используется в зубной пасте?
Ответ: Наиболее часто используемой основой зубной пасты обычно является карбонат кальция или бикарбонат натрия. Эти основы помогают чистить зубы и удалять налет.
Вопрос: Для чего используется сульфат магния?
Ответ: Сульфат магния имеет множество применений, в том числе для лечения эклампсии и преэклампсии во время беременности, в качестве слабительного и слабительного средства, в качестве удобрения, в качестве соли для пивоварения, в качестве антипирена и в качестве высушивающего агента. Он также используется в производстве текстиля, бумаги и химикатов.
Вопрос: Растворим ли сульфат магния?
Ответ: Сульфат магния растворим в воде и спирте.
Вопрос: Растворим ли сульфат магния в воде?
Ответ: Да, сульфат магния хорошо растворим в воде, его растворимость составляет примерно 25,5 г/100 мл при комнатной температуре.
Вопрос: Для чего используется сульфат магния?
Ответ: Сульфат магния имеет различные применения и преимущества в зависимости от конкретного применения. Некоторые из его применений включают в себя медицинское лечение, удобрение, соль для пивоварения, антипирен и сушильный агент. В медицинских целях сульфат магния можно использовать для предотвращения судорог, лечения запоров и уменьшения мышечной боли и скованности.
