Гипохлорит магния (Mg(ClO)2) — химическое соединение, состоящее из магния, кислорода и хлора. Он используется в качестве дезинфицирующего средства, отбеливателя и химиката для очистки воды.
| Название ИЮПАК | Гипохлорит магния |
| Молекулярная формула | Mg(ClO)2 |
| Количество CAS | 10233-03-1 |
| Синонимы | Хлорат магния, магниевая соль хлорноватистой кислоты, оксихлорид магния, MagOCl |
| ИнЧИ | InChI=1S/Cl2O2.Mg/c1-3-2;/q-1;+2 |
Свойства гипохлорита магния
Формула гипохлорита магния
Гипохлорит магния имеет химическую формулу Mg(ClO)2, что означает, что он содержит один атом магния, два атома хлора и два атома кислорода на молекулу. Это белое твердое вещество со слабым запахом хлора, которое обычно используется в качестве дезинфицирующего средства и химиката для очистки воды.
Гипохлорит магния Молярная масса
Молярная масса Mg(ClO)2 составляет 127,21 г/моль. Это значение рассчитывается путем сложения атомных масс каждого элемента химической формулы, а именно магния (24,31 г/моль), хлора (35,45 г/моль) и кислорода (15,99 г/моль). моль), умноженные на соответствующие индексы.
Температура кипения гипохлорита магния
Mg(ClO)2 не имеет определенной температуры кипения, поскольку он разлагается до достижения точки кипения. При нагревании Mg(ClO)2 выделяет газообразный кислород, оставляя хлорид магния в виде твердого остатка.
Гипохлорит магния Температура плавления
Температура плавления Mg(ClO)2 составляет 100°С. При этой температуре твердые кристаллы Mg(ClO)2 превращаются в жидкость. Однако из-за его нестабильности при высоких температурах с ним рекомендуется обращаться осторожно.
Плотность гипохлорита магния г/мл
Плотность Mg(ClO)2 составляет 2,08 г/мл при комнатной температуре. Это означает, что один миллилитр Mg(ClO)2 имеет массу 2,08 грамма.
Гипохлорит магния Молекулярный вес
Молекулярная масса Mg(ClO)2 составляет 127,21 г/моль. Это сумма атомных весов всех элементов соединения, а именно магния, хлора и кислорода.
Структура гипохлорита магния
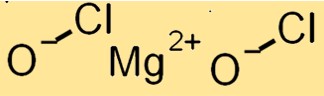
Mg(ClO)2 имеет кристаллическую структуру с моноклинной кристаллической системой. Он состоит из катионов Mg+2 и анионов ClO, которые удерживаются вместе ионными связями. Анионы ClO расположены в искаженном тетраэдрическом расположении вокруг катионов Mg+2.
Растворимость гипохлорита магния
Mg(ClO)2 мало растворим в воде, растворимость 14,6 г/100 мл при 20°С. В результате гидролиза ионов гипохлорита образует слабощелочной раствор в воде. Однако не рекомендуется растворять Mg(ClO)2 в воде, так как при этом может образоваться газообразный хлор, который токсичен и может нанести вред здоровью человека.
| Появление | Белый твердый |
| Удельный вес | 2,08 г/мл при 20°C |
| Цвет | Белый |
| Запах | Слегка хлорированный |
| Молярная масса | 127,21 г/моль |
| Плотность | 2,08 г/мл при 20°C |
| Точка плавления | 100°С |
| Точка кипения | Разлагается до достижения точки кипения |
| Мигающая точка | Непригодный |
| Растворимость в воде | Мало растворим (14,6 г/100 мл при 20°C) |
| Растворимость | Мало растворим в воде, растворим в кислотах |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | Непригодный |
| рН | Немного простое решение |
Безопасность и опасность гипохлорита магния
Mg(ClO)2 может быть опасен при неправильном обращении. Это сильный окислитель, который может бурно реагировать с некоторыми химическими веществами. Контакт с кожей, глазами и слизистыми оболочками может вызвать раздражение и ожоги. Вдыхание пыли или тумана может вызвать проблемы с дыханием. Также важно избегать смешивания Mg(ClO)2 с кислотами или другими хлорсодержащими соединениями, так как это может привести к образованию токсичного газообразного хлора. При работе с Mg(ClO)2 рекомендуется носить защитное оборудование, такое как перчатки и очки, и хранить его в сухом прохладном месте вдали от несовместимых химикатов.
| Символы опасности | Окислитель вредный |
| Описание безопасности | Беречь от источников тепла, искр и открытого огня. Не вдыхайте пыль или туман. Наденьте перчатки и защитные очки. |
| Идентификационные номера ООН | 1748 год |
| код ТН ВЭД | 2828.10.10 |
| Класс опасности | 5.1 (Окислитель), 6.1 (Токсично) |
| Группа упаковки | II |
| Токсичность | ЛД50 (перорально, крыса) – 290 мг/кг; LC50 (ингаляционно, крыса) – 2,07 мг/л/4ч; Раздражение кожи – Легкое; Раздражение глаз – Сильное |
Методы синтеза гипохлорита магния
Для синтеза Mg(ClO)2 наиболее часто используется метод взаимодействия оксида магния с газообразным хлором.
В одном методе для получения Mg(ClO)2 оксид магния необходимо смешать с газообразным хлором в присутствии воды. Во время экзотермической реакции необходим тщательный контроль, чтобы избежать образования нежелательных побочных продуктов.
Другой метод включает реакцию между гидроксидом магния и хлорноватистой кислотой. Для поддержания pH реакцию обычно проводят в растворе гидроксида натрия. Полученный раствор Mg(ClO)2 можно отделить фильтрованием и затем высушить после реакции.
Третий метод включает реакцию между карбонатом магния и хлорноватистой кислотой. В результате этой реакции образуется Mg(ClO)2 и углекислый газ. Чтобы избежать образования нежелательных побочных продуктов, необходимо внимательно следить за реакцией.
Независимо от используемого метода синтеза, важно обращаться с Mg(ClO)2 осторожно из-за его окислительных свойств и потенциальной опасности.
Использование гипохлорита магния
Mg(ClO)2 имеет несколько практических применений благодаря своим окислительным свойствам и способности выделять газообразный хлор. Вот некоторые распространенные варианты использования Mg(ClO)2:
- Очистка воды: обычно используется в качестве дезинфицирующего средства на водоочистных станциях для уничтожения вредных бактерий и вирусов.
- Отбеливатель: используется в качестве отбеливателя для текстиля, бумаги и других материалов.
- Плавательные бассейны: используется в качестве дезинфицирующего средства в плавательных бассейнах для поддержания хорошего химического состава воды.
- Контроль запаха: используется для контроля неприятных запахов на очистных сооружениях и в канализационных системах.
- Окислитель: используется в качестве окислителя при производстве различных химических веществ, таких как эпоксиды и кетоны.
- Сельское хозяйство: используется в сельском хозяйстве в качестве дезинфицирующего средства и пестицида для борьбы с грибковыми и бактериальными заболеваниями.
- Санитария: также используется в качестве дезинфицирующего средства для поверхностей и оборудования в больницах, на предприятиях пищевой промышленности и других объектах.
Вопросы:
Вопрос: Какова формула гипохлорита магния?
Ответ: Формула гипохлорита магния: Mg(ClO)2.
Вопрос: Каков уровень pH гипохлорита магния?
Ответ: Уровень pH Mg(ClO)2 зависит от его концентрации и может варьироваться. Однако раствор Mg(ClO)2 обычно имеет pH от 8 до 10.
Вопрос: Какова молекулярная формула гипохлорита магния?
A: Молекулярная формула гипохлорита магния: Mg(ClO)2.
Вопрос: Как называется Mg(ClO)2?
Ответ: Название Mg(ClO)2 — гипохлорит магния.
Вопрос: Mg(ClO)2 – кислота или основание?
Ответ: Mg(ClO)2 является основной солью и может действовать как слабое основание в водных растворах.
Вопрос: Является ли Mg(ClO)2 солью?
Ответ: Да, Mg(ClO)2 — это соль. Это белое кристаллическое соединение, хорошо растворимое в воде и содержащее как металл (магний), так и неметалл (хлор).
