Бисульфит магния (Mg(HSO3)2) представляет собой химическое соединение, состоящее из магния, серы и кислорода. Он широко используется в пищевой промышленности в качестве консерванта и антиоксиданта для предотвращения порчи и обесцвечивания.
| Название ИЮПАК | Гидросульфит магния |
| Молекулярная формула | Мг(HSO3)2 |
| Количество CAS | 13774-25-9 |
| Синонимы | бисульфит магния; гидросульфит магния; Магнезия бисульфит |
| ИнЧИ | InChI=1S/2H2O3S.Mg/c2 1-4(2)3;/h2 (H2,1,2,3);/q;;+2/p-2 |
Свойства бисульфита магния
Формула бисульфита магния
Химическая формула бисульфита магния: Mg(HSO3)2. Формула представляет количество атомов каждого элемента, присутствующего в молекуле соединения. Формула бисульфита магния необходима для определения химических реакций, которым может подвергаться это соединение.
бисульфит магния Молярная масса
Mg(HSO3)2 имеет молярную массу 186,45 г/моль. Это значение представляет собой вес одного моля соединения в граммах. Молярная масса соединения имеет важное значение для определения того, сколько вещества необходимо для проведения химических реакций. Молярная масса Mg(HSO3)2 рассчитывается путем сложения атомных масс каждого элемента в соединении. Магний имеет атомный вес 24,305 г/моль, сера имеет атомный вес 32,06 г/моль, а кислород имеет атомный вес 15,999 г/моль.
Температура кипения бисульфита магния
Mg(HSO3)2 не имеет температуры кипения, поскольку при нагревании разлагается. Однако он может выделять диоксид серы и триоксид серы при нагревании в присутствии кислоты. Эти газы могут раздражать дыхательную систему и вызывать серьезные последствия для здоровья при вдыхании. Поэтому важно осторожно обращаться с Mg(HSO3)2 и соблюдать меры безопасности при его использовании в промышленных процессах.
Бисульфит магния Температура плавления
Mg(HSO3)2 имеет температуру плавления 110°С. Это значение представляет собой температуру, при которой соединение переходит из твердого состояния в жидкое. Mg(HSO3)2 имеет низкую температуру плавления, что позволяет легко плавить его и использовать в различных промышленных процессах. Однако он может разлагаться при высоких температурах, что приводит к выделению вредных газов.
Плотность бисульфита магния г/мл
Mg(HSO3)2 имеет плотность 2,35 г/мл. Это значение представляет собой количество массы в граммах, присутствующее в одном миллилитре соединения. Плотность Mg(HSO3)2 больше плотности воды, имеющей плотность 1 г/мл. Высокая плотность Mg(HSO3)2 делает его полезным в различных применениях, в том числе в качестве консерванта и антиоксиданта в пищевой промышленности.
Молекулярный вес бисульфита магния
Mg(HSO3)2 имеет молекулярную массу 186,45 г/моль. Это значение представляет собой сумму атомных весов всех атомов соединения. Молекулярная масса Mg(HSO3)2 важна для определения количества соединения, необходимого для проведения химических реакций.
Структура бисульфита магния
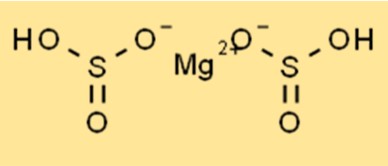
Mg(HSO3)2 имеет кристаллическую структуру и принадлежит к ромбической кристаллической системе. Соединение состоит из катионов магния (Mg2+) и бисульфит-анионов (HSO3-). Бисульфитные анионы имеют тетраэдрическую форму, а катионы магния — октаэдрическую. Кристаллическая структура Mg(HSO3)2 делает его стабильным и позволяет использовать его в различных целях, в том числе в качестве пищевого консерванта.
Растворимость бисульфита магния
Mg(HSO3)2 хорошо растворим в воде, его растворимость составляет около 64 г/100 мл при 20°C. Он также растворим в метаноле, но нерастворим в большинстве органических растворителей. Растворимость Mg(HSO3)2 может варьироваться в зависимости от таких факторов, как температура и pH.
| Появление | белый порошок |
| Удельный вес | 2,35 г/см3 |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 186,45 г/моль |
| Плотность | 2,35 г/мл |
| Точка плавления | 110°С |
| Точка кипения | Разложившийся |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в воде и этаноле |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | 1,91 |
| рН | 4,5 – 5,5 |
Безопасность и опасность бисульфита магния
Mg(HSO3)2 может представлять собой ряд рисков для здоровья и безопасности, если с ним не обращаться осторожно. Он может выделять диоксид серы и триоксид серы при нагревании или воздействии кислой среды. Эти газы при вдыхании могут вызвать раздражение дыхательных путей, кашель и одышку. Mg(HSO3)2 также может вызывать раздражение и покраснение кожи при контакте. При работе с Mg(HSO3)2 необходимо носить защитную одежду и оборудование, такое как перчатки и очки. Кроме того, его следует хранить в сухом прохладном месте, вдали от источников тепла и несовместимых материалов. Правильные процедуры обращения и хранения могут свести к минимуму риск опасностей, связанных с Mg(HSO3)2.
| Символы опасности | Си: Раздражает |
| Описание безопасности | Избегайте контакта с кожей и глазами. Носите защитную одежду и оборудование. Хранить вдали от источников тепла и несовместимых материалов. |
| Идентификационные номера ООН | ООН 2693 |
| код ТН ВЭД | 2831.10.00 |
| Класс опасности | 8 – Коррозионные вещества |
| Группа упаковки | III |
| Токсичность | Может вызвать раздражение кожи и глаз. Вреден при вдыхании или проглатывании. Может вызвать раздражение дыхательных путей и кашель. |
Методы синтеза бисульфита магния
Mg(HSO3)2 можно синтезировать различными методами, в том числе:
- Реакция гидроксида магния с диоксидом серы: При реакции гидроксида магния с диоксидом серы оба вещества реагируют с образованием Mg(HSO3)2 и воды.
- Прямая реакция оксида магния с диоксидом серы: при высоких температурах газообразный диоксид серы реагирует непосредственно с оксидом магния с образованием Mg(HSO3)2 и кислорода.
- Реакция сульфата магния с диоксидом серы: В присутствии восстановителя сульфат магния реагирует с газообразным диоксидом серы, в результате чего образуется Mg(HSO3)2.
- Карбонат магния с диоксидом серы: Реакция между карбонатом магния и газообразным диоксидом серы приводит к образованию Mg(HSO3)2 и диоксида углерода.
- Реакция оксида магния с серной кислотой и диоксидом серы. При взаимодействии оксида магния с серной кислотой и газообразным диоксидом серы в результате реакции образуется Mg(HSO3)2 и вода.
Использование бисульфита магния
Mg(HSO3)2 находит различное применение в различных отраслях промышленности. Вот некоторые распространенные приложения:
- Пищевая промышленность и производство напитков: используется в качестве консерванта в пищевой промышленности и производстве напитков для предотвращения окисления и роста микробов. Его обычно используют во фруктовых соках, вине и пиве.
- Водоочистка: используется при очистке воды в качестве восстановителя для удаления хлора и других окислителей. Эффективно контролирует запах и вкус воды.
- Текстильная промышленность: Используется в качестве отбеливателя в текстильной промышленности. Эффективно удаляет пятна и улучшает цвет тканей.
- Фармацевтическая промышленность: Используется в качестве восстановителя в фармацевтической промышленности. Он используется для преобразования нитрогрупп в аминогруппы в различных молекулах лекарств.
- Целлюлозно-бумажная промышленность: Используется в целлюлозно-бумажной промышленности в качестве отбеливающего агента. Он эффективен для удаления лигнина из древесной массы и улучшения блеска бумаги.
- Сельское хозяйство: используется в сельском хозяйстве в качестве удобрения для устранения дефицита магния в почве. Его также используют в качестве внекорневого удобрения для улучшения роста и урожайности растений.
Вопросы:
Вопрос: Каковы термодинамические свойства бисульфита магния?
A: Термодинамические свойства Mg(HSO3)2 включают температуру кипения 250°C, температуру плавления 70-72°C и плотность 1,84 г/мл.
Вопрос: Какова химическая формула бисульфита магния?
Ответ: Химическая формула бисульфита магния: Mg(HSO3)2.
Вопрос: Где я могу купить бисульфит магния?
Ответ: Mg(HSO3)2 можно приобрести у различных поставщиков и дистрибьюторов химической продукции. Обычно он доступен в больших и малых количествах. Некоторые онлайн-платформы, такие как Sigma Aldrich, Fisher Scientific и VWR International, также предлагают Mg(HSO3)2 для покупки. Важно убедиться, что поставщик имеет хорошую репутацию и что продукт соответствует стандартам, необходимым для предполагаемого применения.
