Бензиловый спирт представляет собой бесцветную жидкость с приятным ароматом. Он используется в качестве растворителя, консерванта и ароматизатора в различных продуктах личной гигиены и лекарствах.
| Название ИЮПАК | Бензиловый спирт |
| Молекулярная формула | C7H8O |
| Количество CAS | 100-51-6 |
| Синонимы | Фенилметанол, бензолметанол, гидрокситолуол, альфа-толуенол |
| ИнЧИ | ИнЧИ=1S/C7H8O/c8-6-7-4-2-1-3-5-7/h1-5.8H,6H2 |
Свойства бензилового спирта
Формула бензилового спирта
Формула бензолметанола: C7H8O. Он состоит из семи атомов углерода, восьми атомов водорода и одного атома кислорода. Эта химическая формула отражает расположение атомов в молекуле бензолметанола.
Бензиловый спирт Молярная масса
Молярную массу бензолметанола рассчитывают путем сложения атомных масс составляющих его элементов. Углерод имеет молярную массу 12,01 г/моль, водород имеет молярную массу 1,01 г/моль и кислород имеет молярную массу 16,00 г/моль. Сложив эти значения, можно определить молярную массу бензолметанола, равную 108,14 г/моль.
Температура кипения бензилового спирта
Бензолметанол имеет температуру кипения примерно 205°C (401°F). Это температура, при которой жидкость переходит в газообразное состояние, обычно при нагревании при стандартном атмосферном давлении. Температура кипения бензолметанола определяет его летучесть и полезность в различных применениях.
Температура плавления бензилового спирта
Температура плавления бензолметанола составляет примерно -15°C (5°F). Эта температура указывает на точку, в которой твердая форма бензолметанола превращается в жидкость при нагревании. Температура плавления является важной характеристикой при хранении и обращении с веществом.
Плотность бензилового спирта г/мл
Бензолметанол имеет плотность примерно 1,045 г/мл. Плотность представляет собой массу вещества в единице объема. Это свойство полезно при определении концентрации или чистоты бензолметанола в растворе.
Бензиловый спирт Молекулярный вес
Молекулярная масса бензолметанола составляет 108,14 г/моль. Это сумма атомных весов всех атомов молекулы. Молекулярный вес дает ценную информацию о массе соединения и облегчает расчеты, включающие стехиометрию и химические реакции.
Структура бензилового спирта
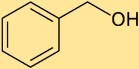
Структура бензолметанола состоит из бензольного кольца, присоединенного к гидроксильной группе (-ОН). Гидроксильная группа присоединена к атому углерода бензольного кольца. Эта структура придает бензолметанолу уникальные свойства и химическую активность.
Растворимость бензилового спирта
Бензолметанол в некоторой степени растворим в воде. Он проявляет умеренную растворимость благодаря наличию гидроксильной группы, которая позволяет образовывать водородные связи с молекулами воды. Однако бензолметанол более растворим в органических растворителях, таких как этанол и хлороформ. Растворимость бензолметанола влияет на его использование в качестве растворителя или добавки в различных отраслях промышленности.
| Появление | Бесцветная жидкость |
| Удельный вес | 1,045 г/мл |
| Цвет | Бесцветный |
| Запах | Приятный аромат |
| Молярная масса | 108,14 г/моль |
| Плотность | 1,045 г/мл |
| Точка плавления | -15°C (5°F) |
| Точка кипения | 205°С (401°Ф) |
| Мигающая точка | 93°С (199°Ф) |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в органических растворителях, таких как этанол и хлороформ. |
| Давление газа | 0,39 мм рт.ст. при 25°C |
| Плотность пара | 3,74 (воздух = 1) |
| пКа | 15,4 |
| рН | Около 7 |
Безопасность и опасность бензилового спирта
Бензолметанол представляет определенные соображения безопасности и опасности, которые необходимо принимать во внимание. При прямом контакте может вызвать раздражение глаз и кожи, поэтому рекомендуется использовать защитные меры, такие как перчатки и очки. Проглатывание или вдыхание большого количества бензолметанола может вызвать тошноту, головную боль и головокружение. Крайне важно обращаться с бензолметанолом в хорошо проветриваемом помещении, чтобы предотвратить накопление паров. Кроме того, длительное или неоднократное воздействие высоких концентраций бензолметанола потенциально может вызвать повреждение печени. Необходимо соблюдать надлежащие процедуры хранения и обращения, чтобы минимизировать риски и обеспечить безопасность в рабочей среде.
| Символы опасности | Раздражающий |
| Описание безопасности | Вреден при проглатывании, вызывает раздражение кожи и глаз. Используйте соответствующие меры защиты. |
| Идентификационные номера ООН | 1986 год |
| код ТН ВЭД | 29062100 |
| Класс опасности | 6.1 |
| Группа упаковки | III |
| Токсичность | Токсично для печени в высоких концентрациях. |
Методы синтеза бензилового спирта
Различные методы синтезируют бензолметанол.
Распространенным методом является каталитическое гидрирование бензальдегида . Бензальдегид реагирует с газообразным водородом в присутствии металлического катализатора, такого как палладий или платина, с образованием бензолметанола. Катализатор способствует восстановлению карбонильной группы бензальдегида с образованием бензолметанола.
Другой метод включает окисление толуола. Толуол сначала окисляется с образованием бензальдегида с использованием окислителя, такого как перманганат калия или хромовая кислота. Впоследствии восстановитель, такой как боргидрид натрия или газообразный водород, дополнительно восстанавливает бензальдегид с образованием бензолметанола.
Бензилхлорид реагирует с гидроксидом натрия или калия с образованием бензолметанола посредством синтеза эфира Вильямсона. Процесс включает обработку бензилхлорида раствором гидроксида, в результате чего образуется бензолметанол.
Эти методы синтеза предлагают различные пути получения бензолметанола, каждый из которых имеет свои преимущества и ограничения. Выбор метода зависит от таких факторов, как доступность сырья, желаемая чистота и конкретные требования к применению. При проведении процессов синтеза важно соблюдать меры предосторожности и обращаться с химикатами в контролируемой среде.
Использование бензилового спирта
Бензолметанол находит различное применение в различных отраслях промышленности благодаря своим универсальным свойствам. Вот некоторые распространенные приложения:
- Растворитель: Бензолметанол эффективно растворяет масла, смолы, красители и производные целлюлозы, что делает его идеальным растворителем для покрытий, красок и чернил.
- Консервант: Бензолметанол сохраняет широкий спектр продуктов, включая предметы личной гигиены, косметику и фармацевтические препараты, активно подавляя рост бактерий и грибков.
- Ароматический ингредиент: Бензолметанол придает приятный аромат и действует как ароматический ингредиент в духах, одеколонах и ароматизированных продуктах.
- Лекарства. В различных лекарствах, таких как мази, лосьоны и антисептические растворы для местного применения, в качестве активного фармацевтического ингредиента используется бензолметанол.
- Ароматизатор: Бензолметанол улучшает вкус пищевых продуктов и напитков в качестве активного ароматизатора.
- Чистящие средства. Растворяющие и антимикробные свойства бензолметанола делают его ценным ингредиентом чистящих, моющих и дезинфицирующих средств.
- Промышленное применение: Бензолметанол используется в промышленности в качестве растворителя и реакционной среды при производстве полимеров и других промышленных процессах.
- Текстильная промышленность: Бензолметанол облегчает процесс прядения синтетических волокон в текстильной промышленности.
- Химическое промежуточное соединение: Бензолметанол активно участвует в качестве промежуточного соединения в синтезе различных химических веществ, включая бензиловые эфиры, бензиловые эфиры и бензиламины.
- Применение в ветеринарии: В ветеринарии бензолметанол служит анестетиком и активно лечит ушные инфекции у животных.
Эти разнообразные применения подчеркивают важность и широкое применение бензилового спирта во многих отраслях промышленности.
Вопросы:
Вопрос: Что такое бензиловый спирт?
Ответ: Бензолметанол — бесцветная жидкость с приятным ароматом, обычно используемая в качестве растворителя, консерванта и ароматизатора в различных продуктах личной гигиены и лекарствах.
Вопрос: вреден ли бензиловый спирт для волос?
Ответ: Бензолметанол при использовании в соответствующих концентрациях, как правило, безопасен для волос и обычно встречается в средствах по уходу за волосами в качестве консерванта или ароматизатора.
Вопрос: Халялен ли бензиловый спирт?
Ответ: Халяльный статус бензолметанола зависит от его источника и производственного процесса. Если он получен из авторизованных источников и произведен в соответствии со стандартами Халяль, его можно считать халяльным.
Вопрос: Где я могу купить бензиловый спирт?
Ответ: Бензолметанол можно приобрести у различных источников, включая поставщиков химикатов, интернет-магазины, а также местные аптеки или магазины, торгующие косметическими ингредиентами.
Вопрос: Для чего используется бензиловый спирт?
Ответ: Бензолметанол используется в качестве растворителя, консерванта, ароматизатора и фармацевтического ингредиента в средствах личной гигиены, косметике, лекарствах и промышленном применении.
Вопрос: Толуол в бензиловый спирт?
Ответ: Толуол можно превратить в бензолметанол посредством двухстадийного процесса: окисления толуола до бензальдегида с последующим восстановлением бензальдегида до бензилового спирта.
Вопрос: От бензилхлорида к бензиловому спирту?
Ответ: Бензилхлорид можно превратить в бензолметанол, обработав его гидроксидом натрия или калия посредством синтеза эфира Вильямсона.
Вопрос: От анилина к бензиловому спирту?
Ответ: Анилин можно превратить в бензолметанол посредством ряда стадий, включающих восстановление анилина до бензиламина с последующим окислением бензиламина до бензилового спирта.
Вопрос: Бензолметанол в 2-фенилэтановую кислоту?
Ответ: Бензолметанол можно превратить в 2-фенилэтановую кислоту путем окисления с использованием сильных окислителей, таких как перманганат калия или хромовая кислота.
Вопрос: Как превратить бензальдегид в бензиловый спирт?
Ответ: Бензальдегид можно восстановить до бензолметанола с использованием восстановителей, таких как боргидрид натрия или газообразный водород, в присутствии катализатора.
Вопрос: Что более кислое: бензиловый спирт или фенол?
Ответ: Фенол более кислый, чем бензолметанол, из-за резонансной стабилизации иона фенокса, образующегося при депротонировании.
