Ацетат никеля с формулой Ni(CH3COO)2 представляет собой химическое соединение. Он используется в различных отраслях промышленности, включая гальванотехнику и синтез катализаторов, благодаря содержащимся в нем компонентам никеля и ацетата.
| Название ИЮПАК | ацетат никеля |
| Молекулярная формула | Ni(CH3COO)2 |
| Количество CAS | 373-02-4 |
| Синонимы | Никелевая соль уксусной кислоты, диацетат никеля, ацетат никеля |
| ИнЧИ | InChI=1S/2C2H4O2.Ni/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
Свойства ацетата никеля
Формула ацетата никеля
Химическая формула диацетата никеля: Ni(CH3COO)2. Это означает, что каждая молекула диацетата никеля содержит один атом Ni, связанный с двумя ионами CH3COO.
ацетат никеля Молярная масса
Молярная масса диацетата никеля составляет примерно 176,7 г/моль. Эта величина рассчитывается путем сложения атомных масс одного атома никеля и четырех атомов кислорода ацетат-ионов.
Температура кипения ацетата никеля
Диацетат никеля имеет температуру кипения около 140°C (284°F). При этой температуре соединение переходит из жидкого состояния в газообразное.
Температура плавления ацетата никеля
Температура плавления диацетата никеля составляет примерно 140°C (284°F). Это температура, при которой твердое соединение превращается в жидкость.
Плотность ацетата никеля г/мл
Диацетат никеля имеет плотность примерно 1,744 г/мл. Это значение плотности представляет собой массу соединения на единицу объема и обычно используется для характеристики жидкостей.
Молекулярный вес ацетата никеля
Молекулярная масса диацетата никеля, также называемая молекулярной массой, составляет 176,7 г/моль. Это значение рассчитывается путем сложения атомных весов всех атомов соединения.
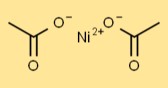
Структура ацетата никеля
В структуру диацетата никеля входит центральный атом Ni, связанный с двумя ионами CH3COO. Ионы ацетата способствуют координации вокруг атома никеля, придавая ему определенную геометрию.
Растворимость ацетата никеля
Диацетат никеля имеет умеренную растворимость в воде. Он может растворяться в воде с образованием раствора. Растворимость может меняться в зависимости от температуры и присутствия других веществ в растворе.
| Появление | Зеленый кристаллический порошок |
| Удельный вес | ~1744 г/мл |
| Цвет | Зеленый |
| Запах | Без запаха |
| Молярная масса | ~176,7 г/моль |
| Плотность | ~1744 г/мл |
| Точка плавления | ~140°С (284°Ф) |
| Точка кипения | ~140°С (284°Ф) |
| Мигающая точка | Непригодный |
| Растворимость в воде | Умеренный |
| Растворимость | Растворим в различных растворителях |
| Давление газа | Не очень хорошо документировано |
| Плотность пара | Не очень хорошо документировано |
| пКа | Не очень хорошо документировано |
| рН | Не очень хорошо документировано |
Ацетат никеля: безопасность и опасности
Диацетат никеля представляет потенциальную угрозу безопасности. Он может вызвать раздражение кожи, глаз и дыхательных путей при контакте или вдыхании. Избегайте проглатывания, так как это может вызвать вредные последствия. Необходима соответствующая вентиляция, чтобы избежать вдыхания его паров. При работе надевайте соответствующие средства защиты, такие как перчатки и очки. Утилизируйте его надлежащим образом и избегайте его попадания в окружающую среду. В случае воздействия обратитесь за медицинской помощью. Следуйте паспортам безопасности и инструкциям при использовании диацетата никеля, чтобы свести к минимуму риски, связанные с его обращением, хранением и утилизацией.
| Символы опасности | Опасность для здоровья |
| Описание безопасности | Вызывает раздражение кожи и глаз. Вреден при проглатывании или вдыхании. Избегать попадания в окружающую среду. Носите защитное снаряжение. В случае воздействия обратитесь за медицинской помощью. |
| Идентификационные номера ООН | UN3077 (Класс 9) |
| код ТН ВЭД | 2915.12.00 |
| Класс опасности | 9 (Разные опасные грузы) |
| Группа упаковки | III |
| Токсичность | Умеренная токсичность; может вызвать раздражение и повреждение при проглатывании, вдыхании или попадании на кожу или в глаза. |
Методы синтеза ацетата никеля
Диацетат никеля можно синтезировать различными методами. Распространенный подход заключается во взаимодействии оксида никеля (NiO) или карбоната никеля (NiCO3) с уксусной кислотой (CH3COOH) или ее производными. Эта реакция протекает в контролируемых условиях, в результате чего в качестве побочных продуктов образуются диацетат никеля и вода. Другой метод включает обработку металлического никеля или гидроксида никеля (Ni(OH)2) уксусной кислотой или ее солями, что способствует образованию диацетата никеля.
Кроме того, можно использовать процесс осаждения путем смешивания растворимой соли никеля, такой как хлорид никеля (NiCl2), с растворимой ацетатной солью. Эта смесь вызывает осаждение диацетата никеля из раствора, который затем можно отделить и собрать. Тщательная регулировка pH во время этого процесса помогает достичь оптимальных результатов.
Эти методы синтеза необходимы для производства диацетата никеля для различных применений, включая его использование в качестве катализатора и прекурсора в химических реакциях. Выбор метода зависит от таких факторов, как желаемая чистота, эффективность и масштаб производства.
Использование ацетата никеля
Диацетат никеля находит универсальное применение в нескольких отраслях промышленности благодаря своим уникальным свойствам и химическому составу. Некоторые важные области применения включают в себя:
- Гальваника: Диацетат никеля служит источником ионов никеля в процессах гальваники. Он облегчает нанесение тонкого слоя никеля на различные подложки, улучшая коррозионную стойкость и обеспечивая декоративную отделку.
- Синтез катализатора: химики используют его в качестве предшественника для создания катализаторов для множества химических реакций. Такие отрасли, как нефтехимия и фармацевтика, в значительной степени полагаются на никельсодержащие катализаторы.
- Текстильная промышленность: в процессах крашения тканей он помогает закрепить красители на тканевых волокнах, улучшить адгезию красителей и стойкость цвета.
- Лабораторный реагент: ученые используют диацетат никеля в качестве реагента для обнаружения и идентификации определенных соединений, что позволяет им проверять наличие определенных функциональных групп.
- Обработка поверхности: производители применяют его при обработке поверхности, например, при производстве печатных плат. Помогает сформировать защитный слой на медных поверхностях.
- Органический синтез. В различных реакциях органического синтеза диацетат никеля играет решающую роль в образовании связей углерод-углерод и углерод-гетероатом.
- Очистка газа: он играет ключевую роль в процессах очистки газа, особенно в удалении примесей, таких как сероводород, из промышленных газов.
- Аналитическая химия: Диацетат никеля является стандартным реагентом в аналитической химии, используемым для калибровки и контроля качества.
В целом, разнообразные применения диацетата никеля подчеркивают его важность в различных отраслях: от улучшения эстетики продукции до содействия критическим химическим превращениям и процессам.
Вопросы:
Вопрос: Можно ли смешать ацеталь и никель в одном контуре?
О: Смешивать ацеталь и никель в пряжке обычно не рекомендуется, так как ацеталь может вступать в реакцию с некоторыми металлами, потенциально вызывая коррозию и повреждение компонентов пряжки.
Вопрос: Какова правильная формула ионного соединения ацетата никеля?
Ответ: Правильная формула диацетата никеля, ионного соединения, — Ni(CH3COO)2.
Вопрос: Имеет ли ацетат никеля(ii) + бромид железа(ii) эмпирическую формулу?
Ответ: Диацетат никеля(II) и бромид железа(II) не образуют прямого соединения, поэтому эмпирическая формула неприменима.
Вопрос: Что такое ацеталь-никелевый водоблок?
О: Водоблок из ацеталя и никеля — это охлаждающий компонент, используемый в системах жидкостного охлаждения ПК, обычно изготовленный из ацеталевого пластика и имеющий никелированную поверхность.
Вопрос: Какова скорость реакции никеля и меди с уксусной кислотой?
Ответ: Никель и медь медленно реагируют с уксусной кислотой, выделяя газообразный водород и образуя соответствующие диацетатные соли.
Вопрос: Как можно получить ацетат никеля?
Ответ: Диацетат никеля можно получить путем взаимодействия оксида или карбоната никеля с уксусной кислотой с последующей кристаллизацией и очисткой.
Вопрос: Как удалить ацетат никеля?
О: Утилизируйте диацетат никеля как опасные отходы в соответствии с местными правилами. Важно проконсультироваться с органами по управлению отходами относительно соответствующих методов утилизации.
Вопрос: Какова формула ацетата никеля (ii)?
Ответ: Формула диацетата никеля(II) — Ni(CH3COO)2.
Вопрос: Растворим ли ацетат никеля?
Ответ: Да, диацетат никеля умеренно растворим в воде, образуя раствор, который можно использовать в различных целях.
