Аллилхлорид — прозрачная легковоспламеняющаяся жидкость с резким запахом. Его используют в производстве различных органических соединений и в качестве растворителя. Он может быть вреден для человека при вдыхании или проглатывании.
| Название ИЮПАК | 3-хлорпроп-1-ен |
| Молекулярная формула | C3H5Cl |
| Количество CAS | 107-05-1 |
| Синонимы | 2-пропенилхлорид, 3-хлорпропен, хлорпропен, аллилхлорид, 3-хлор-1-пропен, 1-хлор-2-пропен |
| ИнЧИ | InChI=1S/C3H5Cl/c1-2-3-4/h2H,1,3H2 |
Свойства аллилхлорида
Формула аллилхлорида
Химическая формула аллилхлорида: C3H5Cl. Это прозрачная бесцветная жидкость с резким запахом. Структура аллилхлорида состоит из молекулы пропена, ко второму атому углерода присоединен атом хлора. Это важный промежуточный продукт в производстве различных органических соединений, таких как эпоксиды, аллиламины и аллиловые спирты.
Аллилхлорид Молярная масса
Молярная масса 3-хлорпропена составляет 76,53 г/моль. Это рассчитывается путем сложения атомных масс углерода, водорода и хлора, которые составляют 12,01 г/моль, 1,01 г/моль и 35,45 г/моль соответственно. Молярная масса является важным свойством химического соединения, поскольку она используется для расчета количества вещества в данной массе.
Температура кипения аллилхлорида
Температура кипения 3-хлорпропена составляет 46,05°C (114,9°F). Это относительно мало по сравнению с другими органическими соединениями, что делает 3-хлорпропен летучим веществом. Низкая температура кипения также делает 3-хлорпропен полезным в промышленных процессах, поскольку его можно легко испарять и конденсировать для очистки.
Температура плавления аллилхлорида
Температура плавления 3-хлорпропена составляет -136°C (-213°F). Это очень низкая температура и означает, что 3-хлорпропен существует в жидкой форме при комнатной температуре. Однако когда 3-хлорпропен охлаждается до очень низких температур, он может затвердеть в белую кристаллическую форму.
Плотность аллилхлорида г/мл
Плотность 3-хлорпропена составляет 0,950 г/мл. Это означает, что 3-хлорпропен плотнее воды, плотность которой составляет 1 г/мл. Высокая плотность 3-хлорпропена делает его полезным для отделения его от других веществ с более низкой плотностью, таких как вода.
Аллилхлорид Молекулярный вес
Молекулярная масса 3-хлорпропена составляет 76,53 г/моль. Это значение рассчитывается путем сложения атомных весов всех атомов молекулы. Молекулярная масса важна для определения физических и химических свойств соединения.
Структура аллилхлорида
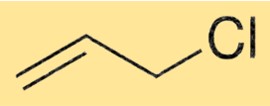
Структура 3-хлорпропена состоит из молекулы пропилена с атомом хлора, присоединенным ко второму атому углерода. При этом образуется винильная группа, которая является функциональной группой в органической химии. Винильная группа отвечает за реакционную способность 3-хлорпропена в различных химических реакциях.
Растворимость аллилхлорида
3-Хлорпропен растворим во многих органических растворителях, таких как эфир и бензол, но нерастворим в воде. Растворимость 3-хлорпропена в различных растворителях обусловлена его полярной природой. Полярность 3-хлорпропена определяется разницей электроотрицательности между связью углерод-водород и связью углерод-хлор.
| Появление | Прозрачная бесцветная жидкость |
| Удельная плотность | 0,950 г/мл |
| Цвет | Бесцветный |
| Запах | Акко |
| Молярная масса | 76,53 г/моль |
| Плотность | 0,950 г/мл |
| Точка плавления | -136°С (-213°Ф) |
| Точка кипения | 46,05°С (114,9°Ф) |
| Мигающая точка | -13°С (9°Ф) |
| Растворимость в воде | < 1 г/л |
| Растворимость | Растворим в органических растворителях |
| Давление газа | 21,5 кПа при 20°C |
| Плотность пара | 2,64 (воздух = 1) |
| пКа | 9.18 |
| рН | Не применимо (pH определяется только для водных растворов) |
Безопасность и опасность аллилхлорида
3-Хлорпропен — высокотоксичное и коррозийное вещество. При попадании он может вызвать серьезные ожоги кожи и повреждения глаз, а также может быть опасен при вдыхании или проглатывании. Он также легко воспламеняется и может бурно реагировать с некоторыми соединениями. При работе с 3-хлорпропеном следует соблюдать надлежащие меры безопасности, включая ношение защитной одежды, перчаток и средств защиты глаз. Хранить следует в прохладном, сухом и хорошо проветриваемом месте, вдали от источников тепла и воспламенения. При попадании или проглатывании следует немедленно обратиться за медицинской помощью. Важно соблюдать надлежащие протоколы безопасности, чтобы избежать несчастных случаев и травм при работе с 3-хлорпропеном.
| Символы опасности | Т, С |
| Описание безопасности | Легковоспламеняющийся, токсичный и коррозионный. Вызывает серьезные ожоги кожи и повреждения глаз. Вреден при вдыхании или проглатывании. |
| Идентификационные номера ООН | ООН 1100 |
| код ТН ВЭД | 2903.39.90 |
| Класс опасности | Класс 3 (Воспламеняющиеся жидкости), Класс 6.1 (Токсичные вещества), Класс 8 (Коррозионные вещества) |
| Группа упаковки | II |
| Токсичность | LD50 = 250 мг/кг (перорально, крыса); LC50 = 1220 ppm (ингаляция, крыса, 4 часа) |
Методы синтеза аллилхлорида
Существует несколько методов синтеза 3-хлорпропена.
Одним из наиболее распространенных методов является добавление газообразного хлористого водорода к аллиловому спирту в присутствии катализатора. Другой метод включает реакцию пропилена с газообразным хлором в присутствии катализатора с образованием 3-хлорпропена.
Чтобы получить 3-хлорпропен, аллиловый спирт можно подвергнуть реакции с тионилхлоридом или трихлоридом фосфора. Эта реакция включает преобразование спирта в соответствующий хлорид посредством реакции нуклеофильного замещения.
Третий способ получения 3-хлорпропена включает реакцию аллилбромида с хлоридом натрия в присутствии медного порошка. Химики часто используют этот метод, когда у них есть свободный доступ к бромистому аллилу, но нет 3-хлорпропена.
Другой метод синтеза 3-хлорпропена включает реакцию аллилового спирта с газообразным хлористым водородом в присутствии дегидратирующего агента, такого как хлорид цинка. Химики часто используют этот метод для получения 3-хлорпропена с высоким выходом и чистотой.
Использование аллилхлорида
Благодаря своим уникальным свойствам 3-хлорпропен имеет несколько важных применений в различных отраслях промышленности:
- Производство аллильных соединений: 3-хлорпропен служит предшественником различных аллильных соединений, таких как аллиловый спирт, аллиламин и аллиловые эфиры. Производство фармацевтических препаратов, парфюмерии и ароматизаторов обычно предполагает использование аллильных соединений.
- Производство полимеров: производители используют 3-хлорпропен в качестве мономера для производства различных полимеров, таких как поли3-хлорпропен и аллилдигликолькарбонат.
- Растворитель: используется в качестве растворителя различных органических соединений из-за низкой температуры кипения и высокой полярности.
- Пестицид: используется в качестве фумиганта и стерилизатора почвы в сельском хозяйстве для борьбы с вредителями и сорняками.
- Производство красителей и пигментов: используются при производстве красителей и пигментов для текстильной и лакокрасочной промышленности.
- Нефтяная и газовая промышленность: Также используется в нефтегазовой промышленности в качестве ингибитора коррозии, смазочных материалов и добавок к буровым растворам.
Вопросы:
Вопрос: Почему аллилхлорид вступает в реакции SN1, хотя он является галогенидом 1°?
A: 3-Хлорпропен вступает в реакции SN1 из-за стабильности промежуточного карбокатиона, который резонансно стабилизируется аллильной группой.
Вопрос: Что происходит с аллилхлоридом в реакции SN2?
A: В реакции SN2 нуклеофил атакует аллильный углерод сзади, что приводит к изменению стереохимии и образованию соответствующего аллилового спирта или амина.
Вопрос: Является ли аллилхлорид первичным, вторичным или третичным?
Ответ: 3-хлорпропен является первичным галогенидом.
Вопрос: Какая из следующих реакций протекает быстрее: AcO- + 3-хлорпропен или MeO- + 3-хлорпропен? А: МеО-+3-хлорпропен образуется быстрее, чем АсО-+3-хлорпропен, из-за стерического затруднения, вызванного большей ацетильной группой последнего.
Вопрос: Является ли аллилхлорид первичным винилгалогенидом?
Ответ: Да, 3-хлорпропен является первичным винилгалогенидом.
Вопрос: Как можно получить эпихлоргидрин из аллилхлорида?
Ответ: Эпихлоргидрин можно получить из 3-хлорпропена реакцией эпоксидирования с использованием смеси гипохлорита натрия и соляной кислоты.
