Щавелевая кислота — органическое соединение без цвета и запаха, содержащееся во многих овощах и фруктах. Он используется в различных промышленных процессах, таких как очистка и полировка металлов. Он также может быть вредным, если его проглотить в больших количествах.
| Название ИЮПАК | Этандиовая кислота |
| Молекулярная формула | C2H2O4 |
| Количество CAS | 144-62-7 |
| Синонимы | Этандиовая кислота, сахарная кислота, оксириновая кислота, отбеливатель древесины, щавелевая кислота, дикарбоновая кислота C2 и т. д. |
| ИнЧИ | InChI=1S/C2H2O4/c3-1(4)2(5)6/h(H,3.4)(H,5.6) |
Свойства щавелевой кислоты
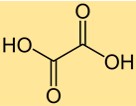
Формула щавелевой кислоты
Химическая формула щавелевой кислоты: C2H2O4. Он состоит из двух атомов углерода, двух атомов кислорода и четырех атомов водорода. Формула щавелевой кислоты важна во многих химических расчетах, таких как определение молекулярной массы или количества молей щавелевой кислоты в образце. Формула также дает информацию о соотношении атомов, присутствующих в молекуле.
Молярная масса of Щавелевая кислота
Молярная масса этандиовой кислоты составляет 90,03 г/моль. Это рассчитывается путем сложения атомных масс каждого элемента, присутствующего в молекуле (2 атома углерода, 2 атома кислорода и 4 атома водорода). Молярная масса этандиовой кислоты важна во многих химических расчетах, например, при определении количества этандиовой кислоты, необходимого для конкретной реакции, или концентрации раствора этандиовой кислоты.
Температура кипения щавелевой кислоты
Температура кипения этандиовой кислоты составляет 365°С. При этой температуре жидкая фаза этандиовой кислоты переходит в паровую фазу и переходит в газ. На температуру кипения этандиовой кислоты влияют различные факторы, такие как давление, чистота и наличие примесей. Щавелевая кислота относительно стабильна при высоких температурах, но длительное воздействие тепла может привести к ее разложению с образованием углекислого газа и воды.
Температура плавления щавелевой кислоты
Температура плавления этандиовой кислоты составляет 189-191°С. Это температура, при которой твердая этандиовая кислота начинает разжижаться и переходить в жидкость. На температуру плавления этандиовой кислоты могут влиять различные факторы, такие как чистота, давление и кристаллическая структура. Температура плавления является важным физическим свойством этандиовой кислоты, поскольку помогает определить ее пригодность для различных применений.
Плотность щавелевой кислоты г/мл
Плотность этандиовой кислоты составляет 1,90 г/мл. Это означает, что один миллилитр этандиовой кислоты весит 1,90 грамма. Плотность этандиовой кислоты может меняться в зависимости от температуры, давления и концентрации раствора. Плотность этандиовой кислоты является важным свойством, используемым во многих химических и промышленных процессах, таких как определение количества этандиовой кислоты, необходимой для реакции, или расчет объема раствора.
Щавелевая кислота Молекулярный вес
Молекулярная масса этандиовой кислоты составляет 90,03 г/моль. Это сумма атомных весов всех атомов молекулы. Молекулярная масса этандиовой кислоты используется в различных химических расчетах, таких как определение количества молей этандиовой кислоты в данном образце или концентрации раствора этандиовой кислоты.
Структура щавелевой кислоты
Щавелевая кислота имеет структуру дикарбоновой кислоты с двумя карбоксильными группами (-СООН), присоединенными к центральному атому углерода. Молекула имеет плоскую структуру с двумя карбоксильными группами, ориентированными перпендикулярно. Структура щавелевой кислоты делает ее сильной органической кислотой, способной отдавать два протона в растворе.
| Появление | Белый кристаллический порошок |
| Удельный вес | 1,90 г/мл при 20°C |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Молярная масса | 90,03 г/моль |
| Плотность | 1,90 г/мл при 20°C |
| Точка плавления | 189-191°С |
| Точка кипения | 365°С |
| Мигающая точка | Непригодный |
| Растворимость в воде | 90 г/л при 20°C |
| Растворимость | Растворим в воде, спирте, эфире и глицерине. |
| Давление газа | 0,0001 мм рт.ст. при 25°C |
| Плотность пара | 3,3 (воздух=1) |
| пКа | рКа1=1,25, рКа2=4,14 |
| рН | 1,2 (0,1М растворов) |
Безопасность и вред щавелевой кислоты
Щавелевая кислота — опасное вещество, которое может нанести вред при неправильном обращении. Он может вызывать коррозию кожи, глаз и дыхательных путей, а также вызывать раздражение или ожоги при контакте. Вдыхание пыли или паров этандиовой кислоты также может вызвать раздражение дыхательных путей и повреждение легких. При работе с этандиовой кислотой важно носить соответствующие средства индивидуальной защиты, такие как перчатки, очки и респиратор. Кроме того, его следует хранить в сухом прохладном месте, вдали от источников тепла и возгорания. Утилизация этандиовой кислоты должна осуществляться в соответствии с местными правилами.
| Символы опасности | Т, С |
| Описание безопасности | Избегайте контакта с кожей и глазами. Надевайте соответствующую защитную одежду, перчатки и средства защиты глаз/лица. При попадании в глаза немедленно промыть большим количеством воды и промыть врачу. В случае несчастного случая или плохого самочувствия немедленно обратитесь за медицинской помощью (по возможности покажите этикетку). |
| Идентификаторы сети | ООН3261 |
| код ТН ВЭД | 291711 |
| Класс опасности | 8 |
| Группа упаковки | III |
| Токсичность | Пероральная LD50: 750 мг/кг (крыса), кожная LD50: 1000 мг/кг (кролик), ингаляционная LC50: 1100 частей на миллион/8 часов (крыса) |
Методы синтеза щавелевой кислоты
Существует несколько методов синтеза щавелевой кислоты (этандиовой кислоты), включая окисление углеводов, окисление этиленгликоля и реакцию оксида углерода с гидроксидом натрия .
Одним из наиболее распространенных методов является окисление углеводов с помощью азотной кислоты. При гидролизе углеводов образуются моносахариды, которые мы затем окисляем с помощью азотной кислоты и такого катализатора, как пентоксид ванадия. Обработав полученную смесь карбонатом кальция, обрабатываем ее серной кислотой для выделения этандиовой кислоты.
Другим методом синтеза этандиовой кислоты является окисление этиленгликоля с использованием азотной кислоты и такого катализатора, как платина или палладий. Мы окисляем этиленгликоль до гликолевой кислоты, а затем дополнительно окисляем его до этандиовой кислоты с использованием азотной кислоты и катализатора. Затем мы обрабатываем полученную смесь карбонатом кальция и серной кислотой, чтобы высвободить этандиовую кислоту.
Третий метод синтеза этандиовой кислоты включает реакцию монооксида углерода с гидроксидом натрия в присутствии такого катализатора, как никель или кобальт. В результате реакции монооксида углерода с гидроксидом натрия образуется формиат натрия, который затем взаимодействуют с гидроксидом натрия с образованием оксалата натрия. Обработка оксалата натрия серной кислотой приводит к высвобождению этандиовой кислоты.
Использование щавелевой кислоты
Щавелевая кислота имеет множество применений в различных отраслях промышленности благодаря своим уникальным химическим свойствам. Вот некоторые распространенные способы применения этандиовой кислоты:
- Удаление ржавчины: обычно используется в качестве средства для удаления ржавчины с металлических поверхностей, включая железо, сталь и медь.
- Отбеливатель: используется в текстильной промышленности для отбеливания тканей и волокон.
- Деревообработка: используется для удаления пятен с древесины, таких как пятна от воды или пятна, вызванные железом или другими металлами.
- Чистящее средство: используется в качестве чистящего средства для различных поверхностей, включая сантехнику в ванной и кухне, столешницы и полы.
- Хелатирующий агент: также используется в качестве хелатирующего агента в различных промышленных процессах, включая производство керамики и фармацевтических препаратов.
- Травитель: используется в качестве травителя в электронной промышленности для удаления оксидов металлов и примесей с поверхностей полупроводников.
- Фотография: используется в фотографии в качестве проявителя для определенных типов фотопленки.
- Медицинское использование: используется в некоторых медицинских целях, включая удаление отложений кальция из организма и лечение инфекций мочевыводящих путей.
Вопросы:
Вопрос: Где я могу купить щавелевую кислоту рядом со мной?
О: Щавелевую кислоту можно купить во многих хозяйственных магазинах, магазинах товаров для дома и в интернет-магазинах. Его также можно приобрести в специализированных магазинах химической продукции.
Вопрос: Как нейтрализовать щавелевую кислоту в пище?
Ответ: Щавелевую кислоту можно нейтрализовать в пищевых продуктах, добавив в нее вещества, богатые кальцием, например молоко или сыр. Кальций связывается с щавелевой кислотой, уменьшая ее воздействие на организм.
Вопрос: Какова массовая доля углерода в щавелевой кислоте H2C2O4?
A: Молекулярная масса щавелевой кислоты составляет 90,03 г/моль. Масса углерода в одном моле этандиовой кислоты равна 24,02 г. Следовательно, массовая доля углерода в этандиовой кислоте равна (24,02 г/90,03 г) x 100% = 26,66%.
Вопрос: Как снизить содержание щавелевой кислоты в шпинате?
Ответ: Уровень щавелевой кислоты в шпинате можно снизить, если его бланшировать перед употреблением. Этот процесс включает в себя непродолжительное кипячение шпината, а затем его охлаждение в ледяной воде, чтобы уменьшить содержание этандиовой кислоты.
Вопрос: Какова массовая доля углерода в щавелевой кислоте H2C2O4?
A: Молекулярная масса щавелевой кислоты составляет 90,03 г/моль. Масса углерода в одном моле этандиовой кислоты равна 24,02 г. Следовательно, массовая доля углерода в этандиовой кислоте равна (24,02 г/90,03 г) x 100% = 26,66%.
Вопрос: H2C2O4 – это кислота или основание?
Ответ: H2C2O4 — это кислота, также известная как этандиовая кислота.
Вопрос: Каков порядок реакции H2C2O4? Ответ: Порядок реакции H2C2O4 зависит от конкретной рассматриваемой реакции. Его можно определить экспериментально с использованием таких методов, как метод начальной скорости или законы интегральной скорости.
