Фосген — токсичный газ, используемый в промышленных процессах и в войне. Его вдыхание представляет серьезную угрозу для здоровья, вызывая повреждение органов дыхания и может привести к летальному исходу.
| Название ИЮПАК | Карбонилдихлорид |
| Молекулярная формула | COCl2 |
| Количество CAS | 75-44-5 |
| Синонимы | Дихлорид углерода, газообразный фосген, хлористый карбонил |
| ИнЧИ | InChI=1S/CCl2O/c2-1(3)4 |
Свойства фосгена
Фосгенная формула
Химическая формула фосгена или дихлорида углерода — COCl2. Он состоит из одного атома углерода (С), одного атома кислорода (О) и двух атомов хлора (Cl). Этот молекулярный состав важен для понимания его свойств и реакций.
фосген Молярная масса
Молярная масса дихлорида углерода составляет примерно 98,92 г/моль. Он рассчитывается путем сложения атомных масс его составляющих: углерода (12,01 г/моль), кислорода (16,00 г/моль) и хлора (35,45 г/моль каждый).
Температура кипения фосгена
Дихлорид углерода имеет относительно низкую температуру кипения, около -23,3°C (-9,94°F). При этой температуре он переходит из жидкого состояния в газообразное, что имеет решающее значение для его применения в различных промышленных процессах.
Точка плавления фосгена
Температура плавления углекислого газа довольно низкая, около -118,3°C (-180,94°F). При этой температуре твердая форма углекислого газа превращается в жидкость. Понимание этого свойства важно для безопасного обращения с дихлоридом углерода.
Плотность фосгена г/мл
Дихлорид углерода имеет плотность примерно 1,432 г/мл при комнатной температуре (25°C или 77°F). Это свойство имеет решающее значение для определения его поведения и взаимодействия с другими веществами.
Молекулярный вес фосгена
Молекулярная масса дихлорида углерода составляет 98,92 г/моль. Это значение имеет жизненно важное значение для различных расчетов в химии, включая стехиометрию и определение количества углекислого газа, необходимого для реакций.
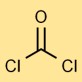
Структура фосгена
Дихлорид углерода имеет линейную молекулярную структуру, в которой атом углерода связан двойной связью с атомом кислорода и одинарной связью с каждым атомом хлора. Такое расположение влияет на его отзывчивость и стабильность.
Растворимость фосгена
Дихлорид углерода плохо растворим в воде, в жидкости растворяется лишь небольшое количество газа. Однако он может вступать в реакцию с водой с образованием соляной кислоты и углекислого газа, что делает его опасным в водной среде.
Понимание этих свойств дихлорида углерода необходимо для безопасного обращения и использования этого химического вещества в промышленных целях и других условиях. При обращении с этим токсичным и химически активным соединением всегда следует принимать надлежащие меры предосторожности, чтобы предотвратить несчастные случаи и опасность для здоровья.
| Появление | Бесцветный газ |
| Удельный вес | 3,428 (газ) |
| Цвет | Н/Д |
| Запах | Удушающий, жгучий |
| Молярная масса | 98,92 г/моль |
| Плотность | 1432 г/мл (жидкость) |
| Точка плавления | -118,3°C (-180,94°F) |
| Точка кипения | -23,3°C (-9,94°F) |
| Мигающая точка | Н/Д |
| Растворимость в воде | Реагирует с водой |
| Растворимость | Реагирует с водой с образованием соляной кислоты и диоксида углерода. |
| Давление газа | 736 мм рт.ст. (25°С) |
| Плотность пара | 2,98 (воздух = 1) |
| пКа | Н/Д |
| рН | Н/Д |
Эти физико-химические свойства предоставляют важную информацию о дихлориде углерода, облегчая безопасное обращение с ним и понимание его поведения в различных средах.
Безопасность и опасность фосгена
Дихлорид углерода представляет значительную угрозу безопасности из-за своей токсичности и реакционной способности. При работе с дихлоридом углерода надевайте соответствующие средства индивидуальной защиты (СИЗ), включая средства защиты органов дыхания, перчатки и средства защиты глаз. Обеспечьте достаточную вентиляцию в рабочих помещениях, чтобы избежать воздействия при вдыхании. Избегайте попадания на кожу и в глаза, так как это может вызвать серьезное раздражение и ожоги. Углекислый газ не имеет запаха, что затрудняет его обнаружение. Поэтому устройства мониторинга имеют решающее значение. В случае воздействия немедленно обратитесь за медицинской помощью. Храните и транспортируйте дихлорид углерода безопасно, в соответствии с правилами и передовыми практиками. Понимание его опасности имеет важное значение для предотвращения несчастных случаев и защиты здоровья человека и окружающей среды.
| Символы опасности | Череп и кости |
| Описание безопасности | Высокотоксичный газ. Обращайтесь с особой осторожностью. Используйте соответствующие средства индивидуальной защиты. Избегайте вдыхания и контакта с кожей. |
| Идентификационные номера ООН | ООН1076 |
| код ТН ВЭД | 2812.10.0000 |
| Класс опасности | 2.3 (Токсичный газ) |
| Группа упаковки | я |
| Токсичность | Фосген очень токсичен и может быть смертельным при вдыхании или попадании на кожу. Используйте строгие меры безопасности. |
Понимание аспектов риска и безопасности дихлорида углерода имеет решающее значение для безопасного обращения и предотвращения несчастных случаев. Он очень токсичен и представляет значительный риск для здоровья, поэтому необходимы надлежащие процедуры безопасности и меры предосторожности.
Методы синтеза фосгена
Несколько методов позволяют синтезировать дихлорид углерода.
Распространенным подходом является «процесс Дикона», в котором газообразный хлор реагирует с окисью углерода при повышенных температурах в присутствии подходящего катализатора, такого как хлорид меди (II) . Другой метод включает «прямое хлорирование» окиси углерода газообразным хлором, чему способствуют хлориды железа или других металлов в качестве катализаторов.
Производство дихлорида углерода включает «окислительное карбонилирование» хлористого метилена или хлористого метила с использованием кислорода и металлического катализатора, такого как хлорид меди. Другим методом синтеза дихлорида углерода является «путь мочевины», при котором дихлорид углерода образуется в качестве побочного продукта при производстве мочевины.
Однако важно отметить, что дихлорид углерода — очень опасное вещество, и его синтез требует предельной осторожности и опыта. Рабочие должны выполнять эти процессы в хорошо контролируемых промышленных условиях со строгими мерами безопасности и защитным оборудованием, чтобы избежать воздействия токсичных газов и обеспечить свою безопасность и безопасность окружающей среды.
Использование фосгена
Дихлорид углерода имеет различные промышленные применения благодаря своим уникальным свойствам, но важно отметить, что к его использованию следует относиться с особой осторожностью из-за его токсичного характера. Вот некоторые из его применений:
- Химические промежуточные продукты: дихлорид углерода помогает производить несколько основных химикатов, включая изоцианаты, которые играют важную роль в производстве пенополиуретанов, покрытий и клеев.
- Производство пестицидов: дихлорид углерода облегчает синтез некоторых пестицидов и гербицидов, тем самым способствуя защите сельскохозяйственных культур и борьбе с вредителями.
- Производство поликарбоната. Углекислый газ является важнейшим компонентом в производстве поликарбонатного пластика, который используется в широком спектре продукции: от очков до бутылок для воды.
- Текстильная промышленность: Дихлорид углерода используется в производстве определенных красителей и других химикатов, используемых в текстильной промышленности.
- Производство пены: углекислый газ играет ключевую роль в производстве пенопластов, в том числе некоторых типов пенопласта, используемого в изоляции.
- Фармацевтика: Дихлорид углерода действует как промежуточный химический продукт при производстве некоторых фармацевтических препаратов.
- Лабораторные исследования: исследователи иногда используют дихлорид углерода в лабораторных экспериментах.
- Производство синтетического каучука: Углекислый газ является неотъемлемой частью производства некоторых синтетических каучуков.
- Очистка воды: дихлорид углерода раньше использовался в небольших количествах для очистки воды, но в настоящее время для этой цели чаще используются более безопасные альтернативы.
Хотя дихлорид углерода имеет важное промышленное применение, его высокая токсичность и опасные свойства требуют строгих мер безопасности при обращении, хранении и транспортировке для предотвращения несчастных случаев и обеспечения благополучия рабочих и людей. окружающая среда.
Вопросы:
Вопрос: Что газ фосген делает с человеком?
Ответ: Углекислый газ может вызвать повреждение дыхательных путей, что приведет к затруднению дыхания и потенциально смертельному отеку легких.
Вопрос: Что такое фосген?
Ответ: Углекислый газ — высокотоксичное химическое соединение, используемое в различных промышленных процессах.
Вопрос: Что такое фосген?
Ответ: Газообразный дихлорид углерода — это газообразная форма химического соединения, известного своим удушающим и токсическим воздействием на дыхательную систему.
Вопрос: Что фосген делает с организмом?
Ответ: Углекислый газ может повредить легкие, вызывая скопление жидкости и серьезное расстройство дыхания.
Вопрос: Как часто Гриньяр будет реагировать с фосгеном?
Ответ: Реактив Гриньяра реагирует с дихлоридом углерода только один раз, образуя кетон.
Вопрос: Какой орган человека поражает газообразный хлор и фосген?
Ответ: Газы хлора и дихлорида углерода в основном поражают легкие.
Вопрос: Как вас убивает фосген?
Ответ: Углекислый газ вызывает сильное раздражение легких, приводящее к скоплению жидкости и удушью.
Вопрос: Кто изобрел газ фосген?
Ответ: Углекислый газ был открыт британским химиком Джоном Дэви в 1812 году.
Вопрос: Воздействие углекислого газа?
Ответ: Углекислый газ может вызвать повреждение дыхательных путей, отек легких и, в тяжелых случаях, смерть.
Вопрос: Структура углекислого газа по Льюису?
Ответ: Структура Льюиса дихлорида углерода состоит из углерода, дважды связанного с кислородом и одинарной связи с двумя атомами хлора.
Вопрос: Углекислый газ во время Первой мировой войны?
Ответ: Дихлорид углерода использовался в качестве химического оружия во время Первой мировой войны, оказывая разрушительное воздействие на солдат.
Вопрос: Когда впервые был использован газообразный фосген?
Ответ: Газообразный дихлорид углерода впервые был использован в качестве химического оружия во время Первой мировой войны в 1915 году.
Вопрос: Откуда берется фосген?
Ответ: Углекислый газ обычно получается путем реакции хлора с окисью углерода или другими углеродосодержащими соединениями.
