Тионилхлорид — химическое соединение, используемое в различных отраслях промышленности. Реагирует со спиртами и карбоновыми кислотами с образованием соответствующих хлоридов и сульфурилхлорида соответственно.
| Название ИЮПАК | Тионилхлорид |
| Молекулярная формула | SOCl₂ |
| Количество CAS | 7719-09-7 |
| Синонимы | Дихлорид серы, оксихлорид серы, дихлорид тионила |
| ИнЧИ | ИнХИ=1S/Cl2OS/c1-4(2)3 |
Свойства тионилхлорида
Формула тионилхлорида
Формула тионилдихлорида — SOCl₂, что представляет собой один атом серы, связанный с двумя атомами хлора. Это химическое соединение, широко используемое в различных отраслях промышленности.
Молярная масса тионилхлорида
Тионилдихлорид имеет молярную массу примерно 118,97 грамм на моль. Молярная масса определяется путем сложения атомных масс составляющих его элементов.
Температура кипения тионилхлорида
Тионилдихлорид имеет температуру кипения примерно 79,6 градусов Цельсия. Это температура, при которой жидкая форма дихлорида тионила переходит в газообразное состояние.
Температура плавления тионилхлорида
Температура плавления тионилдихлорида составляет примерно -104,5 градусов Цельсия. Это температура, при которой твердая форма тионилдихлорида переходит в жидкое состояние.
Плотность тионилхлорида, г/мл
Тионилдихлорид имеет плотность примерно 1,64 грамма на миллилитр. Плотность является мерой массы единицы объема и является важной характеристикой вещества.
Тионилхлорид Молекулярный вес
Молекулярная масса тионилдихлорида составляет примерно 118,97 грамм на моль. Его рассчитывают путем сложения атомных масс серы, хлора и кислорода.
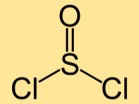
Структура тионилхлорида
Структура тионилдихлорида состоит из атома серы, связанного с двумя атомами хлора. Атомы серы и хлора расположены линейно, образуя молекулу изогнутой формы.
Растворимость тионилхлорида
Тионилдихлорид плохо растворяется в воде, но легко растворяется в органических растворителях, таких как бензол, толуол и четыреххлористый углерод. Его растворимость является важным фактором в его применении.
| Появление | Бесцветная или бледно-желтая жидкость |
| Удельный вес | 1638 г/мл |
| Цвет | Бесцветный |
| Запах | Острый, удушающий |
| Молярная масса | 118,97 г/моль |
| Плотность | 1638 г/мл |
| Точка плавления | -104,5°С |
| Точка кипения | 79,6°С |
| Мигающая точка | Непригодный |
| Растворимость в воде | Реагирует бурно |
| Растворимость | Растворим в органических растворителях, таких как бензол, толуол и четыреххлористый углерод. |
| Давление газа | 4,33 кПа при 20°C |
| Плотность пара | 3,9 (воздух = 1) |
| пКа | -6,3 |
| рН | Непригодный |
Безопасность и опасность тионилхлорида
Тионил дихлорид представляет собой несколько рисков для безопасности, и с ним следует обращаться осторожно. Он очень едкий и может вызвать серьезные ожоги при попадании на кожу, в глаза или на слизистые оболочки. Вдыхание его паров может вызвать раздражение и повреждение органов дыхания. Соединение бурно реагирует с водой, выделяя токсичные газы, такие как хлористый водород. Поэтому его следует хранить и обращаться с ним вдали от источников влажности. Тионилдихлорид также бурно реагирует со спиртами и водосодержащими соединениями, что может привести к опасности пожара или взрыва. Для обеспечения безопасного обращения с тионилдихлоридом необходимы адекватная вентиляция, средства индивидуальной защиты и надлежащие методы хранения.
| Символы опасности | Коррозионный (C), Токсичный (T), Опасный для окружающей среды (N) |
| Описание безопасности | – Хранить вдали от источников влаги и несовместимых веществ.<br>- Использовать в хорошо проветриваемом помещении и носить соответствующие средства индивидуальной защиты.<br>- Обращаться с осторожностью, избегать контакта с кожей, глазами и слизистыми оболочками.<br> – Хранить в плотно закрытой таре в сухом прохладном месте. |
| Идентификационные номера ООН | № ООН 1836 (Тионил дихлорид) |
| код ТН ВЭД | 2812.10.00 |
| Класс опасности | 8 (Коррозионные вещества) |
| Группа упаковки | II (Умеренно опасный) |
| Токсичность | Очень токсичен при вдыхании, проглатывании и попадании на кожу.<br>- Может вызвать серьезные ожоги и раздражение дыхательных путей.<br>- Может оказывать долгосрочное вредное воздействие на водные организмы. |
Методы синтеза тионилхлорида
Различные методы позволяют синтезировать тионилдихлорид.
Обычный подход включает реакцию между триоксидом серы (SO₃) и дихлоридом серы (SCl₂) в присутствии катализатора, такого как активированный уголь или хлорид алюминия . Реакция протекает при высоких температурах, обычно от 300 до 400 ° C, в результате чего образуется тионилдихлорид.
Другой метод включает прямую реакцию диоксида серы (SO₂) с пентахлоридом фосфора (PCl₅) или оксихлоридом фосфора (POCl₃). Эта реакция протекает при кипячении с постепенным добавлением реагентов и приводит к тионилдихлориду.
Реакция серы с трихлоридом фосфора (PCl₃) дает тионилдихлорид. Этот процесс включает нагревание реагентов и образование тионилдихлорида.
Другой метод включает реакцию между пентасульфидом фосфора (P2S₅) и пентахлоридом фосфора (PCl₅) в присутствии катализатора на основе кислоты Льюиса, такого как хлорид алюминия. Реакция протекает при высоких температурах и приводит к образованию тионилдихлорида.
Важно отметить, что эти методы синтеза требуют надлежащего обращения и мер безопасности из-за опасного характера используемых реагентов. Безопасный и эффективный синтез дихлорида тионила требует опыта опытных химиков и использования соответствующего лабораторного оборудования.
Использование тионилхлорида
Тионилдихлорид находит широкое применение в различных отраслях промышленности благодаря своим универсальным химическим свойствам. Вот некоторые распространенные варианты использования тионилдихлорида:
- Преобразование карбоновых кислот: Тионилдихлорид преобразует карбоновые кислоты в ацилхлориды, в основном используя реакцию Вильсмайера-Хаака в органическом синтезе.
- Хлорирование спирта: дихлорид тионила реагирует со спиртами, образуя алкилхлориды и находя применение в производстве хлорированных соединений для фармацевтических препаратов и агрохимикатов, известное как реакция Дарценса.
- Дегидратирующий агент: тионилдихлорид действует как дегидратирующий агент, облегчая удаление различных соединений из воды. Его обычно используют в синтезе красителей, парфюмерии и фармацевтических промежуточных продуктов.
- Производство литий-иониловых аккумуляторов. Производители используют тионилдихлорид для производства литий-тионилдихлоридных аккумуляторов, которые имеют высокую плотность энергии и длительный срок хранения. Эти батареи находят применение в медицинских приборах, военной технике и дистанционных датчиках.
- Реакции полимеризации: Тионилдихлорид участвует в реакциях полимеризации, способствуя синтезу различных полимеров, в том числе поликарбонатов и полиангидридов.
- Соединения фосфора: дихлорид тионила реагирует с соединениями фосфора, такими как трихлорид фосфора, с образованием фосфорилхлоридов. Химики используют эти промежуточные соединения для синтеза фосфорорганических соединений и антипиренов.
- Химический реагент: Тионилдихлорид служит универсальным реагентом во многих химических превращениях, включая реакции этерификации, галогенирования и нуклеофильного замещения.
Вопросы:
Вопрос: Чем можно промыть тионилхлорид?
Ответ: Тионилдихлорид можно промыть большим избытком спирта или совместимого основания, такого как метанол или раствор бикарбоната натрия.
Вопрос: Что представляет собой продукт валериановой кислоты с тионилхлоридом?
Ответ: Реакция валериановой кислоты с дихлоридом тионила приводит к образованию хлорида валерила, а также газообразного диоксида серы.
Вопрос: Можете ли вы добавить тионилхлорид к карбоновой кислоте?
Ответ: Да, тионилдихлорид можно добавить к карбоновой кислоте, чтобы превратить ее в ацилхлорид по реакции Вильсмайера-Хаака.
Вопрос: Что из следующего является правильной формулой Льюиса для тионилхлорида (SOCl2)?
A: Правильная формула Льюиса для тионилдихлорида (SOCl2) представлена как S=O | Кл – Кл.
Вопрос: Что управляет реакцией тионилхлорида?
Ответ: Реакция тионилдихлорида обусловлена высокой реакционной способностью тионилхлорида, который действует как электрофил в различных химических превращениях.
Вопрос: Как погасить тионилхлорид?
Ответ: Тионилдихлорид можно погасить, добавив подходящий гасящий агент, такой как первичный или вторичный спирт, или тщательно гидролизовав его водой.
Вопрос: Что получится, если смешать амины с тионилхлоридом?
A: Смешивание аминов с дихлоридом тионила приводит к образованию соответствующих солей гидрохлоридов аминов.
Вопрос: Что такое тионилхлорид?
Ответ: Тионилдихлорид представляет собой химическое соединение формулы SOCl2, обычно используемое в качестве реагента в органическом синтезе и в качестве дегидратирующего агента.
Вопрос: Что будет делать избыток тионилхлорида?
Ответ: Избыточное количество тионилдихлорида может вызвать бурные реакции, которые могут привести к образованию токсичных газов или опасности взрыва, поэтому с ним следует обращаться с осторожностью.
Вопрос: Как нейтрализовать тионилхлорид?
Ответ: Тионилдихлорид можно нейтрализовать, осторожно добавив его к большому избытку подходящего основания, такого как бикарбонат натрия или гидроксид натрия, соблюдая при этом соответствующие меры предосторожности.
