Карбонат лития (Li2CO3) является важным соединением, используемым в лекарствах, стабилизирующих настроение. Он лечит биполярное расстройство и помогает эффективно справляться с депрессией, тем самым способствуя общему психическому благополучию.
| Название ИЮПАК | Карбонат лития |
| Молекулярная формула | Ли2СО3 |
| Количество CAS | 554-13-2 |
| Синонимы | Дилития карбонат; Угольная кислота, дилитиевая соль; Карбонат лития (1+); Угольная кислота, литиевая соль (1:1) |
| ИнЧИ | InChI=1S/CH2O3.2Li/c2-1(3)4;;/h(H2,2,3,4);;/q;2*+1/p-2 |
Свойства карбоната лития
Формула карбоната лития
Формула карбоната дилития Li2CO3. Это означает, что каждая молекула содержит два атома лития (Li), один атом углерода (C) и три атома кислорода (O). Этот химический состав играет решающую роль в его свойствах и применении.
карбонат лития Молярная масса
Молярная масса карбоната дилития составляет приблизительно 73,89 г/моль. Его рассчитывают путем сложения атомных масс составляющих его элементов с учетом их соответствующих пропорций в формуле. Это значение важно для различных химических расчетов и реакций с участием карбоната дилития.
Температура кипения карбоната лития
Карбонат дилития имеет высокую температуру кипения, обычно около 1310 градусов по Цельсию (2390 градусов по Фаренгейту). При этой температуре соединение превращается из жидкости в газ, что делает его пригодным для конкретных промышленных процессов и применений.
Карбонат лития Температура плавления
Карбонат дилития имеет относительно низкую температуру плавления, обычно около 720 градусов по Цельсию (1328 градусов по Фаренгейту). При этой температуре соединение переходит из твердого состояния в жидкое, что облегчает его использование при изготовлении керамики, стекла и других материалов.
Плотность карбоната лития г/мл
Плотность карбоната дилития составляет примерно 2,11 г/мл. Это значение представляет собой его массу на единицу объема и указывает, насколько плотно упакованы частицы вместе. Плотность карбоната дилития имеет решающее значение для понимания его физических свойств и поведения.
Молекулярный вес карбоната лития
Карбонат дилития имеет молекулярную массу примерно 73,89 г/моль. Эта величина соответствует массе одного моля соединения и имеет важное значение при различных химических расчетах, например при определении количества молей в заданном количестве вещества.
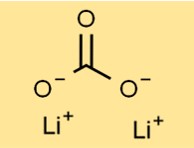
Структура карбоната лития
Карбонат дилития имеет кристаллическую структуру, образующую белый порошок без запаха. Его структура состоит из катионов Li+ и карбонат-анионов (CO3^2-), скрепленных ионными связями. Такое специфическое расположение способствует стабильности и реакционной способности соединения.
Растворимость карбоната лития
Карбонат дилития имеет ограниченную растворимость в воде. Он в некоторой степени растворяется, образуя слабощелочной раствор. Растворимость карбоната дилития является критически важным фактором в фармацевтических составах и других применениях, где требуется контролируемое растворение.
| Появление | Белый порошок без запаха |
| Удельный вес | 2,11 г/мл |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 73,89 г/моль |
| Плотность | 2,11 г/мл |
| Точка плавления | 720°С (1328°Ф) |
| Точка кипения | 1310°С (2390°Ф) |
| Мигающая точка | Непригодный |
| Растворимость в воде | Ограниченная растворимость |
| Растворимость | Растворим в воде, образуя слабощелочной раствор. |
| Давление газа | Нет в наличии |
| Плотность пара | Нет в наличии |
| пКа | Нет в наличии |
| рН | Слегка щелочной |
Безопасность и опасность карбоната лития
Карбонат дилития представляет потенциальную угрозу безопасности, требующую осторожного обращения. Прямой контакт с кожей может вызвать раздражение, а проглатывание может привести к желудочно-кишечному дискомфорту. В случае чрезмерного воздействия это может вызвать вредное воздействие на нервную систему. При обращении с ним следует соблюдать надлежащие меры предосторожности, такие как ношение защитного оборудования, чтобы избежать потенциальных опасностей. Крайне важно хранить и транспортировать карбонат дилития вдали от несовместимых веществ и источников тепла или пламени. В экстренных ситуациях немедленно обратитесь за медицинской помощью. При работе с карбонатом дилития следует внимательно ознакомиться с паспортами безопасности и рекомендациями и следовать им.
| Символы опасности | Коррозионное, Раздражающее |
| Описание безопасности | Может вызвать раздражение. Избегайте приема внутрь. Используйте при достаточной вентиляции. Носите защитное снаряжение. |
| Идентификационные номера ООН | Непригодный |
| код ТН ВЭД | 2836.40.00 |
| Класс опасности | Не классифицируется как опасный |
| Группа упаковки | Неклассифицированный |
| Токсичность | Низкая токсичность |
Методы синтеза карбоната лития
Существуют различные методы синтеза карбоната дилития.
Обычный подход состоит в том, чтобы подвергать соединения лития, такие как гидроксид лития или оксид лития, воздействию диоксида углерода в контролируемых условиях. В результате реакции в качестве побочного продукта образуется карбонат лития и вода. Другой метод включает смешивание растворимых солей лития , таких как хлорид лития, с растворимым карбонатным соединением. В результате реакции образуется твердый осадок карбоната лития, который исследователи могут отделить и собрать.
Кроме того, можно получить карбонат дилития термическим разложением бикарбоната лития. При нагревании бикарбоната лития он разлагается на карбонат лития с выделением углекислого газа и воды. В некоторых промышленных условиях этот процесс используется для получения карбоната лития высокой чистоты.
Для достижения желаемых выходов и уровней чистоты, независимо от используемого метода, необходимо обеспечить соответствующий контроль параметров реакции, таких как температура, давление и стехиометрия. Синтез карбоната дилития играет жизненно важную роль в производстве этого соединения для различных применений, включая фармацевтику, керамику и батареи.
Использование карбоната лития
Карбонат дилития находит разнообразное применение благодаря своим уникальным свойствам. Вот его основные применения:
- Фармацевтические препараты: это важный компонент лекарств, стабилизирующих настроение, эффективно лечащих биполярное расстройство и депрессию и способствующих психическому благополучию.
- Батареи. В перезаряжаемых литий-ионных батареях карбонат дилития служит предшественником соединений лития и играет решающую роль в технологиях хранения энергии.
- Пиротехника. Экзотермическая реакция карбоната дилития с некоторыми химическими веществами делает его ценным при использовании в фейерверках и фейерверках.
- Химический синтез: Как источник ионов лития он необходим в различных химических реакциях и органическом синтезе.
- Источник щелочных металлов: он действует как источник лития в лабораториях и исследованиях, используемый для изучения свойств щелочных металлов.
- Применение в окружающей среде: Карбонат дилития помогает регулировать pH в процессах очистки воды, контролируя кислотность и щелочность.
- Керамика и стекло: Карбонат дилития улучшает стабильность керамических и стеклянных изделий, выступая в качестве флюса, тем самым снижая температуру плавления.
- Металлургия. В металлургии карбонат дилития очищает такие металлы, как алюминий и медь, эффективно удаляя примеси и улучшая их механические свойства.
- Кондиционирование воздуха: осушители в системах кондиционирования воздуха используют карбонат дилития для эффективного поглощения влаги, обеспечивая оптимальную производительность кондиционирования воздуха.
В целом, широкий спектр применения карбоната дилития подчеркивает его важность во всех отраслях промышленности, что делает его ценным соединением в современных технологиях, медицине и материаловедении.
Вопросы:
Вопрос: Какой из следующих элементов имеет наименьшее количество валентных электронов?
Ответ: У бериллия наименьшее количество валентных электронов — всего два.
Вопрос: Для чего используется карбонат лития?
Ответ: Карбонат дилития используется в препаратах, стабилизирующих настроение, для лечения биполярного расстройства и депрессии.
Вопрос: Растворим ли карбонат дилития?
Ответ: Да, карбонат дилития в ограниченной степени растворим в воде.
Вопрос: Как работает карбонат лития?
Ответ: Карбонат дилития стабилизирует настроение и балансирует нейротрансмиттеры в мозге.
Вопрос: Что лечит карбонат лития?
Ответ: Карбонат дилития используется для лечения биполярного расстройства и депрессии в психиатрической медицине.
Вопрос: LiNO3 ионный или ковалентный?
Ответ: LiNO3 является ионным.
Вопрос: Что из перечисленного не растворяется в воде? Li2CO3, NaOH, PbCl2, Ba(OH)2, (NH4)2S.
Ответ: PbCl2 и Ba(OH)2 нерастворимы в воде.
Вопрос: Растворим ли Li2CO3 в воде?
Ответ: Li2CO3 слабо растворим в воде.
Вопрос: Сколько ионов в Li2CO3?
Ответ: Li2CO3 содержит три иона: два иона Li+ и один ион CO3^2-.
Вопрос: Сколько формульных единиц содержится в 0,0067 г Li2CO3?
Ответ: В 0,0067 г Li2CO3 содержится примерно 1,24 x 10^20 формульных единиц.
Вопрос: Сколько ионов лития содержится в 30,0 мл 0,600 М раствора Li2CO3?
Ответ: В 30,0 мл 0,600 М раствора Li2CO3 содержится 0,036 моль ионов Li+.
Вопрос: Каков массовый процент углерода в карбонате лития Li2CO3?
A: Массовый процентный состав углерода в Li2CO3 составляет примерно 11,3%.
Вопрос: Какая из следующих пар водных растворов выпадет в осадок при смешивании NH4NO3 + Li2CO3?
Ответ: NH4NO3 + Li2CO3 не образует осадка, поскольку оба соединения растворимы в воде.
