Диоксид хлора или ClO2 — очень эффективный и быстродействующий отбеливатель, используемый при очистке воды и консервировании пищевых продуктов. Это желтовато-зеленый газ с резким запахом.
| Название ИЮПАК | Диоксид хлора |
| Молекулярная формула | ClO2 |
| Количество CAS | 10049-04-4 |
| Синонимы | Пероксид хлора, ClO2, оксид хлора (IV) |
| ИнЧИ | ИнХИ=1S/ClO2/c2-1-3 |
Формула диоксида хлора
Формула диоксида хлора – ClO2. Это высокореактивный газ, состоящий из одного атома хлора и двух атомов кислорода. Формула диоксида хлора отражает его молекулярную структуру, которая имеет решающее значение для понимания его физических и химических свойств, включая его реакционную способность, стабильность и растворимость.
ClO2 Молярная масса
ClO2 имеет молярную массу 67,45 г/моль. Это очень реактивный окислитель, известный своими сильными отбеливающими свойствами. ClO2 широко используется в качестве дезинфицирующего и дезинфицирующего средства в различных промышленных и бытовых целях, включая очистку воды, отбеливание бумаги и консервирование пищевых продуктов. Молярная масса вещества играет решающую роль в определении его физических и химических свойств, включая плотность, температуру кипения и растворимость.
Температура кипения ClO2
Температура кипения ClO2 составляет 11,3°C (52,3°F). ClO2 существует в виде желтовато-зеленого газа при стандартной температуре и давлении. Он имеет резкий запах и очень реактивен, что делает его отличным окислителем. Температура кипения вещества — важное физическое свойство, которое помогает определить его стабильность, летучесть и транспортабельность.
ClO2 Точка плавления
Температура плавления ClO2 составляет -51,5°C (-60,7°F). Будучи газом при стандартных температуре и давлении, он не имеет твердого состояния. ClO2 хорошо растворим в воде и обычно используется в качестве дезинфицирующего и дезинфицирующего средства при очистке воды и консервировании пищевых продуктов. Температура плавления вещества — важное свойство, которое может влиять на его физическое и химическое поведение, особенно в реакциях, связанных с изменением состояния.
ClO2 Плотность г/мл
Плотность ClO2 составляет 1,97 г/мл при стандартных температуре и давлении. Это высокореактивный газ, который обычно используется в качестве отбеливателя и дезинфицирующего средства в различных отраслях промышленности. Плотность вещества является важным физическим свойством, которое может влиять на его поведение в различных процессах, включая транспортировку, хранение и обращение.
ClO2 Молекулярный вес
Молекулярная масса ClO2 составляет 67,45 г/моль. Это окислитель, широко используемый при очистке воды, отбеливании бумаги и консервировании пищевых продуктов. Молекулярная масса вещества — важное свойство, влияющее на его физическое и химическое поведение, включая плотность, температуру кипения и растворимость.
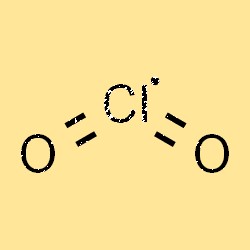
Структура ClO2
Структура ClO2 представлена молекулярной формулой ClO2. Это высокореактивный газ, состоящий из одного атома хлора и двух атомов кислорода. Молекула имеет изогнутую форму и полярна по своей природе, то есть имеет положительный и отрицательный конец. Структура ClO2 играет решающую роль в его химической активности, стабильности и растворимости в различных растворителях.
| Появление | Желтовато-зеленый газ |
| Удельный вес | 1,97 г/мл |
| Цвет | желтовато-зеленый |
| Запах | Акко |
| Молярная масса | 67,45 г/моль |
| Плотность | 1,97 г/мл |
| Точка плавления | -51,5°C (-60,7°F) |
| Точка кипения | 11,3°С (52,3°Ф) |
| Мигающая точка | Не применимо (газ) |
| Растворимость в воде | Очень растворим |
| Растворимость | Растворим в воде и органических растворителях. |
| Давление газа | Неопределенные |
| Плотность пара | Неопределенные |
| пКа | Неопределенные |
| рН | Неопределенные |
Примечание. Некоторые из перечисленных значений являются оценками, основанными на доступных данных. Всегда лучше обратиться к надежному источнику для получения конкретной и точной информации о свойствах вещества.
Безопасность и опасность диоксида хлора
ClO2 — высокореактивное и токсичное вещество, которое при неправильном обращении может представлять серьезную угрозу для здоровья и безопасности. Воздействие высоких концентраций газа ClO2 может вызвать раздражение глаз, носа и горла, а также проблемы с дыханием и затрудненное дыхание. Проглатывание ClO2 может вызвать серьезное расстройство пищеварения, включая тошноту, рвоту и диарею. Контакт кожи с ClO2 может вызвать раздражение и химические ожоги. Кроме того, ClO2 легко воспламеняется и может воспламениться при наличии тепла или искр. Чтобы свести к минимуму риски, связанные с ClO2, при работе с ним важно использовать соответствующие средства индивидуальной защиты, такие как перчатки, очки и респиратор. Также важно соблюдать правила безопасного хранения и обращения, чтобы избежать выброса ClO2 в окружающую среду.
| Символы опасности | Окислитель, Токсичный |
| Описание безопасности | S2- Хранить в недоступном для детей месте. S22- Не дышать пылью. S26- При попадании в глаза немедленно промыть их большим количеством воды и обратиться к врачу. |
| Идентификаторы сети | ООН 1479 |
| код ТН ВЭД | 2828.90.90 |
| Класс опасности | 5.1 |
| Группа упаковки | III |
| Токсичность | Диоксид хлора очень токсичен при вдыхании, проглатывании или контакте с кожей. Это может вызвать расстройство дыхания, расстройство пищеварения, раздражение глаз и химические ожоги. |
Методы синтеза диоксида хлора
ClO2 обычно синтезируют двумя основными методами: хлорат-хлоритным процессом и процессом электролиза.
Хлорат-хлоритный процесс включает реакцию хлората натрия с кислотой, например серной, с образованием ClO2. Этот процесс может осуществляться в промышленных масштабах и обычно используется для производства ClO2 для очистки воды и других применений.
Процесс электролиза предполагает использование электрического тока для генерации ClO2. Этот процесс обычно проводится в лаборатории и используется для производства небольших количеств ClO2 для исследований и экспериментов.
Независимо от используемого метода синтеза, важно соблюдать надлежащие протоколы безопасности и использовать соответствующее защитное оборудование при работе с ClO2. Это включает в себя ношение перчаток, средств защиты глаз и респиратора, чтобы избежать воздействия высокотоксичного газа.
Помимо этих способов, диоксид хлора можно также получить реакцией хлорита натрия с кислотой или реакцией хлората натрия с соляной кислотой. Выбор метода синтеза будет зависеть от конкретного применения и желаемых свойств конечного продукта.
Использование диоксида хлора
Диоксид хлора — универсальное химическое вещество, имеющее широкий спектр применения, включая очистку воды, консервацию пищевых продуктов и отбеливание. Некоторые из наиболее распространенных применений диоксида хлора включают:
Диоксид хлора для очистки воды обычно используется в качестве дезинфицирующего средства при очистке питьевой воды, сточных вод и промышленных технологических вод. Он очень эффективен против широкого спектра патогенов, включая бактерии, вирусы и паразиты, и часто используется в качестве альтернативы хлору или озону.
Диоксид хлора для консервации пищевых продуктов используется в качестве противомикробного средства при консервировании фруктов, овощей, мяса и других пищевых продуктов. Он эффективен против различных микроорганизмов, включая бактерии, дрожжи и плесень, и помогает продлить срок хранения пищевых продуктов.
Диоксид хлора используется для отбеливания древесной массы и других волокон для получения ярких и однородных цветов. Он также используется при отбеливании тканей, таких как хлопок и шерсть, для удаления загрязнений и улучшения белизны.
Другие области применения Диоксид хлора также используется при переработке промышленных и бытовых отходов, а также в производстве других химикатов, таких как хлораты, хлорамины и другие дезинфицирующие средства. Во всех своих применениях диоксид хлора очень эффективен и предлагает множество преимуществ по сравнению с другими химическими обработками. Однако важно проявлять осторожность при обращении и использовании диоксида хлора, поскольку это высокореактивное и токсичное вещество, которое может представлять серьезную угрозу для здоровья и безопасности, если с ним неправильно обращаться.
