Азид натрия (NaN3) – химическое соединение. Он очень токсичен и взрывоопасен. Он используется в подушках безопасности для быстрого выработки газообразного азота для надувания при ударе.
| Название ИЮПАК | Азид натрия |
| Молекулярная формула | NaN3 |
| Количество CAS | 26628-22-8 |
| Синонимы | Азиум, натриевая соль азотистоводородной кислоты, тринитрид натрия |
| ИнЧИ | InChI=1S/3HNO.Na/c1-4-2;2-1-3;/h3*1H;/q;;;+1/p-1 |
Свойства азида натрия
Формула азида натрия
Формула азида натрия: NaN3. Он состоит из одного атома натрия (Na) и трех атомов азота (N). Атом натрия заряжен положительно, а атомы азота – отрицательно. Формула представляет соотношение атомов натрия и азота в соединении.
азид натрия Молярная масса
Молярную массу натрияазида рассчитывают путем сложения атомных масс его составляющих. Натрий имеет молярную массу 22,99 г/моль, а азот имеет молярную массу 14,01 г/моль. Поскольку в азиде натрия три атома азота, умножим молярную массу азота на три. Сложение этих значений дает молярную массу натрияазида примерно 65,01 г/моль.
Температура кипения азида натрия
Натрийазид имеет высокую температуру кипения. При нагревании он подвергается разложению, а не кипению. При температуре выше 275 градусов по Цельсию (527 градусов по Фаренгейту) он быстро разлагается на металлический натрий и газообразный азот. Поэтому его точка кипения точно не определена.
Азид натрия Температура плавления
Температура плавления натрияазида относительно низкая по сравнению с его температурой кипения. Он плавится при температуре около 275 градусов по Цельсию (527 градусов по Фаренгейту). При этой температуре соединение переходит из твердого состояния в жидкое. Однако важно обращаться с натрийазидом с осторожностью из-за его токсичности и взрывоопасности.
Плотность азида натрия г/мл
Плотность натрияазида обычно выражается в граммах на миллилитр (г/мл). Приблизительная плотность твердого азида натрия составляет примерно 1,85 г/мл. Однако следует отметить, что плотность может незначительно меняться в зависимости от таких факторов, как температура и давление.
Азид натрия Молекулярный вес
Молекулярная масса натрияазида представляет собой сумму атомных масс составляющих его элементов. Как упоминалось ранее, азид натрия состоит из одного атома натрия и трех атомов азота. Сложение атомных масс этих элементов дает молекулярную массу примерно 65,01 грамма на моль (г/моль).
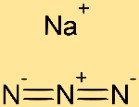
Структура азида натрия
Структура азида натрия состоит из чередующихся катионов натрия (Na+) и анионов азида (N3-). Ион натрия окружен тремя атомами азота, каждый из которых имеет общую электронную пару с атомом натрия. Такое расположение создает стабильную структуру кристаллической решетки азида натрия.
Растворимость азида натрия
Натрийазид умеренно растворим в воде. Растворяется в воде с образованием прозрачного раствора. Растворимость натрияазида увеличивается с повышением температуры. Однако важно обращаться с раствором осторожно из-за токсичной и взрывоопасной природы натрияазида.
| Появление | Белый твердый |
| Удельный вес | 1,85 г/мл |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Молярная масса | 65,01 г/моль |
| Плотность | 1,85 г/мл |
| Точка плавления | 275°С |
| Точка кипения | Разложившийся |
| Мигающая точка | Непригодный |
| Растворимость в воде | Умеренно растворим |
| Растворимость | Растворим в полярных растворителях, таких как аммиак. |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | Непригодный |
| рН | Нейтральный |
Безопасность и опасность азида натрия
Натрийазид представляет значительный риск для безопасности, и с ним следует обращаться с особой осторожностью. Он очень токсичен при проглатывании, вдыхании или проникновении через кожу. Воздействие натрияазида может вызвать серьезные риски для здоровья, включая проблемы с дыханием, головокружение и даже смерть. Это также потенциальная опасность взрыва, особенно при воздействии тепла, ударов или контакта с некоторыми металлами. При работе с азидом натрия люди должны носить соответствующие средства индивидуальной защиты, включая перчатки и защитные очки. Крайне важно хранить и обращаться с этим соединением в хорошо проветриваемых помещениях, вдали от источников возгорания и несовместимых веществ, чтобы свести к минимуму риск несчастных случаев и обеспечить безопасность на рабочем месте.
| Символы опасности | Токсичный, Взрывоопасный |
| Описание безопасности | Обращайтесь с особой осторожностью. Токсичное и взрывчатое вещество. |
| Идентификационные номера ООН | UN1687 (для азида натрия, токсичных твердых веществ, неорганических, н.у.) |
| код ТН ВЭД | 28500090 |
| Класс опасности | 6.1 (Токсичные вещества) |
| Группа упаковки | II (умеренно опасное вещество) |
| Токсичность | Очень токсичен |
Методы синтеза азида натрия
Существует несколько распространенных методов синтеза натрияазида.
Один метод включает реакцию между амидом натрия (NaNH2) и азотистоводородной кислотой (HN3). В этом методе растворите амид натрия в жидком аммиаке , а затем медленно добавьте азотистоводородную кислоту. Происходит реакция, в результате которой в качестве побочных продуктов образуются азид натрия и хлорид аммония.
Другой метод синтеза включает реакцию между нитритом натрия (NaNO2) и азидом натрия (NaN3). В водном растворе реакция тщательно контролируется добавлением нитрита натрия к раствору азида натрия, что приводит к образованию азида натрия и нитрата натрия.
Чтобы синтезировать азид натрия, цианид натрия (NaCN) можно ввести в реакцию с закисью азота (N2O) при высокой температуре. В ходе этой реакции в качестве побочных продуктов образуются азид натрия и цианат натрия.
Всегда соблюдайте соответствующие меры предосторожности, чтобы минимизировать риски, связанные с процессом синтеза. Это включает в себя использование средств индивидуальной защиты и соблюдение протоколов обращения.
Применение азида натрия
Натрийазид имеет несколько важных применений в различных отраслях промышленности. Вот некоторые известные приложения:
- Надувание подушек безопасности. Натрийазид является ключевым компонентом автомобильных подушек безопасности. Во время столкновения небольшое количество азида натрия быстро реагирует, выделяя газообразный азот, надувая подушку безопасности и защищая пассажиров.
- Биохимические исследования: исследователи используют натрийазид для ингибирования ферментов, таких как цитохромоксидаза, что облегчает изучение клеточных процессов и метаболических путей.
- Сохранение биологических образцов. Натрийазид сохраняет биологические образцы, такие как антитела, предотвращая рост бактерий и поддерживая их стабильность.
- Инициирование взрывчатых веществ: натрийазид из-за своей взрывной природы служит основным взрывчатым веществом в некоторых пиротехнических устройствах, детонаторах и инициаторах взрывчатых веществ.
- Химический синтез: Натрийазид действует как предшественник в различных химических реакциях, позволяя синтезировать органические соединения, фармацевтические препараты и красители.
- Предотвращение коррозии. Промышленность использует азид натрия в качестве ингибитора коррозии для защиты металлических поверхностей от деградации, вызванной окислением или воздействием коррозионных агентов.
- Горнодобывающая промышленность: Натрийазид помогает отделить ценные минералы от нежелательных веществ при добыче полезных ископаемых в качестве депрессанта в процессах флотации полезных ископаемых.
- Полимерная промышленность: Натрийазид действует как вспениватель при производстве пенополиуретанов, способствуя образованию пузырьков газа, которые придают пене желаемую структуру.
- Аналитическая химия: Натрийазид служит реагентом для различных химических анализов, включая спектрофотометрию, газовую хроматографию и масс-спектрометрию.
- Ветеринария: Ветеринары в некоторых случаях в ветеринарной практике используют натрийазид в качестве средства для эвтаназии животных.
Эти применения подчеркивают разнообразные возможности азида натрия, но крайне важно обращаться с этим соединением осторожно и соблюдать протоколы безопасности из-за его токсичного и взрывоопасного характера.
Вопросы
Вопрос: Как проверить наличие азида натрия?
Ответ: Натрийазид можно протестировать с использованием соответствующих аналитических методов, таких как спектроскопия, хроматография или испытание на химическую реактивность.
Вопрос: Азид натрия все еще используется в подушках безопасности?
Ответ: Да, натрийазид до сих пор используется в подушках безопасности в качестве топлива, обеспечивающего быстрое надувание при ударе.
Вопрос: Сколько граммов азида натрия необходимо для получения 30,5 г азота?
Ответ: Для производства 30,5 граммов газообразного азота требуется примерно 34 грамма азида натрия.
Вопрос: Где купить азид натрия?
Ответ: Натрийазид можно приобрести у поставщиков химикатов, поставщиков лабораторий или на химических интернет-площадках.
Вопрос: Как приготовить раствор 0,01% азида натрия в PBS?
Ответ: Чтобы приготовить 0,01% раствор натрияазида в PBS, растворите 0,01 грамма натрияазида в 100 мл физиологического раствора с фосфатным буфером (PBS).
Вопрос: Какова роль азида натрия в экспериментах?
Ответ: Натрийазид обычно используется в качестве ингибитора или консерванта в экспериментах, направленных на ингибирование активности ферментов или предотвращение роста бактерий.
Вопрос: Как удалить азид натрия из образца?
Ответ: Натрийазид можно удалить из образца тщательной промывкой или ополаскиванием соответствующими растворителями или подвергая его разложению при высокой температуре.
Вопрос: Как азид натрия влияет на ETC?
Ответ: Натрийазид ингибирует цепь переноса электронов (ЭТС) в митохондриях, блокируя фермент цитохромоксидазу, тем самым прерывая поток электронов и выработку АТФ.
Вопрос: Сколько граммов натрия образуется при реакции 93 граммов азида натрия?
Ответ: При реакции 93 граммов азида натрия образуется 35,9 граммов натрия.
Вопрос: Является ли взрывное разложение азида натрия физическим изменением срабатывания подушки безопасности?
Ответ: Нет, взрывное разложение азида натрия при надувании автомобильной подушки безопасности — это химическое изменение.
Вопрос: Как приготовить азид натрия?
Ответ: Натрийазид обычно получают методами химического синтеза, включающими реакции между подходящими предшественниками, такими как амид натрия и азотистоводородная кислота.
Вопрос: Насколько азид натрия токсичен?
Ответ: Натрийазид очень токсичен, и даже небольшие количества, например несколько граммов, могут представлять значительный риск для здоровья при проглатывании, вдыхании или проникновении через кожу.
Вопрос: Для чего используется азид натрия?
Ответ: Натрийазид используется в различных целях, включая надувание подушек безопасности, биохимические исследования, химический синтез, а также в качестве консерванта или ингибитора в биологических образцах.
Вопрос: Реагирует ли азид натрия с кислотами?
Ответ: Да, азид натрия может реагировать с кислотами, такими как соляная кислота (HCl), образуя токсичные газы, такие как азид водорода (HN3). При обращении с натрийазидом и кислотами следует соблюдать соответствующие меры предосторожности.
