O tetrahidreto de carbono, também conhecido como metano, é um gás incolor, inodoro e inflamável com a fórmula química CH4. É o principal componente do gás natural e é utilizado como fonte de combustível e matéria-prima em muitos processos industriais.
| Nome IUPAC | Metano |
| Fórmula molecular | CH4 |
| Número CAS | 74-82-8 |
| Sinônimos | Gás do pântano, CH4 |
| InChI | InChI=1S/CH4/h1H4 |
Propriedades do tetrahidreto de carbono
Fórmula de tetrahidreto de carbono
A fórmula química do tetrahidreto de carbono é CH4, um gás incolor e inodoro que é o principal componente do gás natural.
Massa molar de tetrahidreto de carbono
A massa molar do metano é 16,04 g/mol. Esta é a massa de um mol de moléculas de metano e é usada para calcular o número de moléculas em uma determinada massa da substância.
Ponto de ebulição do tetrahidreto de carbono
O ponto de ebulição do metano é -162°C. Isto significa que a esta temperatura, a pressão de vapor do metano é igual à pressão atmosférica e o líquido começa a ferver.
Ponto de fusão de tetrahidreto de carbono
O ponto de fusão do metano é -182,5°C. Esta é a temperatura na qual a forma sólida do metano se transforma em líquido.
Densidade de tetrahidreto de carbono g/mL
A densidade do metano à temperatura e pressão padrão é 0,717 g/mL. Isso significa que o volume de um mililitro de metano tem massa de 0,717 gramas.
Peso Molecular do Tetrahidreto de Carbono
O peso molecular do metano é 16,04 g/mol, que é a soma dos pesos atômicos dos quatro átomos de hidrogênio e um átomo de carbono na molécula de metano.
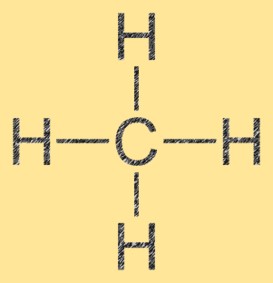
Estrutura do tetrahidreto de carbono
O metano tem uma estrutura molecular tetraédrica, com o átomo de carbono no centro e os quatro átomos de hidrogênio ligados a ele. Os ângulos de ligação no metano são 109,5° e os comprimentos de ligação são de aproximadamente 1,09 Å. A molécula é apolar, ou seja, não possui momento de dipolo elétrico permanente, devido à sua estrutura simétrica. O metano é um gás padrão de temperatura e pressão e é usado como fonte de combustível e matéria-prima em muitos processos industriais.
| Aparência | Gás incolor |
| Gravidade Específica | 0,554 (ar = 1) |
| Cor | Incolor |
| Cheiro | Inodoro |
| Massa molar | 16,04 g/mol |
| Densidade | 0,717 g/mL em temperatura e pressão padrão |
| Ponto de fusão | -182,5ºC |
| Ponto de ebulição | -162ºC |
| Ponto flash | N / D |
| Solubilidade em Água | 1,15g/L |
| Solubilidade | Solúvel em solventes orgânicos |
| Pressão de vapor | N / D |
| Densidade do vapor | 0,554 (ar = 1) |
| pKa | N / D |
| pH | N / D |
Segurança e perigos do tetrahidreto de carbono
O tetrahidreto de carbono (metano) é um gás inflamável que pode pegar fogo ou explodir se exposto a uma fonte de ignição. Em espaços confinados, o metano pode deslocar o oxigênio e causar asfixia. O metano é também um poderoso gás com efeito de estufa, contribuindo para as alterações climáticas. Ao manusear metano, é importante tomar as devidas precauções de segurança e seguir os regulamentos locais e os padrões da indústria.
| Símbolos de perigo | Flam. Gás |
| Descrição de segurança | 2/2/2 |
| Números de identificação da ONU | ONU1956 |
| Código SH | 2709.00.90 |
| Classe de perigo | 2.1 |
| Grupo de embalagem | N / D |
| Toxicidade | A inalação de altas concentrações de metano pode causar asfixia e deslocar o oxigênio em espaços confinados. |
Métodos para a síntese de tetrahidreto de carbono
O tetrahidreto de carbono (metano) pode ser sintetizado por vários métodos, incluindo métodos biológicos, químicos e termoquímicos. O método mais comum de síntese é através do processo biológico de metanogênese, que envolve microrganismos como arquéias metanogênicas e bactérias que produzem metano como subproduto de seu metabolismo. No processo químico, o metano pode ser produzido pela reação do dióxido de carbono com gás hidrogênio na presença de um catalisador. Além disso, o metano pode ser produzido a partir do carvão ou do gás natural através de processos termoquímicos, como gaseificação ou pirólise. Esses métodos envolvem o aquecimento da fonte de combustível a altas temperaturas na ausência de oxigênio, produzindo uma mistura de gases, incluindo metano, que pode ser separada e purificada antes do uso.
Usos do tetrahidreto de carbono
O tetrahidreto de carbono (metano) é uma fonte de energia versátil e amplamente utilizada, com aplicações em diversos setores, incluindo geração de energia, aquecimento, transporte e agricultura. É um componente importante do gás natural e é usado como combustível para aquecer casas e cozinhar alimentos. Na indústria de geração de energia, o metano é queimado para produzir vapor, que alimenta turbinas para produzir eletricidade. No setor de transportes, é utilizado como combustível para veículos e transporte marítimo. O metano também é utilizado como matéria-prima na produção de produtos químicos, como metanol e hidrogênio, e é utilizado na indústria de refrigeração como gás refrigerante. Além disso, o metano é utilizado na agricultura como combustível para bombas de irrigação e na pecuária para aquecer estábulos, bem como como fonte de energia para alimentação animal.
