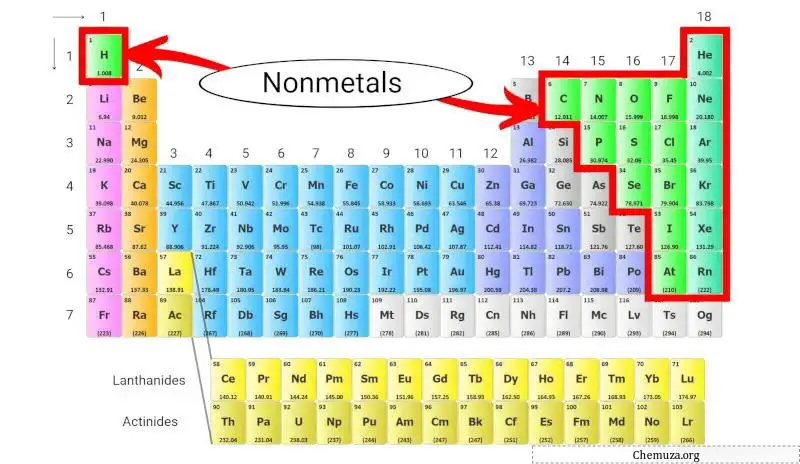
Os não-metais são um grupo de elementos que não possuem as propriedades dos metais, como alta condutividade elétrica e brilho. Esses não metais estão localizados no lado direito da tabela periódica , com exceção do hidrogênio .
Os não-metais podem ser encontrados em uma variedade de formas, incluindo gases como oxigênio e cloro , líquidos como bromo e sólidos como enxofre e carbono . [1]
Vamos ver coisas mais importantes sobre não metais.
O que exatamente são não metais?
Não metais são elementos que tendem a ganhar elétrons durante reações químicas, formando íons ou ânions com carga negativa.
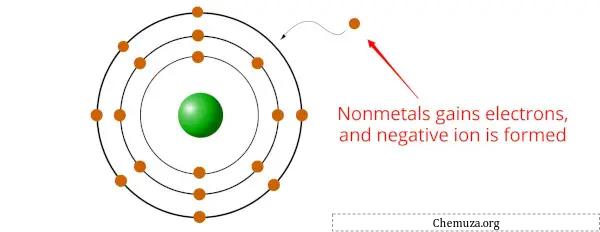
Isso ocorre porque os não-metais geralmente têm uma eletronegatividade mais alta que os metais, [2] o que significa que eles têm uma atração maior pelos elétrons.
Quando os não-metais se ligam aos metais , o elemento não-metálico ganha um ou mais elétrons do metal para formar um composto estável.
Por exemplo, o cloro ganha um elétron do sódio para formar o composto iônico cloreto de sódio (NaCl).
Pode-se dizer também que – Os não metais são um grupo de elementos químicos que não possuem as propriedades físicas e químicas dos metais.
Bem, vamos ver a lista dos não metais presentes na tabela periódica.
Lista de não metais presentes na tabela periódica
Aqui está uma lista de não metais presentes na tabela periódica:
- Hidrogênio (H)
- Hélio (Ele)
- Carbono (C)
- Nitrogênio (N)
- Oxigênio (O)
- Fluorita (F)
- Néon (Ne)
- Fósforo (P)
- Enxofre (S)
- Cloro (Cl)
- Argônio (Ar)
- Selênio (Se)
- Bromo (Br)
- Criptônio (Kr)
- Iodo (I)
- Xenônio (Xe)
- Astatino (At)
- Radônio (Rn)
Esses não-metais estão localizados no lado direito da tabela periódica, com exceção do hidrogênio, que está localizado no topo da tabela periódica, acima dos metais alcalinos .
Estado dos não metais (sólido, líquido ou gasoso?)
Os não-metais podem existir em todos os três estados da matéria: sólido, líquido e gasoso.
O estado de um não metal depende das condições de temperatura e pressão às quais está exposto.
Entre todos os não metais da tabela periódica;
- 11 não metais estão no estado gasoso à temperatura ambiente. [3]
- O bromo (Br) é um não metal encontrado no estado líquido à temperatura ambiente.
- O restante dos não metais são sólidos à temperatura ambiente.
Não-metal mais reativo
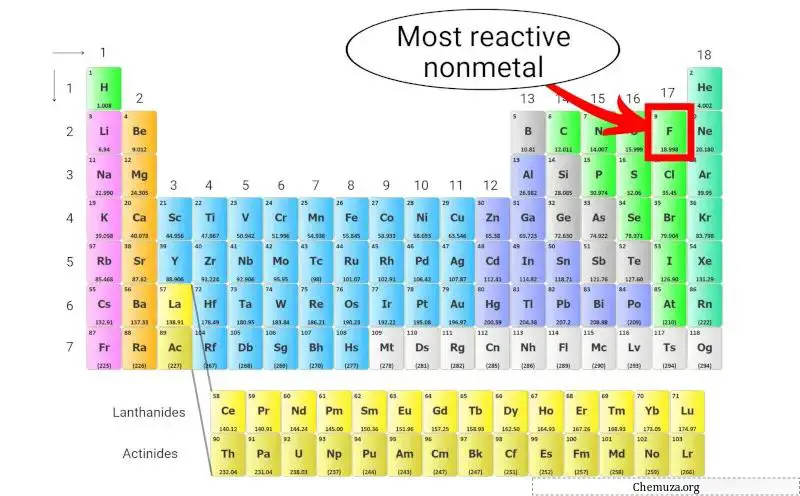
O flúor (F) é o não metal mais reativo presente na tabela periódica.
Mas por que? Por que o flúor é o mais reativo?
Isso ocorre porque ele possui a maior eletronegatividade de todos os elementos, o que significa que possui uma forte atração por elétrons.
O flúor tem sete elétrons em seu nível de energia mais externo e requer um elétron adicional para preencher sua camada de valência e atingir uma configuração estável.
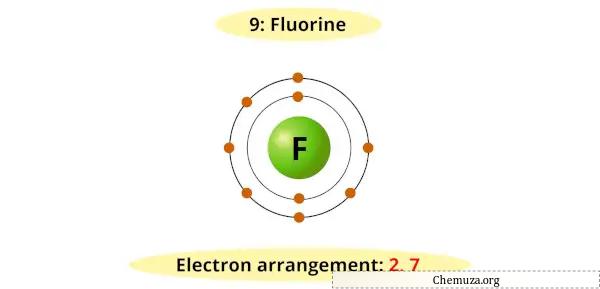
Portanto, ele aceita prontamente um elétron de outros elementos para formar um íon fluoreto (F-).
Devido à sua alta reatividade, o flúor pode reagir de forma explosiva com muitos outros elementos e compostos, incluindo água, metais e até mesmo vidro. [4]
O flúor é tão reativo que normalmente é armazenado e transportado em recipientes especializados feitos de materiais resistentes às suas propriedades corrosivas.
Papel dos não metais em aplicações ambientais e industriais
Os não metais são utilizados em vários processos industriais e aplicações ambientais devido às suas propriedades únicas. aqui estão alguns exemplos:
- Controle da poluição do ar: Não metais como nitrogênio e oxigênio desempenham um papel vital no controle da poluição do ar. Os óxidos de nitrogênio (NOx) são poluentes nocivos liberados por veículos e processos industriais. Catalisadores não metálicos são usados para converter NOx em gases inofensivos como nitrogênio e água. Da mesma forma, o oxigênio é utilizado em processos de combustão para reduzir emissões prejudiciais.
- Fertilizante: Nitrogênio, fósforo e enxofre são nutrientes essenciais para o crescimento das plantas. Fertilizantes não metálicos como nitrato de amônio e superfosfato são amplamente utilizados na agricultura para aumentar o rendimento das colheitas.
- Baterias: Elementos não metálicos como enxofre, carbono e lítio são usados em baterias. As baterias de íon-lítio são comumente usadas em dispositivos eletrônicos, veículos elétricos e sistemas de energia renovável.
- Purificação de água: Não metais como cloro e iodo são comumente usados como desinfetantes em sistemas de purificação de água. Eles matam bactérias e vírus nocivos e tornam a água segura para beber. [5]
- Fabricação de produtos químicos: Não metais como enxofre e cloro são amplamente utilizados na produção de produtos químicos como ácido sulfúrico, ácido clorídrico e solventes à base de cloro.
Resumo
Os não-metais não possuem as propriedades dos metais, como alta condutividade elétrica e brilho, e estão localizados no lado direito da tabela periódica, com exceção do hidrogênio. Eles existem em todos os três estados da matéria, dependendo das condições de temperatura e pressão.
O flúor é o não-metal mais reativo devido à sua alta eletronegatividade e aceita prontamente um elétron de outros elementos para formar um íon fluoreto (F-).
Os não-metais têm vários usos em aplicações ambientais e industriais, incluindo controle de poluição do ar, fertilizantes, baterias, purificação de água e fabricação de produtos químicos.
