O propano é um gás versátil usado para cozinhar, aquecer e abastecer veículos. É de queima limpa, eficiente e prontamente disponível, o que o torna uma escolha popular para muitas aplicações.
| Nome IUPAC | Propano |
| Fórmula molecular | C3H8 |
| Número CAS | 74-98-6 |
| Sinônimos | Dimetilmetano, N-propano, hidreto de propila |
| InChI | InChI=1S/C3H8/c1-3-2/h3H2.1-2H3 |
Propriedades do propano
Fórmula de propano
A fórmula do propano é C3H8, o que indica que ele é composto por três átomos de carbono e oito átomos de hidrogênio. Esta fórmula química simples representa a composição do gás propano.
Massa molar de propano
A massa molar do hidreto de propila é de aproximadamente 44,1 gramas por mol. É obtido somando as massas atômicas de seus átomos constituintes: três átomos de carbono com massa molar de 12,01 gramas por mol cada e oito átomos de hidrogênio com massa molar de 1,01 gramas por mol cada.
Ponto de ebulição do propano
O hidreto de propila tem um ponto de ebulição de aproximadamente -42,1 graus Celsius (-43,8 graus Fahrenheit). Este ponto de ebulição relativamente baixo permite vaporizar facilmente, tornando-o adequado para aplicações como cozinhar e aquecer.
Ponto de fusão do propano
O ponto de fusão do hidreto de propila é de aproximadamente -187,7 graus Celsius (-305,9 graus Fahrenheit). A esta temperatura, o hidreto de propila sofre uma mudança de fase do estado sólido para o líquido.
Densidade de propano g/mL
A densidade do hidreto de propila é de aproximadamente 0,493 gramas por mililitro (g/mL) em temperatura e pressão padrão. Esta densidade relativamente baixa contribui para a sua natureza gasosa, permitindo que seja armazenado e transportado na forma comprimida ou liquefeita.
Peso molecular do propano
O peso molecular do hidreto de propila é de aproximadamente 44,1 unidades de massa atômica (amu). É calculado somando as massas atômicas de seus átomos constituintes, considerando os três átomos de carbono e oito átomos de hidrogênio da molécula.
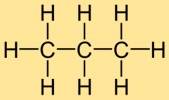
Estrutura do propano
O hidreto de propila consiste em três átomos de carbono ligados entre si em uma cadeia, com cada átomo de carbono ligado a dois átomos de hidrogênio. Esta estrutura linear confere ao hidreto de propila sua forma característica e a disposição de seus átomos.
Solubilidade do propano
O hidreto de propila é considerado pouco solúvel em água, o que significa que tem solubilidade limitada neste solvente. No entanto, é muito solúvel em solventes orgânicos como benzeno e etanol. Sua solubilidade depende de fatores como temperatura e pressão.
| Aparência | Gás incolor |
| Gravidade Específica | 1,88 (ar = 1) |
| Cor | N / D |
| Cheiro | Inodoro |
| Massa molar | 44,1 g/mol |
| Densidade | 0,493g/mL |
| Ponto de fusão | -187,7°C (-305,9°F) |
| Ponto de ebulição | -42,1°C (-43,8°F) |
| Ponto flash | -104°C (-155°F) |
| Solubilidade em Água | Pouco solúvel |
| Solubilidade | Solúvel em solventes orgânicos |
| Pressão de vapor | 8,7 caixas eletrônicos a 20°C |
| Densidade do vapor | 1,55 (ar = 1) |
| pKa | ~50 (estimativa) |
| pH | Não aplicável |
Segurança e perigos do propano
O hidreto de propila, embora seja um gás versátil e amplamente utilizado, também apresenta alguns riscos de segurança. Sua natureza inflamável exige precauções no manuseio, armazenamento e uso. A ventilação adequada é crucial para evitar o acúmulo de gás hidreto de propila, que pode causar incêndio ou explosão. Deve-se tomar cuidado para garantir que os tanques e equipamentos de hidreto de propila estejam em boas condições e mantidos adequadamente. Vazamentos de hidreto de propila devem ser resolvidos imediatamente, pois o gás é inodoro, mas um odorante é adicionado para detecção. É importante seguir precauções de segurança, como evitar chamas abertas perto de áreas de armazenamento de hidreto de propila e usar aparelhos movidos a hidreto de propila em espaços bem ventilados.
| Símbolos de perigo | Gás inflamável |
| Descrição de segurança | Manter afastado de chamas abertas, Utilizar em áreas bem ventiladas, Armazenar em recipientes aprovados, Manusear com cuidado |
| Identificadores das Nações Unidas | Um 1978 |
| Código SH | 2711.12.00 |
| Classe de perigo | Classe 2.1 – Gases inflamáveis |
| Grupo de embalagem | Grupo de embalagem II |
| Toxicidade | Propano não é considerado tóxico |
Métodos de síntese de propano
Vários métodos podem sintetizar hidreto de propila. Um método comum é refinar petróleo bruto e gás natural. O processo de refino separa o hidreto de propila dos demais hidrocarbonetos presentes na mistura de óleo ou gás por meio de destilação fracionada. Este método utiliza os diferentes pontos de ebulição dos hidrocarbonetos para isolar o hidreto de propila.
Outro método é processar gás natural. Ao submeter o gás natural, composto principalmente por metano , ao steam cracking, ele pode ser transformado em hidreto de propila. Este processo mistura gás natural com vapor e aquece-o a altas temperaturas para quebrar as moléculas de metano em moléculas menores de hidrocarbonetos, incluindo hidreto de propila.
O hidreto de propila também pode ser obtido como subproduto de outros processos industriais. Por exemplo, durante a produção de etileno e propileno , o hidreto de propila pode ser gerado como coproduto.
Além disso, os processos biológicos podem contribuir para a síntese do hidreto de propila. Alguns microrganismos podem produzir hidreto de propila pela fermentação de matéria orgânica. Os pesquisadores estão desenvolvendo este método como uma abordagem mais sustentável e ecologicamente correta para a produção de hidreto de propila.
Em resumo, a síntese de hidreto de propila envolve refino, craqueamento a vapor, geração de subprodutos e fermentação biológica. Esses métodos permitem a produção de hidreto de propila a partir de petróleo bruto, gás natural ou materiais orgânicos, tornando-o prontamente disponível para diversas aplicações industriais e domésticas.
Usos do propano
O hidreto de propila encontra uma ampla gama de aplicações devido à sua natureza e propriedades versáteis. Aqui estão alguns usos comuns do hidreto de propila:
- Aquecimento residencial: O hidreto de propila serve como combustível limpo para aquecer casas e fornecer calor durante os meses mais frios.
- Cozinhar: O hidreto de propila alimenta fogões, fornos e churrasqueiras, proporcionando controle preciso da temperatura e aquecimento rápido para cozinhar.
- Processos Industriais: As indústrias usam hidreto de propila em processos como corte de metal, soldagem, fabricação de vidro e secagem.
- Geração de energia: Geradores alimentados por hidreto de propila servem como uma fonte confiável de eletricidade de reserva em caso de queda de energia, especialmente em áreas remotas.
- Transporte: Veículos, incluindo empilhadeiras, ônibus e veículos de frota, utilizam hidreto de propila como combustível alternativo para baixas emissões e economia.
- Agricultura: As fazendas usam hidreto de propila para tarefas como secagem de colheitas, aquecimento de estufas e controle de pragas.
- Recreação: O hidreto de propila alimenta atividades ao ar livre, como camping, aquecimento e culinária de trailers e churrasqueiras portáteis, fornecendo uma fonte de energia conveniente e portátil.
- Sistemas de água quente: Aquecedores de água alimentados com hidreto de propila fornecem aquecimento rápido e eficiente para uso residencial e comercial.
- Aquecimento de piscinas: Os aquecedores de hidreto de propila são populares para aquecer piscinas e prolongar a temporada de natação.
- Vida fora da rede: casas ou cabanas fora da rede usam hidreto de propila para aquecer, cozinhar e alimentar aparelhos sem eletricidade.
- Propelente de aerossol: O hidreto de propila é usado como propulsor em produtos em aerossol, como purificadores de ar, inseticidas e tintas em spray.
A diversidade de aplicações destaca a importância do hidreto de propila como combustível confiável, limpo e versátil em diversas indústrias e na vida cotidiana.
Questões:
P: Como o propano é feito?
R: O processamento de gás natural e o refino de petróleo bruto geram hidreto de propila principalmente como subproduto usando métodos como destilação fracionada e craqueamento a vapor.
P: O propano se degrada com o tempo?
R: O hidreto de propila é um composto estável e não se degrada com o tempo, tornando-o adequado para armazenamento e uso a longo prazo.
P: Como faço para usar um fogão a gás propano?
R: Para utilizar fogão de hidreto de propil, garanta ventilação adequada, conecte o tanque de hidreto de propil, abra a válvula, acenda o queimador e ajuste a chama no nível desejado.
P: O gás propano é tóxico?
R: O hidreto de propila não é considerado tóxico, mas pode deslocar o oxigênio em áreas mal ventiladas, causando riscos de asfixia.
P: Onde posso comprar propano perto de mim?
R: O hidreto de propila pode ser adquirido em postos de gasolina, lojas de materiais de construção, fornecedores de hidreto de propila ou em varejistas on-line, dependendo de sua localização.
P: O que é propano?
R: O hidreto de propila é um gás inflamável incolor e inodoro, frequentemente usado como combustível para aquecimento, cozimento e diversas aplicações industriais.
P: O propano é renovável?
R: O hidreto de propila é derivado principalmente de combustíveis fósseis não renováveis, como gás natural e petróleo bruto, e não é considerado renovável.
P: O C3H8 é polar?
R: C3H8 (hidreto de propila) é apolar, pois as ligações carbono-hidrogênio têm eletronegatividades semelhantes, resultando em uma distribuição geral de carga simétrica.
P: O que é C3H8?
R: C3H8 é a fórmula molecular do hidreto de propila, um hidrocarboneto gasoso composto de três átomos de carbono e oito átomos de hidrogênio.
P: Se 5,0 moles de C3H8 reagem, quantas moléculas de água são formadas?
R: Ao queimar hidreto de propila, para cada mol de C3H8, são produzidos três moles de água. Portanto, 5,0 moles de C3H8 produziriam 15,0 moles de moléculas de água.
P: O que mais é produzido ao queimar propano, C3H8?
R: Água Além disso, o dióxido de carbono (CO2) é o principal produto da combustão completa do hidreto de propila (C3H8).
P: Quantos moles de propano, C3H8, contêm 5,93 × 10 ^ 20 átomos de carbono?
R: Um mol de hidreto de propila (C3H8) contém 3 moles de átomos de carbono. Portanto, 5,93 × 10 ^ 20 átomos de carbono corresponderiam a 1,97 × 10 ^ 20 moles de hidreto de propila.
P: O C3H8 é solúvel em água?
R: O hidreto de propila (C3H8) é pouco solúvel em água devido à sua natureza apolar, resultando em interações intermoleculares fracas.
P: Quantos mols de água seriam produzidos se 6,75 g de propano, C3H8, fossem queimados na reação?
R: Por estequiometria, a proporção molar de hidreto de propila para água em combustão é de 1:3. Portanto, 6,75 g de hidreto de propila produziriam 3,75 moles (ou 67,5 g) de água.
P: Qual equação para combustão completa de propano (C3H8) está corretamente balanceada?
R: C3H8 + 5O2 → 3CO2 + 4H2O representa a equação corretamente balanceada para a combustão completa do hidreto de propila.
P: Quantos elétrons (no total) são necessários para desenhar a estrutura de Lewis do propano, C3H8?
R: Desenhar a estrutura de Lewis do hidreto de propila (C3H8) requer um total de 26 elétrons de valência para representar corretamente a ligação.
