A piperidina é uma amina cíclica que consiste em um anel de seis membros com um átomo de nitrogênio. É utilizado em produtos farmacêuticos, pesticidas e como solvente para reações orgânicas.
| Nome IUPAC | Piperidina |
| Fórmula molecular | C₅H₁₁N |
| Número CAS | 110-89-4 |
| Sinônimos | Hexahidropiridina, Azaciclohexano, Ciclopentimina |
| InChI | InChI=1S/C5H11N/c1-2-4-6-5-3-1/h6H,1-5H2 |
Propriedades da piperidina
Fórmula de piperidina
A fórmula química da hexahidropiridina é C₅H₁₁N. Consiste em cinco átomos de carbono, onze átomos de hidrogênio e um átomo de nitrogênio. A fórmula representa a composição exata dos elementos em uma molécula de hexahidropiridina.
Massa molar de piperidina
A massa molar da hexahidropiridina é calculada somando as massas atômicas de seus elementos constituintes. Para hexahidropiridina (C₅H₁₁N), a massa molar é de aproximadamente 85,15 gramas por mol. Este valor é útil para determinar a quantidade de hexahidropiridina numa determinada amostra.
Ponto de ebulição da piperidina
A hexahidropiridina tem um ponto de ebulição de cerca de 106 graus Celsius. Esta temperatura representa o ponto em que a forma líquida da hexahidropiridina se transforma em gás. O ponto de ebulição é importante em vários processos industriais que envolvem o uso de hexahidropiridina.
Ponto de fusão da piperidina
O ponto de fusão da hexahidropiridina é de aproximadamente -7 graus Celsius. Indica a temperatura na qual a hexahidropiridina sólida muda para o estado líquido. O ponto de fusão é uma característica crucial para o manuseio e armazenamento da hexahidropiridina em diferentes aplicações.
Densidade de Piperidina g/mL
A densidade da hexahidropiridina é de aproximadamente 0,86 gramas por mililitro (g/mL). Densidade refere-se à massa de uma substância por unidade de volume. Esta propriedade é valiosa na determinação da quantidade de hexahidropiridina necessária para aplicações específicas.
Peso molecular da piperidina
O peso molecular da hexahidropiridina é de aproximadamente 85,15 gramas por mol. Representa a soma dos pesos atômicos de todos os átomos presentes em uma molécula de hexahidropiridina. O peso molecular é um parâmetro essencial utilizado em vários cálculos químicos e reações envolvendo hexahidropiridina.
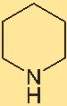
Estrutura da piperidina
A hexahidropiridina tem uma estrutura de anel que consiste em um anel de seis membros contendo um átomo de nitrogênio e cinco átomos de carbono. O arranjo dos átomos nesta estrutura afeta as propriedades químicas e o comportamento da hexahidropiridina. Compreender a estrutura nos permite estudar sua reatividade e interações.
Solubilidade da piperidina
A hexahidropiridina é solúvel em água e solventes orgânicos. Forma ligações de hidrogênio com moléculas de água devido à presença de um átomo de nitrogênio. A solubilidade da hexahidropiridina permite que ela seja utilizada como solvente em diversos processos químicos e como reagente em síntese orgânica.
| Aparência | Líquido transparente |
| Gravidade Específica | 0,862g/ml |
| Cor | Incolor |
| Cheiro | Forte, amoniacal |
| Massa molar | 85,15 g/mol |
| Densidade | 0,862g/ml |
| Ponto de fusão | -7ºC |
| Ponto de ebulição | 106°C |
| Ponto flash | 9ºC |
| Solubilidade em Água | Miscível |
| Solubilidade | Solúvel em solventes polares, como água e solventes orgânicos |
| Pressão de vapor | 7,4 mmHg a 25°C |
| Densidade do vapor | 2,95 (ar=1) |
| pKa | 11.24 |
| pH | Básico |
Segurança e perigos da piperidina
A hexahidropiridina apresenta vários riscos de segurança e deve ser manuseada com cautela. É irritante para a pele, olhos e sistema respiratório. O contato direto pode causar queimaduras ou irritação. A inalação de vapores de hexahidropiridina pode causar dificuldade respiratória e danos nos pulmões. É inflamável e pode formar misturas explosivas com o ar. Quando aquecido, pode liberar vapores tóxicos, incluindo óxidos de nitrogênio. Ventilação adequada e equipamentos de proteção individual, como luvas e óculos de proteção, são necessários ao trabalhar com hexahidropiridina. Além disso, deve ser armazenado em local fresco e bem ventilado, longe de fontes de ignição. O treinamento adequado e o conhecimento dos protocolos de segurança são essenciais ao manusear a hexahidropiridina para minimizar riscos potenciais.
| Símbolos de perigo | Caveira e ossos cruzados, chama, corrosiva |
| Descrição de segurança | Evitar o contato com a pele e os olhos. Usar em uma área bem ventilada. Manter afastado de fontes de ignição. |
| Números de identificação da ONU | Nº ONU 2879 (para Piperidina) |
| Código SH | 2933.99.80 |
| Classe de perigo | Classe 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | Grupo de embalagem II |
| Toxicidade | A piperidina é tóxica e pode causar sérios efeitos à saúde. A inalação, ingestão ou absorção pela pele devem ser evitadas. A exposição prolongada ou repetida pode causar danos aos órgãos ou problemas respiratórios. Devem ser tomadas medidas de proteção adequadas durante o manuseio e armazenamento. |
Métodos de síntese de piperidina
Existem diferentes métodos para sintetizar hexahidropiridina.
Um método comumente usado envolve a reação de 1,5-dihalopentano com amônia . Neste processo, o grupo amino (-NH2) substitui os átomos de halogênio sofrendo substituição nucleofílica. Outro método envolve a redução da piridina com gás hidrogênio sobre um catalisador, como paládio ou platina. Esta reação de redução converte piridina em hexahidropiridina adicionando dois átomos de hidrogênio ao átomo de nitrogênio.
Além disso, a hidrogenação de sais de piridínio ou derivados de piridina produz hexahidropiridina. Este processo de hidrogenação ocorre sob alta pressão e temperatura utilizando um catalisador adequado. Outra abordagem envolve a reação de 2,5-dimetilpirrol com acetileno seguida de hidrogenação, que produz hexahidropiridina.
Além disso, a aminação redutiva da ciclopentanona ou dos seus derivados com amônia ou aminas primárias também pode levar à formação de hexahidropiridina. Esta reação envolve a adição de um grupo amino ao grupo cetona, seguida de redução para formar o anel hexahidropiridina.
No geral, esses métodos sintéticos permitem a obtenção da hexahidropiridina a partir de diversas matérias-primas, possibilitando sua produção em diversos ambientes industriais e de pesquisa. A escolha do método depende de fatores como disponibilidade de matéria-prima, rendimento desejado e requisitos específicos de aplicação.
Usos da Piperidina
A hexahidropiridina possui diversas aplicações em diversas indústrias devido às suas propriedades versáteis. Alguns usos comuns de hexahidropiridina incluem:
- Indústria farmacêutica: A indústria farmacêutica utiliza a hexahidropiridina como bloco de construção para sintetizar muitos compostos farmacêuticos. Desempenha um papel crucial na produção de medicamentos como anti-histamínicos, antipsicóticos, analgésicos e agentes antivirais.
- Agroquímicos: A hexahidropiridina melhora a eficácia dos pesticidas e inseticidas porque os fabricantes a utilizam em sua produção. Melhora o controle de pragas e melhora o rendimento das colheitas.
- Síntese orgânica: A hexahidropiridina atua como catalisador ou solvente em reações orgânicas, facilitando os processos de condensação, ciclização e oxidação. Permite a síntese de diversos compostos químicos.
- Indústria da Borracha: Na indústria da borracha, a hexahidropiridina funciona como acelerador de vulcanização. Melhora a resistência mecânica, elasticidade e durabilidade dos produtos de borracha, melhorando a reticulação dos polímeros de borracha.
- Solvente: A hexahidropiridina serve como solvente para vários compostos orgânicos, tornando-a útil em processos de extração, reações químicas e como meio para formulações farmacêuticas. Dissolve uma ampla gama de substâncias.
- Inibidor de corrosão: A hexahidropiridina funciona como um inibidor de corrosão, protegendo as superfícies metálicas da degradação. Forma uma película protetora sobre o metal, retardando ou prevenindo reações de corrosão.
- Reagente de laboratório: Os pesquisadores usam a hexahidropiridina como reagente em experimentos de laboratório, principalmente em química orgânica. Participa ativamente de reações, como N-alquilações e reações de abertura de anel, facilitando a síntese dos compostos desejados.
- Intermediários Químicos: Os derivados de hexahidropiridina servem como intermediários na produção de vários produtos químicos, incluindo corantes, fragrâncias e surfactantes.
Essas aplicações demonstram os diversos e valiosos papéis que a hexahidropiridina desempenha em vários setores, contribuindo para o desenvolvimento de produtos farmacêuticos, agroquímicos, produtos de borracha e muito mais.
Questões:
P: Qual é o pKa da piperidina?
R: O pKa da hexahidropiridina é aproximadamente 11,24.
P: Qual é o pKa do malonato de dietila?
R: O pKa do malonato de dietila é aproximadamente 12,5.
P: Por que o ácido conjugado da morfolina é mais ácido do que o ácido conjugado da piperidina?
R: O ácido conjugado de morfolina é mais ácido devido à presença de um átomo de oxigênio que retira elétrons no anel de morfolina, que estabiliza a carga positiva do ácido conjugado.
P: Como remover o aduto de dibenzofulveno-piperidina?
R: O aduto de dibenzofulveno-piperidina pode ser removido por técnicas de purificação apropriadas, como extração com solvente, cromatografia ou recristalização, dependendo das condições específicas e da pureza desejada.
P: Qual é o papel da piperidina na reação que você realizou?
R: A hexahidropiridina pode atuar como catalisador, base ou reagente, dependendo das condições e requisitos específicos da reação.
P: A piperidina é miscível com THF?
R: Sim, a hexahidropiridina é miscível com THF (tetrahidrofurano).
P: O que acontece quando a piperidina e o DMF são combinados?
R: Quando a hexahidropiridina e a DMF (dimetilformamida) são combinadas, elas podem potencialmente sofrer várias reações dependendo das condições de reação e da presença de outros reagentes ou catalisadores.
P: Qual é o pH de uma solução que é 0,120 M em piperidina e 0,079 M em seu sal cloreto?
R: O pH da solução dependeria do pKa da hexahidropiridina e da dissociação do seu sal cloreto e exigiria cálculos adicionais para determinar o valor exato do pH.
P: Como quebrar o anel de piperidina?
R: A quebra do anel hexahidropiridina pode ser alcançada por vários métodos, como oxidação, redução ou reações de abertura do anel, usando reagentes e condições de reação apropriados.
P: Basicidade da piridina ou piperidina?
R: A hexahidropiridina é geralmente mais básica que a piridina devido à presença de um átomo de nitrogênio mais nucleofílico em seu anel, tornando-a mais facilmente capaz de doar um próton.
