O pentassulfeto de fósforo (P2S5) é um composto composto por dois átomos de fósforo e cinco átomos de enxofre. É utilizado em diversas aplicações, incluindo a produção de inseticidas e lubrificantes.
| Nome IUPAC | Pentassulfeto de fósforo |
| Fórmula molecular | P2S5 |
| Número CAS | 1314-80-3 |
| Sinônimos | Sulfeto de fósforo (V); Pentassulfureto de difósforo; Sulfureto fosfórico; Fósforo pentassulfurizado |
| InChI | InChI=1S/2P.5S |
Propriedades do pentassulfeto de fósforo
Fórmula de pentassulfeto de fósforo
A fórmula do pentassulfeto de fósforo é P2S5. É composto por dois átomos de fósforo ligados a cinco átomos de enxofre.
Massa molar de Pentassulfeto de Fósforo
A massa molar do pentassulfeto de difósforo pode ser calculada somando as massas atômicas dos elementos constituintes. A massa atômica do fósforo (P) é de aproximadamente 30,97 g/mol e a do enxofre (S) é de aproximadamente 32,07 g/mol. A massa molar do P2S5 é, portanto, aproximadamente 222,27 g/mol.
Ponto de ebulição do pentassulfeto de fósforo
O pentassulfeto de difósforo tem um ponto de ebulição de aproximadamente 514 graus Celsius (957 graus Fahrenheit). A esta temperatura, o composto sofre uma transição de fase de líquido para gás.
Ponto de fusão do pentassulfeto de fósforo
O ponto de fusão do pentassulfeto de difósforo é de aproximadamente 280 graus Celsius (536 graus Fahrenheit). Esta é a temperatura na qual o composto muda do estado sólido para o estado líquido.
Densidade de pentassulfeto de fósforo g/mL
A densidade do pentassulfeto de difósforo é de aproximadamente 2,02 g/mL. Isso indica que o composto é relativamente denso, com alta massa por unidade de volume.
Peso Molecular do Pentassulfeto de Fósforo
O peso molecular do pentassulfeto de difósforo, que é a soma dos pesos atômicos de seus elementos constituintes, é de aproximadamente 222,27 g/mol.
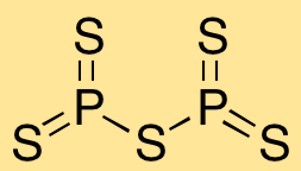
Estrutura do pentassulfeto de fósforo
O pentassulfeto de difósforo tem uma estrutura molecular na qual dois átomos de fósforo estão ligados a cinco átomos de enxofre. O arranjo dos átomos forma uma forma trigonal bipiramidal, com os átomos de fósforo no centro e os átomos de enxofre ao seu redor.
Solubilidade do pentassulfeto de fósforo
O pentassulfeto de difósforo é pouco solúvel em água, o que significa que se dissolve apenas até certo ponto. No entanto, é mais solúvel em solventes orgânicos como benzeno e dissulfeto de carbono.
| Aparência | Sólido amarelo |
| Gravidade Específica | 2.02 |
| Cor | AMARELO |
| Cheiro | Cheiro forte |
| Massa molar | 222,27 g/mol |
| Densidade | 2,02g/ml |
| Ponto de fusão | 280°C (536°F) |
| Ponto de ebulição | 514°C (957°F) |
| Ponto flash | Não disponível |
| Solubilidade em Água | Pouco solúvel |
| Solubilidade | Solúvel em solventes orgânicos como benzeno e dissulfeto de carbono |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Não disponível |
Segurança e perigos do pentassulfeto de fósforo
O pentassulfeto de difósforo apresenta vários riscos de segurança e deve-se tomar cuidado ao manuseá-lo. Pode causar irritação grave e queimaduras na pele, olhos e sistema respiratório por contato ou inalação. O contato direto com o composto deve ser evitado e devem ser utilizadas luvas de proteção, óculos de proteção e equipamento respiratório. Também é inflamável e pode inflamar-se quando exposto ao calor ou chama, produzindo óxidos de enxofre tóxicos. É necessário armazenamento adequado longe de fontes de ignição. Além disso, o pentassulfeto de difósforo não deve ser misturado com água ou substâncias reativas, pois pode gerar gases inflamáveis ou tóxicos. A ventilação adequada e o cumprimento dos protocolos de segurança são cruciais ao trabalhar com este composto.
| Símbolos de perigo | Inflamável, Irritante |
| Descrição de segurança | Causa queimaduras na pele e lesões oculares graves. Nocivo se inalado. Sólido inflamável. |
| Números de identificação da ONU | ONU 1340 |
| Código SH | 2812120000 |
| Classe de perigo | 4,2 (sólido inflamável), 8 (corrosivo) |
| Grupo de embalagem | II |
| Toxicidade | Tóxico |
Métodos para a síntese de pentassulfeto de fósforo
Diferentes métodos podem ser usados para sintetizar pentassulfeto de difósforo.
Um método comum para sintetizar pentassulfeto de difósforo envolve o aquecimento de fósforo elementar e enxofre juntos em um ambiente controlado, geralmente em um recipiente selado. A alta temperatura facilita a reação, levando à formação do pentassulfeto de difósforo.
Outro método envolve misturar trissulfeto de fósforo (P4S3) com excesso de enxofre e aquecer a mistura para promover a reação. O excesso de enxofre combina-se com o trissulfeto de fósforo, resultando na produção de pentassulfeto de difósforo.
A reação do pentacloreto de fósforo (PCl5) com o sulfeto de hidrogênio (H2S) na presença de um solvente adequado, como o dissulfeto de carbono, permite a preparação do pentassulfeto de difósforo. A reação gera pentassulfeto de difósforo e libera gás cloreto de hidrogênio (HCl) como subproduto.
Tenha cuidado ao usar estes métodos sintéticos devido à natureza perigosa dos reagentes e produtos envolvidos. Garanta medidas de segurança adequadas, como usar equipamentos de proteção adequados e trabalhar em áreas bem ventiladas, durante o processo de síntese.
Usos do Pentassulfeto de Fósforo
O pentassulfeto de difósforo encontra aplicações em diversas indústrias e processos devido às suas propriedades únicas. Aqui estão alguns de seus usos:
- Produção de inseticidas: Os fabricantes usam pentassulfeto de difósforo como ingrediente chave na fabricação de inseticidas, especialmente aqueles destinados ao controle de pragas como mosquitos e carrapatos.
- Aditivo lubrificante: As empresas adicionam pentassulfeto de difósforo aos lubrificantes como um aditivo para melhorar suas propriedades de extrema pressão e antidesgaste. Este aditivo melhora o desempenho da lubrificação e protege as máquinas sob condições de alto estresse.
- Síntese química: O pentassulfeto de difósforo atua como reagente em diversas reações químicas, como na síntese do cloreto de tionila (SOCl2), amplamente utilizado em síntese orgânica.
- Indústria farmacêutica: A indústria farmacêutica utiliza pentassulfeto de difósforo em processos de pesquisa e desenvolvimento para sintetizar compostos e intermediários específicos.
- Extração de metais: Os processos metalúrgicos utilizam pentassulfeto de difósforo para extrair certos metais, principalmente cobre e zinco, de seus minérios. Ajuda a remover impurezas e facilita a purificação de metais.
- Produção de corantes e pigmentos: O pentassulfeto de difósforo desempenha um papel na síntese de vários corantes e pigmentos, servindo como um alicerce chave para sua estrutura química.
- Agentes de guerra química: Historicamente, o pentassulfeto de difósforo tem sido usado na produção de agentes de guerra química. No entanto, os tratados internacionais regulam e controlam estritamente a sua utilização para estes fins.
É importante observar que, devido à natureza perigosa do pentassulfeto de difósforo, medidas e protocolos de segurança apropriados devem ser seguidos ao manuseá-lo, armazená-lo e descartá-lo.
Questões:
P: O que é dímero de pentassulfeto de fósforo?
R: O dímero de pentassulfeto de difósforo refere-se à estrutura molecular de duas moléculas de pentassulfeto de fósforo quimicamente ligadas entre si.
P: Qual é a entropia do pentassulfeto de fósforo?
R: A entropia do pentassulfeto de difósforo refere-se à medição de sua desordem molecular ou aleatoriedade em uma determinada temperatura.
P: Qual é a entalpia do pentassulfeto de fósforo?
R: A entalpia do pentassulfeto de difósforo refere-se ao conteúdo de calor ou mudança de energia associada às suas reações ou transformações químicas.
P: O que é P2S5?
R: P2S5 é a fórmula molecular do pentassulfeto de difósforo, um composto que consiste em dois átomos de fósforo ligados a cinco átomos de enxofre.
P: Quantos gramas de enxofre existem em 45,0 g de P2S5?
R: 45,0 g de P2S5 contém aproximadamente 28,13 g de enxofre.
P: Quantas moléculas de P2S5 você precisa para fazer 222 gramas?
R: Aproximadamente 1,54 x 10 ^ 23 moléculas de P2S5 são necessárias para igualar 222 gramas.
P: Qual é o nome do P2S5?
R: O nome de P2S5 é pentassulfeto de fósforo.
P: O P2S5 é um eletrólito fraco?
R: Não, P2S5 não é um eletrólito fraco; é um não eletrólito.
P: Como posso saber se o tamanho da partícula P2S5 está incorreto?
R: O tamanho incorreto de partícula de P2S5 pode ser determinado observando desvios das propriedades físicas e comportamento esperados do composto.
P: O que é P2S5 ochem2?
R: “ochem2” não é um termo ou designação reconhecido para P2S5 no campo da química orgânica.
P: Como é chamado o composto P2S5?
R: O composto P2S5 é chamado pentassulfeto de difósforo.
P: O que é P2S5 em química?
R: Em química, P2S5 representa a fórmula molecular do pentassulfeto de difósforo, um composto usado em diversas aplicações e reações químicas.
