Heptóxido de cloro ou Cl2O7 é um composto altamente explosivo e reativo. Pode se decompor violentamente em contato com matéria orgânica e é um poderoso agente oxidante usado em síntese e análise química.
| Nome IUPAC | Heptóxido de cloro |
| Fórmula molecular | Cl2O7 |
| Número CAS | 12015-53-1 |
| Sinônimos | Anidrido perclórico, heptóxido de dicloro, óxido de cloro (VII), óxido de cloro, perclorato de percloril |
| InChI | InChI=1S/Cl2O7/c2-1(3,4,5,6)10-7(8,9)11-12-13-14-10 |
Massa molar de heptóxido de cloro
O heptóxido de cloro, fórmula química Cl2O7, tem massa molar de 182,9 g/mol. Este composto é composto por dois átomos de cloro e sete átomos de oxigênio, o que o torna um agente altamente oxidante. A massa molar do heptóxido de cloro é usada para calcular a quantidade de substância em uma determinada massa ou volume de uma amostra usando a constante de Avogadro.
Ponto de ebulição do heptóxido de cloro
O heptóxido de cloro é um sólido incolor a amarelado, altamente reativo e volátil. O ponto de ebulição do heptóxido de cloro não está bem definido, pois ele se decompõe antes de atingir o ponto de ebulição. O heptóxido de cloro é um poderoso agente oxidante que pode reagir com matéria orgânica, água e outras substâncias para formar compostos explosivos.
Ponto de fusão do heptóxido de cloro
O heptóxido de cloro tem um ponto de fusão de -96°C (-141°F), tornando-o um sólido de baixo ponto de fusão. O heptóxido de cloro pode existir como um líquido amarelado à temperatura ambiente devido ao seu baixo ponto de fusão e alta reatividade. É importante manusear o heptóxido de cloro com cuidado, pois pode causar queimaduras graves e é um forte agente oxidante.
Densidade de heptóxido de cloro g/ml
A densidade do heptóxido de cloro é 2,48 g/mL à temperatura ambiente. A alta densidade do heptóxido de cloro o torna um líquido denso que pode afundar rapidamente no fundo de um recipiente. A alta densidade e reatividade do heptóxido de cloro tornam-no um composto difícil de manusear e requer precauções especiais de segurança quando utilizado em síntese ou análise química.
Peso molecular do heptóxido de cloro
O peso molecular do heptóxido de cloro, também conhecido como massa molecular relativa, é 182,9 g/mol. O peso molecular do heptóxido de cloro é importante em cálculos químicos que envolvem quantidade, massa e volume de substância. O alto peso molecular do heptóxido de cloro o torna um composto denso e volátil que requer manuseio e armazenamento cuidadosos.
Estrutura do heptóxido de cloro
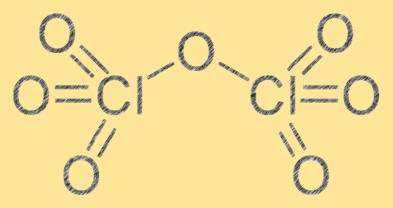
A estrutura do heptóxido de cloro é composta por dois átomos de cloro e sete átomos de oxigênio. Tem uma fórmula molecular de Cl2O7 e sua geometria molecular é uma forma octaédrica distorcida devido à repulsão entre os átomos de oxigênio. O heptóxido de cloro é um forte agente oxidante e pode reagir com diversas substâncias orgânicas e inorgânicas. A estrutura do heptóxido de cloro é essencial para a compreensão de suas propriedades químicas e de seu comportamento em diferentes reações.
Fórmula de heptóxido de cloro
A fórmula química do heptóxido de cloro é Cl2O7. A fórmula indica que cada molécula de heptóxido de cloro contém dois átomos de cloro e sete átomos de oxigênio. A fórmula é usada para calcular a estequiometria de reações químicas envolvendo heptóxido de cloro. A fórmula do heptóxido de cloro também é importante na determinação de seu peso molecular, densidade e outras propriedades físicas e químicas.
| Aparência | Sólido incolor a amarelado |
| Gravidade Específica | 2,48 a 25°C |
| Cor | Incolor a amarelado |
| Cheiro | Picante, azedo |
| Massa molar | 182,9 g/mol |
| Densidade | 2,48 g/mL a 25°C |
| Ponto de fusão | -96°C (-141°F) |
| Ponto de ebulição | Decompõe-se antes do ponto de ebulição |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Reage violentamente com água |
| Solubilidade | Solúvel em solventes orgânicos |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Não aplicável |
Segurança e perigos do heptóxido de cloro
O heptóxido de cloro é um composto altamente reativo e perigoso que apresenta riscos significativos à segurança se não for manuseado adequadamente. Pode causar queimaduras graves e danos aos olhos, pele e sistema respiratório em contato. O heptóxido de cloro também pode reagir violentamente com água e materiais orgânicos, causando explosões e risco de incêndio. É essencial usar equipamento de proteção individual adequado, incluindo luvas, óculos de proteção e respiradores ao manusear heptóxido de cloro. O composto deve ser armazenado e transportado em um recipiente seguro e bem fechado, longe de fontes de ignição, calor ou umidade. Procedimentos de manuseio adequados e precauções de segurança devem ser seguidos para minimizar os riscos associados ao heptóxido de cloro.
| Símbolos de perigo | Agente oxidante, corrosivo |
| Descrição de segurança | Evite contato com água, ácidos, materiais orgânicos e agentes redutores. Utilize equipamento de proteção individual adequado. Armazenar em recipiente bem fechado, longe do calor, umidade e fontes de ignição. Em caso de contato com os olhos, pele ou aparelho respiratório, procurar imediatamente atendimento médico. |
| Números de identificação da ONU | ONU 3083 |
| Código SH | 28299090 |
| Classe de perigo | 5.1 (Materiais oxidantes) |
| Grupo de embalagem | II |
| Toxicidade | Muito tóxico por inalação, ingestão ou absorção pela pele. Causa queimaduras graves e danos aos tecidos. Pode causar explosões e risco de incêndio em contato com água, materiais orgânicos e outras substâncias reativas. |
Métodos para a síntese de heptóxido de cloro
O heptóxido de cloro é um composto altamente reativo e difícil de sintetizar.
Um dos métodos mais comuns de síntese de heptóxido de cloro é a reação do gás cloro e do ozônio. Esta reação é exotérmica e pode levar a uma reação explosiva se não for cuidadosamente controlada.
Outro método envolve a reação do gás cloro com clorato de potássio, que produz heptóxido de cloro e cloreto de potássio como subprodutos. Este método também requer um controle cuidadoso das condições de reação para evitar a formação de intermediários explosivos.
O heptóxido de cloro pode ser sintetizado pela reação do gás cloro com pentóxido de dicloro, que produz heptóxido de cloro e hexóxido de dicloro como subprodutos. No entanto, os pesquisadores não costumam usar este método devido à natureza perigosa do pentóxido de dicloro.
Outros métodos de síntese de heptóxido de cloro incluem a reação de cloro gasoso com vários compostos orgânicos, como benzeno ou tolueno, sob condições controladas. No entanto, estes métodos requerem uma otimização cuidadosa das condições de reação e não são tão confiáveis ou comumente usados como os métodos cloro-ozônio ou cloro-clorato de potássio.
No geral, a síntese de heptóxido de cloro requer um controle cuidadoso das condições de reação e apresenta riscos de segurança significativos devido à natureza altamente reativa do composto. Precauções de segurança e procedimentos de manuseio adequados devem ser seguidos ao trabalhar com heptóxido de cloro ou qualquer outra substância perigosa.
Usos do heptóxido de cloro
- Cl2O7 encontra seu principal uso como agente oxidante em síntese química e pesquisa.
- Atua como um poderoso oxidante, reagindo com uma ampla gama de compostos orgânicos e inorgânicos, tornando-o útil em muitas reações químicas.
- Um dos usos mais comuns do Cl2O7 é a produção de dióxido de cloro, um poderoso desinfetante e agente branqueador usado no tratamento de água, na produção de celulose e papel e na fabricação de têxteis.
- Também é utilizado como um poderoso oxidante na síntese de diversos compostos orgânicos, incluindo farmacêuticos e agroquímicos.
- Cl2O7 é usado na academia e na pesquisa para estudar a reatividade de vários compostos orgânicos e inorgânicos. Também serve como catalisador na síntese de certos compostos, como resinas epóxi e anidrido acético.
- Devido à sua natureza perigosa, as aplicações industriais em grande escala geralmente não utilizam Cl2O7. Requer manuseio e armazenamento cuidadosos para evitar a formação de intermediários explosivos e outros riscos à segurança.
No geral, o Cl2O7 é um composto útil na síntese química e na pesquisa, mas requer precauções de segurança e procedimentos de manuseio adequados para minimizar os riscos associados ao seu uso.
Questões:
P: O que é Cl2O7?
R: Cl2O7 é um composto químico composto por dois átomos de cloro e sete átomos de oxigênio, com a fórmula química Cl2O7.
P: Qual é o nome correto para Cl2O7?
R: O nome correto para Cl2O7 é heptóxido de dicloro.
P: O Cl2O7 é iônico ou covalente?
R: Cl2O7 é um composto covalente. É composto por dois elementos não metálicos, cloro e oxigênio, e forma um composto molecular através do compartilhamento de elétrons entre os átomos.
P: Qual óxido abaixo reage com a água para formar um ácido fraco? MgO, Cl2O7, P4O10, Bi2O3, N2O5.
R: O óxido que reage com a água para formar um ácido fraco é o N2O5. Quando o N2O5 reage com a água, forma ácido nítrico, que é um ácido fraco. Os outros óxidos listados, MgO, P4O10, Bi2O3 e Cl2O7, não reagem com a água para formar ácidos fracos.
