O dicromato de sódio é um composto químico. É um agente oxidante e uma substância altamente tóxica. É utilizado em diversos processos industriais, como metalurgia e produção de pigmentos.
| Nome IUPAC | Dicromato de sódio |
| Fórmula molecular | Na2Cr2O7 |
| Número CAS | 10588-01-9 |
| Sinônimos | Dicromato de sódio, Dicromato dissódico, Dicromato de sódio |
| InChI | InChI=1S/2Cr.2Na.7O/q2*+6;2*+1;7*-2 |
Propriedades do dicromato de sódio
Fórmula de dicromato de sódio
A fórmula do dicromato de sódio é Na2Cr2O7. Consiste em dois átomos de sódio (Na), dois átomos de cromo (Cr) e sete átomos de oxigênio (O). A fórmula representa a proporção de cada elemento no composto.
Massa molar de dicromato de sódio
A massa molar do dicromato de sódio é calculada somando as massas atômicas de todos os seus elementos constituintes. O sódio (Na) tem massa atômica de 22,99 g/mol, o cromo (Cr) tem massa de 51,99 g/mol e o oxigênio (O) tem massa de 16,00 g/mol. A adição desses valores dá uma massa molar de 261,97 g/mol para o dicromato de sódio.
Ponto de ebulição do dicromato de sódio
O dicromato de sódio tem um ponto de ebulição de aproximadamente 400°C (752°F). Esta é a temperatura na qual o composto muda de uma fase líquida para uma fase gasosa quando aquecido sob pressão atmosférica normal.
Ponto de fusão do dicromato de sódio
O ponto de fusão do dicromato de sódio é de aproximadamente 357°C (675°F). Esta é a temperatura na qual o composto sólido se transforma no estado líquido. É importante notar que o ponto de fusão pode variar ligeiramente dependendo da pureza da amostra.
Densidade de dicromato de sódio g/mL
A densidade do dicromato de sódio é de aproximadamente 2,52 g/mL. A densidade é uma medida da massa de uma substância por unidade de volume. No caso do dicromato de sódio, este valor indica que um determinado volume do composto é relativamente pesado.
Peso molecular do dicromato de sódio
O peso molecular do dicromato de sódio é 261,97 g/mol. Este valor representa a soma dos pesos atômicos de todos os átomos presentes em uma molécula do composto.
Estrutura do dicromato de sódio
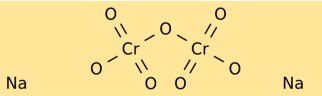
O dicromato de sódio possui uma estrutura cristalina formando cristais vermelho-laranja brilhantes. Consiste em íons de sódio (Na+) e íons dicromato (Cr2O7^2-). O íon dicromato possui um átomo central de cromo ligado a dois átomos de oxigênio de um lado e três átomos de oxigênio do outro lado.
Solubilidade do dicromato de sódio
O dicromato de sódio é muito solúvel em água. Dissolve-se facilmente em água, formando uma solução amarelo-laranja. A solubilidade do dicromato de sódio em água é influenciada por fatores como temperatura e pH, com temperaturas mais altas e níveis mais baixos de pH aumentando sua solubilidade.
| Aparência | Cristais vermelho-laranja |
| Gravidade Específica | 2,52 |
| Cor | Vermelho-laranja brilhante |
| Cheiro | Inodoro |
| Massa molar | 261,97 g/mol |
| Densidade | 2,52g/ml |
| Ponto de fusão | 357°C (675°F) |
| Ponto de ebulição | 400°C (752°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em água, ligeiramente solúvel em etanol/metanol |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Não disponível |
Segurança e perigos do dicromato de sódio
O dicromato de sódio apresenta riscos de segurança significativos. É altamente tóxico se ingerido, inalado ou absorvido pela pele. Isso pode causar queimaduras graves e danos aos olhos por contato. O composto também é classificado como potencial cancerígeno, capaz de causar câncer. Além disso, é um agente oxidante, o que significa que pode reagir violentamente com materiais combustíveis, aumentando o risco de incêndio ou explosão. Devem ser tomadas precauções de segurança adequadas ao manusear o dicromato de sódio, incluindo o uso de roupas de proteção, luvas e óculos. Deve ser armazenado em local seguro e bem ventilado, longe de substâncias incompatíveis. Se exposto ou ingerido, atenção médica imediata é crucial.
| Símbolos de perigo | Corrosivo, perigoso para a saúde |
| Descrição de segurança | Muito tóxico, corrosivo, cancerígeno |
| Números de identificação da ONU | UN3086 |
| Código SH | 28415000 |
| Classe de perigo | 6.1 |
| Grupo de embalagem | II |
| Toxicidade | Muito tóxico |
Métodos para a síntese de dicromato de sódio
Existem vários métodos para sintetizar dicromato de sódio. Um método comumente usado é a reação entre cromato de sódio (Na2CrO4) e dicromato de sódio (Na2Cr2O7). O ácido sulfúrico (H2SO4) reage com o cromato de sódio, produzindo dicromato de sódio e água. A equação química para esta reação é:
2Na2CrO4 + 2H2SO4 → Na2Cr2O7 + Na2SO4 + H2O
Outro método envolve a oxidação do cromato de sódio utilizando um agente oxidante forte, como o permanganato de potássio (KMnO4) . Nesta reação, o cromato de sódio reage com o permanganato de potássio na presença de ácido sulfúrico para produzir dicromato de sódio, dióxido de manganês (MnO2) e água.
2Na2CrO4 + 6KMnO4 + 7H2SO4 → 2Na2Cr2O7 + 6MnO2 + 7K2SO4 + 8H2O
A reação entre hidróxido de sódio (NaOH) e trióxido de cromo (CrO3) produz dicromato de sódio. A reação ocorre em meio aquoso e produz dicromato de sódio e água.
2NaOH + CrO3 → Na2Cr2O7 + H2O
Ao implementar estes métodos sintéticos, os indivíduos devem ter cautela devido à natureza tóxica e perigosa do dicromato de sódio. A utilização de medidas de segurança e equipamentos de proteção adequados é imprescindível para garantir o bem-estar dos envolvidos no processo.
Usos do dicromato de sódio
O dicromato de sódio tem diversas aplicações em diferentes indústrias. Aqui estão alguns de seus usos:
- Chapeamento de metal: Os processos de galvanoplastia usam dicromato de sódio para aplicar um revestimento protetor e decorativo em diversas superfícies metálicas, como aço, alumínio e zinco.
- Produção de pigmentos: O dicromato de sódio desempenha um papel vital na produção de pigmentos como amarelo cromo e verde cromo, amplamente encontrados em tintas, tintas e corantes.
- Preservante de Madeira: O dicromato de sódio, com suas fortes propriedades oxidantes, preserva a madeira contra o apodrecimento, insetos e fungos, principalmente em aplicações externas.
- Curtimento de couro: A indústria de curtume utiliza dicromato de sódio como mordente durante o processo de tratamento do couro, melhorando assim a solidez da cor e durabilidade do couro.
- Síntese Química: O dicromato de sódio atua como reagente em diversas reações químicas, incluindo a síntese de compostos orgânicos, reações de oxidação e a preparação de outros compostos de cromo.
- Aplicações laboratoriais: O dicromato de sódio encontra aplicações laboratoriais para testes analíticos, padrões de calibração e pesquisas químicas.
- Indústria Têxtil: O dicromato de sódio melhora a solidez da cor e promove melhor adesão dos corantes ao tecido durante os processos de tingimento e impressão têxtil.
- Fotografia: O dicromato de sódio é um componente crucial em emulsões fotossensíveis e funciona como agente oxidante em alguns processos fotográficos.
É importante manusear o dicromato de sódio com cuidado, seguindo as instruções de segurança e métodos de descarte adequados, devido à sua toxicidade e impacto ao meio ambiente.
Questões:
P: Quantos átomos de oxigênio existem em 3,00 g de dicromato de sódio, Na2Cr2O7?
R: Existem 6,02 x 10 ^ 22 átomos de oxigênio em 3,00 g de dicromato de sódio.
P: Quantos átomos de oxigênio existem em 4,00 g de dicromato de sódio, Na2Cr2O7?
R: Existem 8,03 x 10 ^ 22 átomos de oxigênio em 4,00 g de dicromato de sódio.
P: Quantos átomos de oxigênio existem em 5,00 g de dicromato de sódio, Na2Cr2O7?
R: Existem 1,00 x 10 ^ 23 átomos de oxigênio em 5,00 g de dicromato de sódio.
P: Quantos átomos de oxigênio existem em 6,00 g de dicromato de sódio, Na2Cr2O7?
R: Existem 1,20 x 10 ^ 23 átomos de oxigênio em 6,00 g de dicromato de sódio.
P: Quantos átomos de oxigênio existem em 7,00 g de dicromato de sódio?
R: Existem 1,40 x 10 ^ 23 átomos de oxigênio em 7,00 g de dicromato de sódio.
P: MSDS de dicromato de sódio?
R: A Ficha de Dados de Segurança de Material (MSDS) do dicromato de sódio fornece informações detalhadas sobre suas propriedades, precauções de manuseio e medidas de segurança.
P: O que poderia substituir o dicromato de sódio?
R: As alternativas ao dicromato de sódio incluem outros compostos de cromo, como sais de cromo trivalente ou substâncias sem cromo, dependendo da aplicação específica.
P: Para que é usado o dicromato de sódio?
R: O dicromato de sódio é utilizado como agente oxidante, preservativo de madeira e pigmento, bem como em diversos processos industriais, como revestimento de metais e curtimento de couro.
P: A solução de cromato amarelo pode ser feita a partir de dicromato de sódio di-hidratado?
R: Sim, uma solução de cromato amarelo pode ser preparada dissolvendo dicromato de sódio di-hidratado em água.
P: Qual é a fórmula do dicromato de sódio?
R: A fórmula do dicromato de sódio é Na2Cr2O7.
P: O dicromato de sódio é inorgânico?
R: Sim, o dicromato de sódio é um composto inorgânico.
P: Para que serve o teste de dicromato de sódio?
R: O dicromato de sódio pode ser usado para fins de teste, por exemplo, para avaliar a presença de certas substâncias ou monitorar reações químicas específicas.
