O dicromato de potássio é um composto químico laranja brilhante usado em diversas aplicações. É um forte agente oxidante e pode ser tóxico se ingerido ou inalado.
| Nome IUPAC | Dicromato de potássio |
| Fórmula molecular | K2Cr2O7 |
| Número CAS | 7778-50-9 |
| Sinônimos | Dicromato de potássio, Cromato de potássio (VI), Dicromato de potássio |
| InChI | InChI=1S/2Cr.2K.7O/q;;2*+1;;;;;;/h;;2*;7*1- |
Propriedades do dicromato de potássio
Fórmula de dicromato de potássio
A fórmula do dicromato de potássio é K2Cr2O7. Consiste em dois átomos de potássio (K), dois átomos de cromo (Cr) e sete átomos de oxigênio (O). Cada átomo de potássio tem carga +1, enquanto cada átomo de cromo tem carga +6. A presença de dois átomos de cromo na fórmula indica a estrutura dimérica do composto.
Massa molar de Dicromato de Potássio
A massa molar do dicromato de potássio é calculada somando as massas atômicas de seus elementos constituintes. O potássio tem massa molar de 39,10 gramas por mol (g/mol), o cromo tem massa molar de 52,00 g/mol e o oxigênio tem massa molar de 16,00 g/mol. A massa molar do dicromato de potássio é, portanto, 294,18 g/mol.
Ponto de ebulição do dicromato de potássio
O dicromato de potássio não possui ponto de ebulição específico, pois se decompõe antes de atingir o ponto de ebulição. Porém, quando aquecido, sofre decomposição térmica, liberando vapores tóxicos de óxido de cromo e oxigênio.
Ponto de fusão de dicromato de potássio
O ponto de fusão do dicromato de potássio é de aproximadamente 398 graus Celsius (°C) ou 748 graus Fahrenheit (°F). A esta temperatura, os cristais sólidos de dicromato de potássio transformam-se no estado líquido.
Densidade de dicromato de potássio g/mL
A densidade do dicromato de potássio é de aproximadamente 2,68 gramas por mililitro (g/mL). Isto indica que um determinado volume de dicromato de potássio é relativamente mais pesado que um volume igual de água.
Peso molecular do dicromato de potássio
O peso molecular do dicromato de potássio é igual à sua massa molar, que é 294,18 gramas por mol (g/mol). Representa a massa combinada de todos os átomos presentes em uma molécula do composto.
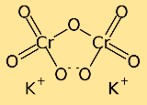
Estrutura do dicromato de potássio
O dicromato de potássio tem uma estrutura dimérica, o que significa que é composto por dois átomos de cromo ligados entre si por átomos de oxigênio. Os átomos de potássio também estão ligados aos átomos de oxigênio, criando uma rede complexa de átomos no composto.
Solubilidade do dicromato de potássio
O dicromato de potássio é muito solúvel em água. Dissolve-se facilmente em água para formar uma solução laranja. A solubilidade do dicromato de potássio aumenta com a temperatura. Contudo, a sua solubilidade em solventes orgânicos é limitada.
| Aparência | Cristais laranja brilhantes |
| Gravidade Específica | 2,68 g/ml |
| Cor | Laranja |
| Cheiro | Inodoro |
| Massa molar | 294,18 g/mol |
| Densidade | 2,68 g/ml |
| Ponto de fusão | 398°C (748°F) |
| Ponto de ebulição | Decomposto |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em água, limitado em solventes orgânicos |
| Pressão de vapor | Insignificante |
| Densidade do vapor | Não disponível |
| pKa | Não aplicável |
| pH | Ácido (em torno de pH 4) |
Segurança e perigos do dicromato de potássio
O dicromato de potássio apresenta riscos de segurança significativos. É altamente tóxico se ingerido, inalado ou em contato com a pele. O composto é um forte agente oxidante que pode reagir violentamente com materiais combustíveis, aumentando o risco de incêndio. A exposição ao dicromato de potássio pode causar irritação cutânea grave, queimaduras e reações alérgicas. A inalação de seus vapores ou poeira pode causar problemas respiratórios e danos aos pulmões. A exposição a longo prazo está associada a efeitos adversos à saúde, incluindo câncer de pulmão induzido por cromato. É essencial manusear o dicromato de potássio com extremo cuidado, usando equipamento de proteção adequado e garantindo ventilação adequada para minimizar os riscos à saúde e à segurança.
| Símbolos de perigo | Corrosivo, Perigo para a saúde, Tóxico agudo |
| Descrição de segurança | – Muito tóxico – Corrosivo – Provoca queimaduras |
| Números de identificação da ONU | ONU 3086 (classe 6.1) |
| Código SH | 2841.10.10 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | III |
| Toxicidade | Toxicidade oral aguda: Muito tóxico<br>Toxicidade crônica: Potencial carcinogênico |
Nota: Os símbolos de perigo utilizados na tabela são símbolos internacionais comumente reconhecidos. É importante consultar regulamentos específicos e instruções de segurança para obter informações completas sobre o manuseio e armazenamento do dicromato de potássio.
Métodos de síntese de dicromato de potássio
Existem vários métodos para sintetizar dicromato de potássio. Um método comumente usado envolve a reação entre cromato de potássio (K2CrO4) e ácido crômico (H2CrO4) . A reação ocorre em ambiente ácido, geralmente com ácido sulfúrico (H2SO4) como catalisador. A reação pode resumir tudo.
2K2CrO4 + 2H2CrO4 + 2H2SO4 → K2Cr2O7 + Cr2(SO4)3 + 4H2O
Outro método envolve a oxidação do cromato de potássio utilizando um agente oxidante forte, como o ácido sulfúrico concentrado (H2SO4) , e um agente redutor, como o etanol (C2H5OH). A reação pode resumir tudo.
2K2CrO4 + H2SO4 + 3C2H5OH → K2Cr2O7 + Cr2(SO4)3 + 7H2O + 3CO2
O hidróxido de potássio (KOH) reage com o trióxido de cromo (CrO3) em meio aquoso para produzir dicromato de potássio. Em meio aquoso, a reação ocorre. A reação pode resumir tudo.
2KOH + CrO3 → K2Cr2O7 + H2O
Estes métodos de síntese requerem precauções de segurança adequadas devido à natureza tóxica e corrosiva dos reagentes envolvidos. É importante realizar essas reações em uma área bem ventilada, usar equipamento de proteção e manusear os produtos químicos com cuidado. Além disso, seguir protocolos adequados de descarte de resíduos é essencial para minimizar o impacto ambiental.
Usos do Dicromato de Potássio
O dicromato de potássio encontra aplicações em vários campos devido às suas propriedades únicas. Aqui estão alguns de seus usos comuns:
- Agente oxidante: As reações químicas utilizam amplamente o dicromato de potássio como um forte agente oxidante para oxidar álcoois em aldeídos ou cetonas.
- Reagente de Laboratório: A química analítica utiliza dicromato de potássio como reagente para testes e experimentos, incluindo determinação de compostos orgânicos e realização de reações redox.
- Indústria de Curtumes: A indústria do couro utiliza dicromato de potássio como agente de curtimento para tratar peles de animais e transformá-las em produtos de couro duráveis.
- Fotografia: A fotografia em preto e branco incorpora dicromato de potássio em soluções de revelação e o utiliza para sensibilizar emulsões para obter efeitos fotográficos específicos.
- Preservação de madeira: Para proteger a madeira contra o apodrecimento, fungos e ataque de insetos, a indústria de preservação de madeira utiliza dicromato de potássio como preservante de madeira altamente tóxico.
- Fabricação de pigmentos: O dicromato de potássio desempenha um papel vital na produção de pigmentos como amarelo cromo e laranja cromo, que as indústrias utilizam em tintas, tintas e corantes.
- Galvanoplastia: Os processos de galvanoplastia usam dicromato de potássio para fornecer um revestimento decorativo e resistente à corrosão em metais, incluindo zinco, alumínio e latão.
- Pirotecnia: O dicromato de potássio desempenha um papel essencial nas misturas pirotécnicas, proporcionando cores laranja brilhantes aos fogos de artifício e sinalizadores.
- Indústria Têxtil: O tingimento e a impressão têxtil incorporam dicromato de potássio para obter as cores desejadas e melhorar a solidez da cor.
- Calibração de vidrarias de laboratório: Para medições precisas de volume, soluções de dicromato de potássio são usadas para calibrar vidrarias de laboratório.
Estas diversas aplicações destacam a versatilidade e a importância do dicromato de potássio em diversas indústrias e empreendimentos científicos.
Questões:
P: Qual é a fórmula correta do dicromato de potássio?
R: A fórmula correta para o dicromato de potássio é K2Cr2O7.
P: O que é dicromato de potássio?
R: O dicromato de potássio é um composto químico laranja brilhante e é comumente usado como agente oxidante.
P: O dicromato de potássio é iônico ou covalente?
R: O dicromato de potássio é um composto iônico.
P: Qual é a quantidade mínima de água necessária para dissolver 3 moles de dicromato de potássio?
R: A quantidade mínima de água necessária para dissolver 3 moles de dicromato de potássio é de aproximadamente 564 gramas.
P: Qual é a massa molar do dicromato de potássio?
R: A massa molar do dicromato de potássio é 294,18 gramas por mol (g/mol).
P: MSDS de dicromato de potássio?
R: As Fichas de Dados de Segurança de Materiais (MSDS) do dicromato de potássio fornecem informações detalhadas sobre seus perigos, manuseio, armazenamento e medidas de primeiros socorros. Consulte fontes ou fabricantes confiáveis para obter a MSDS específica.
P: Como o dicromato de potássio é preparado a partir do minério de cromita?
R: O dicromato de potássio pode ser preparado a partir do minério de cromita torrando-o com hidróxido de potássio ou carbonato de potássio e depois isolando o produto.
P: Quantos gramas de dicromato de potássio foram adicionados ao balão volumétrico?
R: O número exato de gramas de dicromato de potássio adicionado ao balão volumétrico depende da concentração e do volume desejados da solução.
P: Como você distinguiria entre propanal e propanona usando dicromato de potássio acidificado?
R: O propanal seria oxidado em ácido propanóico pelo dicromato de potássio acidificado, enquanto a propanona (acetona) não apresentaria reação.
P: O dicromato de potássio é um agente redutor?
R: Não, o dicromato de potássio é um agente oxidante.
P: Como escrever a fórmula do dicromato de potássio?
R: A fórmula do dicromato de potássio é K2Cr2O7.
