O cloreto mercúrico é um composto tóxico com a fórmula HgCl2. É um sólido cristalino branco utilizado em laboratórios como reagente e desinfetante, mas o manuseio adequado é essencial.
| Nome IUPAC | Cloreto de mercúrio (II) |
| Fórmula molecular | HgCl2 |
| Número CAS | 7487-94-7 |
| Sinônimos | Dicloreto de mercúrio, dicloreto de mercúrio, bicloreto de mercúrio, dicloreto de mercúrio (II) |
| InChI | InChI=1S/2ClH.Hg/h2*1H;/q;;+2/p-2 |
Propriedades do cloreto mercúrico
Fórmula de Cloreto Mercúrico
A fórmula do dicloreto de mercúrio é HgCl2. Consiste em um átomo de mercúrio (Hg) e dois átomos de cloro (Cl). Este composto também é conhecido como cloreto de mercúrio (II), simbolizando o estado de oxidação +2 do mercúrio.
Massa molar de cloreto mercúrico
A massa molar do dicloreto de mercúrio é aproximadamente 271,52 g/mol. É calculado adicionando as massas atômicas de um átomo de mercúrio (200,59 g/mol) e dois átomos de cloro (35,45 g/mol cada).
Ponto de ebulição do cloreto mercúrico
O dicloreto de mercúrio tem um ponto de ebulição de aproximadamente 302°C (575,6°F). A esta temperatura, o dicloreto de mercúrio sólido se transforma em vapor.
Ponto de fusão do cloreto mercúrico
O ponto de fusão do dicloreto de mercúrio é de aproximadamente -71°C (-95,8°F). A esta temperatura, o dicloreto de mercúrio sólido se transforma em líquido.
Densidade de cloreto mercúrico g/mL
A densidade do dicloreto de mercúrio é de aproximadamente 5,4 g/mL. Esta alta densidade torna-a uma substância relativamente pesada.
Peso molecular do cloreto mercúrico
O peso molecular do dicloreto de mercúrio é de aproximadamente 271,52 g/mol. Indica a massa de um mol do composto e corresponde à soma de seus pesos atômicos.
Estrutura do cloreto mercúrico
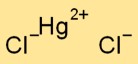
O dicloreto mercúrico possui uma estrutura cristalina. Consiste em íons de mercúrio carregados positivamente (Hg2+) e íons cloreto carregados negativamente (Cl-), mantidos juntos por ligações iônicas. O arranjo forma um padrão semelhante a uma treliça.
Solubilidade do cloreto mercúrico
O dicloreto mercúrico tem solubilidade limitada em água. Aproximadamente 7,7 gramas de dicloreto de mercúrio podem dissolver-se em 100 ml de água à temperatura ambiente (20°C). Sua solubilidade aumenta com temperaturas mais altas.
O dicloreto de mercúrio é uma substância altamente tóxica e deve ser manuseado com extremo cuidado. Tem sido amplamente utilizado em diversas aplicações, inclusive como reagente em laboratórios químicos, como desinfetante e em processos de galvanoplastia. Devido à sua toxicidade, é essencial seguir os protocolos de segurança adequados ao trabalhar com este composto.
| Aparência | Sólido cristalino branco |
| Gravidade Específica | 5,4 g/ml |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 271,52 g/mol |
| Densidade | 5,4 g/ml |
| Ponto de fusão | -71°C (-95,8°F) |
| Ponto de ebulição | 302°C (575,6°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Limite |
| Solubilidade | Solúvel em solventes orgânicos como álcool, éter |
| Pressão de vapor | Insignificante |
| Densidade do vapor | 8,23 (ar = 1) |
| pKa | Não aplicável |
| pH | Ácido (em água) |
Segurança e perigos do cloreto mercúrico
O dicloreto mercúrico apresenta riscos de segurança significativos devido à sua extrema toxicidade. O contato direto com a pele ou a inalação de seus vapores pode causar sérios problemas de saúde. É fundamental manuseá-lo com muito cuidado, utilizando equipamentos de proteção adequados como luvas e respirador. Sempre trabalhe em uma área bem ventilada para minimizar a exposição. Armazene-o em recipientes bem fechados, longe de substâncias incompatíveis. Em caso de ingestão ou exposição acidental, procure imediatamente atendimento médico. Métodos de descarte adequados devem ser seguidos para evitar a contaminação do meio ambiente. No geral, a adesão estrita aos protocolos de segurança é crucial quando se lida com dicloreto de mercúrio.
| Símbolos de perigo | Caveira e ossos cruzados, corrosivos |
| Descrição de segurança | Muito tóxico e corrosivo. Use com extremo cuidado. Evite o contato direto e a inalação de vapores. |
| Números de identificação da ONU | UN1624 (Compostos de mercúrio, nos) |
| Código SH | 2852.10.10 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | II (Intermediário) |
| Toxicidade | Extremamente tóxico para humanos e animais. Manuseie com cuidado e siga protocolos de segurança rígidos. |
Métodos para a síntese de cloreto mercúrico
Existem diferentes métodos para sintetizar dicloreto de mercúrio.
Uma abordagem comum envolve a reação do mercúrio metálico com ácido clorídrico . Em um ambiente controlado, adicione mercúrio ao ácido para produzir dicloreto de mercúrio e liberar gás hidrogênio. A equação química para esta reação é:
Hg + 2HCl -> HgCl2 + H2
Outro método utiliza a reação entre óxido de mercúrio (HgO) e ácido clorídrico . Combine óxido mercúrico com ácido para formar dicloreto de mercúrio e água:
HgO + 2HCl -> HgCl2 + H2O
Além disso, o dicloreto de mercúrio pode ser produzido pela reação do mercúrio com cloro gasoso:
Hg + Cl2 -> HgCl2
Lembre-se de realizar a síntese de dicloreto de mercúrio somente sob uma coifa bem ventilada ou em condições controladas devido à sua natureza tóxica e corrosiva. O manuseio cuidadoso e o cumprimento das precauções de segurança são essenciais para evitar exposição prejudicial durante o processo de síntese.
Usos do cloreto mercúrico
O dicloreto de mercúrio, também conhecido como cloreto de mercúrio (II), encontrou diversas aplicações em diferentes campos devido às suas propriedades únicas. Aqui estão alguns de seus principais usos:
Reagente de Laboratório: O dicloreto de mercúrio serve como um importante reagente em laboratórios químicos para diversos procedimentos analíticos e sintéticos.
Desinfetante: Suas fortes propriedades antimicrobianas o tornam valioso como desinfetante, principalmente para esterilizar equipamentos e superfícies.
Medicina: Embora limitado devido à sua toxicidade, tem sido utilizado na medicina tradicional para certas condições.
Fotografia: No passado, o cloreto mercúrico desempenhou um papel nas primeiras fotografias como agente fixador para revelação de fotografias.
Galvanoplastia: Nos processos de galvanoplastia, os indivíduos usam dicloreto de mercúrio como eletrólito para depositar revestimentos metálicos em vários objetos.
Preservação da Madeira: Ao longo da história, as pessoas a utilizaram para tratar a madeira, protegendo-a do apodrecimento e das pragas.
Indústria têxtil: Os fabricantes utilizavam cloreto mercúrico para remover a cor dos têxteis durante os processos de tingimento.
Química Analítica: Os químicos a utilizam para testes e reações específicas em análises químicas.
Síntese orgânica de nicho: encontra aplicações em reações específicas de síntese orgânica.
Fungicida e Algicida: Os agricultores utilizam-no ativamente como fungicida e algicida para controlar o crescimento de fungos e algas na agricultura.
Questões:
P: O HgCl2 é solúvel ou insolúvel em água?
R: HgCl2 é ligeiramente solúvel em água.
P: Quais são o cátion e o ânion do composto HgCl2?
R: O cátion é Hg2+ (mercúrio) e o ânion é Cl- (cloreto).
P: O HgCl2 é iônico ou covalente?
R: HgCl2 é um composto iônico.
P: Como fazer cloreto de mercúrio no Minecraft?
R: No Minecraft, o Dicloreto de Mercúrio pode ser sintetizado combinando Mercúrio e Cloro em uma mesa de trabalho.
P: Para que é usado o cloreto mercúrico?
R: O dicloreto mercúrico é usado em laboratórios como reagente e desinfetante.
P: Quem inventou o cloreto mercúrico?
R: A descoberta e os primeiros usos do dicloreto de mercúrio remontam à antiguidade, por isso não possui um inventário específico.
P: Como fazer cloreto de mercúrio no Minecraft Education Edition?
R: No Minecraft Education Edition, o Dicloreto de Mercúrio pode ser criado combinando mercúrio e cloro em uma mesa de trabalho, assim como na versão padrão do Minecraft.
P: O que é cloreto mercúrico?
R: O dicloreto de mercúrio é um composto tóxico com a fórmula química HgCl2.
P: O HgCl2 é um sólido?
R: Sim, o HgCl2 é um sólido à temperatura ambiente.
P: Qual é o nome correto para HgCl2 na nomenclatura iônica?
R: O nome correto para HgCl2 na nomenclatura iônica é dicloreto de mercúrio (II).
P: Qual é o nome do HgCl2?
R: O nome de HgCl2 é dicloreto de mercúrio.
Q: 2 HgCl2(aq) + C2O4^(2-)(aq) → 2 Cl^-(aq) + 2 CO2(g) + Hg2Cl2(s), qual é a lei da velocidade da reação?
A: Lei de taxas: Taxa = k[HgCl2]^2[C2O4^2-] (segunda ordem em relação a HgCl2 e primeira ordem em relação a C2O4^2-).
