O cloreto de magnésio (MgCl2) é um composto composto por íons magnésio e cloreto. É comumente usado como suplemento para tratar a deficiência de magnésio e como descongelador de estradas e calçadas.
| Nome IUPAC | Cloreto de magnésio |
| Fórmula molecular | MgCl2 |
| Número CAS | 7786-30-3 |
| Sinônimos | Dicloreto de magnésio, cloromagnesita, biscloromagnésio, cloreto de magnésio (II), E511, Nigari |
| InChI | InChI=1S/2ClH.Mg/h2*1H;/q;;+2/p-2 |
Fórmula de Cloreto de Magnésio
A fórmula química do cloreto de magnésio é MgCl2. Esta fórmula indica que o cloreto de magnésio consiste em um íon Mg+2 e dois íons Cl-. A fórmula é importante para determinar a quantidade de cloreto de magnésio necessária para reações químicas. O cloreto de magnésio é comumente usado como suplemento para tratar a deficiência de magnésio e como descongelante para estradas e calçadas.
Massa molar de cloreto de magnésio
A massa molar do cloreto de magnésio é 95,21 g/mol. É um composto cristalino composto por um íon Mg+2 e dois íons Cl-. A massa molar é uma propriedade importante do cloreto de magnésio porque é usada para calcular a quantidade de substância em reações químicas. O cloreto de magnésio é comumente usado como suplemento para tratar a deficiência de magnésio e como descongelante para estradas e calçadas.
Ponto de ebulição do MgCl2
O MgCl2 tem um alto ponto de ebulição de 1.412°C, o que significa que requer muita energia para quebrar as ligações entre seus átomos e moléculas. Esta propriedade o torna útil em aplicações de alta temperatura, como na produção de metais e ligas. O MgCl2 também é usado como dessecante para absorver a umidade do ar e como catalisador em reações químicas.
Ponto de fusão do MgCl2
O ponto de fusão do MgCl2 é 714°C, o que significa que é um sólido à temperatura ambiente. Esta propriedade o torna útil em diversas aplicações, como na produção de magnésio metálico e como fluxo na soldagem de alumínio. O MgCl2 também é usado como coagulante na produção de tofu e outros produtos de soja.
Densidade MgCl2 g/ml
A densidade do MgCl2 é 2,32 g/ml. Esta propriedade o torna útil em diversas aplicações, como produção de materiais retardadores de chama e tratamento de águas residuais. O MgCl2 também é usado como supressor de poeira em estradas e na construção de rodovias.
Peso molecular de MgCl2
O peso molecular do MgCl2 é 95,21 g/mol. Esta propriedade é importante para determinar a quantidade de MgCl2 necessária para reações químicas. O MgCl2 é comumente usado como suplemento para tratar a deficiência de magnésio e como descongelante para estradas e calçadas.
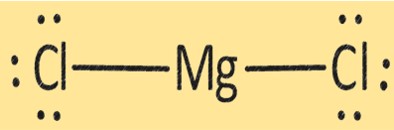
Estrutura MgCl2
O MgCl2 tem uma estrutura cristalina composta por um íon Mg+2 e dois íons Cl-. A estrutura do MgCl2 é importante na determinação de suas propriedades físicas e químicas. O MgCl2 é utilizado em diversas aplicações, como na produção de magnésio metálico, como dessecante e como coagulante na produção de tofu e outros produtos de soja.
| Aparência | Sólido cristalino branco |
| Gravidade Específica | 2,32g/ml |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 95,21 g/mol |
| Densidade | 2,32g/ml |
| Ponto de fusão | 714°C |
| Ponto de ebulição | 1412°C |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em água, etanol, metanol |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | 7,6 (para íons Mg(H2O)6^2+) |
| pH | 6,0 – 8,0 |
Segurança e perigos do cloreto de magnésio
O cloreto de magnésio (MgCl2) é geralmente considerado seguro quando usado conforme as instruções. No entanto, pode representar alguns perigos se não for manuseado corretamente. Pode causar irritação na pele e nos olhos e a inalação de poeira pode causar problemas respiratórios. A ingestão de grandes quantidades de MgCl2 pode causar náuseas, vômitos e diarreia. Também pode ser prejudicial à vida aquática se for lançado nos cursos de água. Equipamento de proteção adequado, como luvas e óculos de proteção, deve ser usado ao manusear MgCl2. Quaisquer derramamentos ou liberações devem ser contidos e limpos imediatamente para evitar danos ambientais.
| Símbolos de perigo | Nenhum atribuído |
| Descrição de segurança | Evitar o contato com a pele e os olhos. Em caso de contato, enxágue com água. Use luvas e óculos de proteção durante o manuseio. |
| Números de identificação da ONU | UM 2019 |
| Código SH | 28273100 |
| Classe de perigo | 8 |
| Grupo de embalagem | III |
| Toxicidade | LD50 (oral, rato) – 4.640 mg/kg; LC50 (inalação, rato) – >4,4 mg/L por 4 horas |
Métodos de síntese de cloreto de magnésio
Vários métodos podem sintetizar MgCl2, incluindo síntese direta, reação com ácido clorídrico e reação com MgO.
Para produzir MgCl2 por síntese direta, queime magnésio metálico em ar ou cloro gasoso para criar MgO. Em seguida, reaja o MgO com ácido clorídrico para produzir MgCl2:
Mg + O2 → MgO
MgO + 2HCl → MgCl2 + H2O
Outro método envolve a reação do Mg metálico com ácido clorídrico para produzir MgCl2 e gás hidrogênio:
Mg + 2HCl → MgCl2 + H2
Para a reação com MgO, misturamos MgO com ácido clorídrico para produzir MgCl2 e água:
MgO + 2HCl → MgCl2 + H2O
A mistura de MgO com ácido clorídrico produz cloreto de magnésio e água ao reagir com MgO:
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
Adicionalmente, podemos obter MgCl2 como subproduto do processo Solvay, que produz carbonato de sódio . O processo resulta na produção de cloreto de cálcio e MgCl2 como subprodutos, que podem ser separados da solução de carbonato de sódio.
Usos do cloreto de magnésio
O cloreto de magnésio tem uma ampla gama de utilizações em diversas indústrias, incluindo:
- Agente Degelo: Utilizado como agente de degelo em estradas e calçadas durante os meses de inverno devido à sua capacidade de diminuir o ponto de congelamento da água.
- Controle de poeira: Usado como agente de controle de poeira em estradas não pavimentadas e canteiros de obras.
- Indústria alimentar: Utilizado como coagulante na produção de tofu e como fonte de magnésio em determinados produtos alimentares.
- Remédio: Usado medicinalmente como suplemento para deficiência de magnésio e como tratamento para certas condições, como prisão de ventre e azia.
- Agricultura: Usado como fertilizante e condicionador de solo para melhorar o teor de magnésio do solo e o crescimento das plantas.
- Tratamento de Água: Utilizado em processos de tratamento de água para remover impurezas e amaciar a água dura.
- Aplicações industriais: Utilizado na produção de têxteis, papel e cimento, bem como em diversos processos industriais.
- Saúde e Bem-Estar: Utilizado em diversas práticas de saúde e bem-estar, como banho, para promover relaxamento e melhorar a saúde da pele.
Questões:
P: Qual é a fórmula do cloreto de magnésio?
R: A fórmula do cloreto de magnésio é MgCl2.
P: O que é cloreto de magnésio?
R: MgCl2 é um composto inorgânico comumente usado em diversas indústrias e aplicações, inclusive como agente de degelo, agente de controle de poeira e aditivo alimentar.
P: O cloreto de magnésio é solúvel?
R: Sim, o MgCl2 é solúvel em água e outros solventes polares.
P: O cloreto de magnésio é iônico ou covalente?
R: MgCl2 é um composto iônico que consiste em um cátion (Mg2+) e um ânion (Cl-).
P: O que é MgCl2?
R: MgCl2 é a fórmula química do cloreto de magnésio, que é um composto inorgânico usado em diversas aplicações industriais e de consumo.
P: Qual é a equação iônica líquida para a reação de MgCl2 com NaOH?
R: A equação iônica líquida para a reação de MgCl2 com NaOH é Mg2+ (aq) + 2OH- (aq) → Mg(OH)2 (s).
