O cloreto de ferro (III) é um composto formado pela combinação de ferro e cloro. É utilizado como catalisador, no tratamento de água e como reagente em reações químicas.
| Nome IUPAC | Cloreto de ferro (III) |
| Fórmula molecular | FeCl₃ |
| Número CAS | 7705-08-0 |
| Sinônimos | Cloreto férrico, tricloreto de ferro, triclorofero |
| InChI | InChI=1S/ClH.3Fe/h1H;;;/q;;3*+3/p-3 |
Propriedades do cloreto de ferro (III)
Fórmula de cloreto de ferro (III)
A fórmula do tricloreto de ferro é FeCl₃. Representa a combinação de um átomo de ferro (Fe) e três átomos de cloro (Cl). Esta fórmula indica a razão estequiométrica de cada elemento do composto.
Cloreto De Ferro(III) Massa molar
A massa molar do tricloreto de ferro é calculada somando as massas atômicas de todos os seus elementos constituintes. O ferro tem massa atômica de 55.845 g/mol, enquanto o cloro tem massa atômica de 35.453 g/mol. Multiplicar a massa atômica do ferro por um e a massa atômica do cloro por três dá uma massa molar de 162,204 g/mol para o tricloreto de ferro.
Ponto de ebulição do cloreto de ferro (III)
O tricloreto de ferro tem um ponto de ebulição de aproximadamente 315°C (599°F). A esta temperatura, o composto sofre uma transição de fase de líquido para gás. O ponto de ebulição é uma medida da pressão de vapor exercida pela substância quando sua temperatura atinge um valor específico.
Ponto de fusão do cloreto de ferro (III)
O ponto de fusão do tricloreto de ferro é de aproximadamente 306°C (583°F). Esta temperatura representa o ponto em que o composto sólido se transforma em líquido. O ponto de fusão é uma propriedade característica de uma substância e permite sua identificação.
Densidade de cloreto de ferro (III) g/mL
A densidade do tricloreto de ferro é de aproximadamente 2,90 g/mL. A densidade é definida como a massa de uma substância por unidade de volume. A densidade do tricloreto de ferro indica que é um composto relativamente denso.
Peso molecular do cloreto de ferro (III)
O peso molecular do tricloreto de ferro é calculado somando os pesos atômicos de seus elementos constituintes. Com um átomo de ferro pesando 55,845 g/mol e três átomos de cloro pesando cada um 35,453 g/mol, o peso molecular do tricloreto de ferro é 162,204 g/mol.
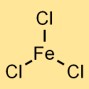
Estrutura do cloreto de ferro (III)
O tricloreto de ferro tem uma estrutura cristalina. Forma uma ligação iônica, com o átomo de ferro (Fe³⁺) atraindo três íons cloro (Cl⁻). O composto resultante adota um arranjo cristalino no qual íons de ferro carregados positivamente são cercados por íons cloreto carregados negativamente.
Solubilidade do cloreto de ferro (III)
O tricloreto de ferro é solúvel em água, etanol e outros solventes polares. Quando dissolvido em água, sofre dissociação, formando cátions Fe³⁺ e ânions Cl⁻. A solubilidade do tricloreto de ferro em água é influenciada por fatores como temperatura e concentração, com temperaturas e concentrações mais altas resultando em maior solubilidade.
| Aparência | Sólido amarelo-marrom |
| Gravidade Específica | 2,90g/ml |
| Cor | Amarelo marrom |
| Cheiro | Inodoro |
| Massa molar | 162.204 g/mol |
| Densidade | 2,90g/ml |
| Ponto de fusão | 306°C (583°F) |
| Ponto de ebulição | 315°C (599°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solúvel, influenciado por fatores como temperatura e concentração |
| Solubilidade | Solúvel em solventes polares |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Ácido (cerca de 2) |
Segurança e perigos do cloreto de ferro (III)
O tricloreto de ferro apresenta certas considerações de segurança e perigos. É corrosivo e pode causar irritação grave na pele e nos olhos. A inalação de poeira ou vapores pode causar irritação do trato respiratório. É fundamental manusear este composto com cautela, utilizando equipamentos de proteção adequados, como luvas e óculos de segurança. Evite o contato direto e a inalação da substância. Em caso de contato com a pele ou olhos, enxaguar com água abundante e consultar um médico se necessário. O tricloreto de ferro deve ser armazenado em recipiente bem fechado, longe de substâncias incompatíveis. Siga os procedimentos de descarte adequados para evitar contaminação ambiental.
| Símbolos de perigo | Corrosivo (C) |
| Descrição de segurança | Causa queimaduras na pele e lesões oculares graves. |
| Números de identificação da ONU | UN3264 |
| Código SH | 2827.39.60 |
| Classe de perigo | 8 |
| Grupo de embalagem | II |
| Toxicidade | Moderadamente tóxico para humanos |
Métodos para a síntese de cloreto de ferro (III)
Existem vários métodos para sintetizar tricloreto de ferro.
Um método comum envolve a reação entre ferro e cloro gasoso. Em um ambiente controlado, como um reator, limalha de ferro ou pó de ferro combinam-se com cloro gasoso em altas temperaturas, geralmente em torno de 300 a 500 °C (572 a 932 °F), iniciadas pelo aquecimento da mistura. O ferro reage com o cloro , resultando na formação de tricloreto de ferro.
Outro método envolve a reação entre óxido de ferro, geralmente óxido de ferro (III) (Fe₂O₃), e ácido clorídrico (HCl) . Para promover a reação, o ácido clorídrico dissolve o óxido de ferro e a mistura é aquecida. À medida que a reação continua, forma tricloreto de ferro enquanto libera água.
A obtenção de tricloreto de ferro também é possível pela reação direta do ferro com ácido clorídrico concentrado. A adição de ferro à solução ácida inicia a reação, que continua com a liberação de gás hidrogênio. O aquecimento da mistura resultante facilita a conversão do ferro em tricloreto de ferro.
É importante ressaltar que estes métodos de síntese devem ser realizados com os devidos cuidados de segurança e em áreas bem ventiladas, pois algumas reações envolvem o uso de substâncias corrosivas e a geração de gases tóxicos.
Usos do cloreto de ferro (III)
O tricloreto de ferro encontra aplicações em diversos campos devido às suas propriedades versáteis. Aqui estão alguns usos comuns:
- Tratamento de Água: A coagulação em processos de tratamento de água utiliza amplamente o tricloreto de ferro para remover impurezas e partículas em suspensão, tornando a água adequada para beber.
- Condicionador: A indústria eletrônica usa tricloreto de ferro como decapante para produzir placas de circuito impresso, gravar cobre seletivamente e permitir a criação de projetos de circuitos.
- Catalisador: O tricloreto de ferro catalisa diversas reações químicas, incluindo a síntese de compostos orgânicos e a cloração de compostos aromáticos.
- Produção de pigmentos: A produção de diversos pigmentos, como azul de ferro e toners utilizados em tintas de impressão, envolve o uso de tricloreto de ferro.
- Fabricação de corantes: A síntese de corantes, principalmente para coloração de têxteis, couro e papel, utiliza tricloreto de ferro.
- Tratamento de superfície de metais: Melhorar a resistência à corrosão de metais, como alumínio e aço inoxidável, envolve o uso de tricloreto de ferro como agente de tratamento de superfície.
- Reagente de Laboratório: O tricloreto de ferro é comumente usado como reagente de laboratório para vários fins analíticos e sintéticos.
- Aplicações Medicinais: A preparação de alguns produtos farmacêuticos, como suplementos de ferro e medicamentos utilizados no tratamento da anemia, utiliza o tricloreto de ferro medicinalmente.
- Fotografia: O tricloreto de ferro atua como agente tonificante em processos fotográficos, criando tons sépia na fotografia em preto e branco.
- Indústria Têxtil: A mordente e tingimento de tecidos na indústria têxtil utiliza tricloreto de ferro para melhorar a solidez da cor e a absorção do corante.
Essas diversas aplicações destacam a importância do tricloreto de ferro em diversas indústrias e campos científicos.
Questões:
P: Qual é a massa molar do cloreto de ferro (III), FeCl₃?
R: A massa molar do tricloreto de ferro é 162,204 g/mol.
P: Quantos átomos de ferro existem em uma unidade de fórmula de cloreto de ferro (III)?
R: Existe um átomo de ferro em uma unidade de fórmula de tricloreto de ferro.
P: Qual é a fórmula do cloreto de ferro (III)?
R: A fórmula do tricloreto de ferro é FeCl₃.
P: Qual é a composição percentual em massa de ferro no cloreto de ferro (III)?
R: A composição percentual em massa de ferro no tricloreto de ferro é de aproximadamente 34,8%.
P: Qual é a fórmula do cloreto de ferro (III)?
R: A fórmula do tricloreto de ferro é FeCl₃.
P: Qual é a massa molar do cloreto de ferro (III)?
R: A massa molar do tricloreto de ferro é 162,204 g/mol.
P: Como fazer cloreto de ferro (III)?
R: O tricloreto de ferro pode ser produzido pela reação do ferro com cloro gasoso ou pela dissolução do óxido de ferro em ácido clorídrico.
P: O cloreto de ferro (III) é ácido?
R: Sim, o tricloreto de ferro é ácido e pode diminuir o pH de uma solução.
P: Quais são os produtos da reação entre o zinco metálico e o cloreto de ferro (III)?
R: A reação entre o zinco metálico e o tricloreto de ferro produz cloreto de zinco e ferro metálico.
P: O cloreto de ferro (III) é tóxico?
R: O tricloreto de ferro é moderadamente tóxico para os humanos e pode causar irritação na pele e nos olhos.
P: O cloreto de ferro (III) é prejudicial ao meio ambiente?
R: O tricloreto de ferro pode ser prejudicial ao meio ambiente se liberado em grandes quantidades, pois pode contaminar fontes de água e afetar a vida aquática.
P: Como removo o cloreto de ferro (III)?
R: O tricloreto de ferro deve ser descartado adequadamente de acordo com os regulamentos locais para descarte de resíduos perigosos. Contacte as autoridades relevantes para aconselhamento.
P: Qual é a massa molar do cloreto de ferro (III)?
R: A massa molar do tricloreto de ferro é 162,204 g/mol.
