O diclorometano (CH2Cl2) ou cloreto de metileno dissolve uma ampla gama de compostos orgânicos e é comumente usado como solvente em laboratórios químicos. Também pode ser utilizado em processos de decapagem e desengorduramento.
| Nome IUPAC | Diclorometano |
| Fórmula molecular | CH2Cl2 |
| Número CAS | 75-09-2 |
| Sinônimos | Cloreto de metileno, dicloreto de metileno, DCM, Narkotil, Solaesthin, Solmetina, etc. |
| InChI | InChI=1S/CH2Cl2/c2-1-3/h1H2 |
Densidade de diclorometano g/ml
A densidade do diclorometano é 1,326 g/mL. Este valor indica a massa de diclorometano por unidade de volume a uma determinada temperatura e pressão. A densidade do diclorometano é relativamente alta, tornando-o um líquido mais denso que a água. Esta propriedade o torna útil em algumas aplicações laboratoriais, onde pode ser usado para separar substâncias de diferentes densidades.
Ponto de ebulição do diclorometano
O ponto de ebulição do diclorometano é 39,6°C (103,3°F). Esta temperatura indica o ponto em que a forma líquida do diclorometano mudará para o estado gasoso. O baixo ponto de ebulição do diclorometano torna-o um composto muito volátil que pode vaporizar facilmente à temperatura ambiente. Esta propriedade o torna útil como solvente em muitas aplicações laboratoriais, onde pode ser facilmente evaporado.
Massa molar de diclorometano
A massa molar do diclorometano, também chamado cloreto de metileno, é 84,93 g/mol. Este valor é obtido somando as massas atômicas dos átomos de uma única molécula de diclorometano. A fórmula molecular do diclorometano é CH2Cl2, o que indica que contém um átomo de carbono, dois átomos de hidrogênio e dois átomos de cloro. A massa molar é uma propriedade importante para determinar a quantidade de uma substância presente em uma determinada amostra.
Ponto de fusão do diclorometano
O ponto de fusão do CH2Cl2 é -97,4°C (-143,3°F). Esta temperatura indica o ponto em que a forma sólida do CH2Cl2 mudará para o estado líquido. No entanto, o CH2Cl2 raramente é encontrado na sua forma sólida, pois é um líquido volátil à temperatura ambiente. O baixo ponto de fusão do CH2Cl2 dificulta o congelamento e permanece líquido mesmo em baixas temperaturas.
Peso molecular do diclorometano
O peso molecular do CH2Cl2 é 84,93 g/mol. Este valor é a soma dos pesos atômicos dos átomos de uma única molécula de CH2Cl2. O peso molecular é uma propriedade importante para determinar a quantidade de uma substância presente em uma determinada amostra.
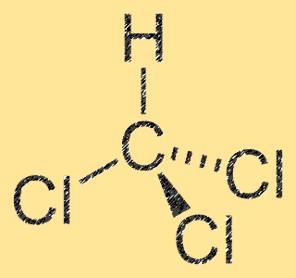
Estrutura do diclorometano
CH2Cl2 tem uma estrutura molecular tetraédrica, com um átomo de carbono central ligado a dois átomos de cloro e dois átomos de hidrogênio. A molécula possui um momento dipolar, que resulta da diferença de eletronegatividade entre os átomos de carbono e cloro. O átomo de carbono tem carga parcialmente positiva, enquanto os átomos de cloro têm carga parcialmente negativa. Esta propriedade torna o CH2Cl2 uma molécula polar.
Fórmula de diclorometano
A fórmula molecular do diclorometano é CH2Cl2. A fórmula indica que a molécula contém um átomo de carbono, dois átomos de hidrogênio e dois átomos de cloro. A fórmula também fornece informações sobre o número relativo de átomos em uma única molécula de diclorometano. A fórmula é útil para determinar a estequiometria de reações químicas envolvendo diclorometano.
| Aparência | Líquido incolor |
| Gravidade Específica | 1.326 |
| Cor | Incolor |
| Cheiro | Odor suave, semelhante ao clorofórmio |
| Massa molar | 84,93 g/mol |
| Densidade | 1.326g/mL |
| Ponto de fusão | -97,4°C (-143,3°F) |
| Ponto de ebulição | 39,6°C (103,3°F) |
| Ponto flash | -22°C (-8°F) |
| Solubilidade em Água | 16,5 g/L a 20°C (68°F) |
| Solubilidade | Miscível com muitos solventes orgânicos |
| Pressão de vapor | 44,6 kPa a 20°C (68°F) |
| Densidade do vapor | 2,93 |
| pKa | 4 |
| pH | Neutro |
Segurança e perigos do diclorometano
O diclorometano (CH2Cl2), também conhecido como cloreto de metileno, é um produto químico perigoso que apresenta riscos significativos à segurança se não for manuseado adequadamente. É altamente inflamável e pode causar incêndios ou explosões se exposto ao calor ou chamas abertas. A inalação de seus vapores pode causar irritação respiratória, dor de cabeça, tontura e até perda de consciência. O contato da pele com CH2Cl2 pode causar irritação, queimaduras ou queimaduras químicas. É também um potencial cancerígeno, com a exposição a longo prazo aumentando o risco de cancro do fígado e do pulmão. Precauções de segurança adequadas, como a utilização de equipamento de proteção individual adequado e o trabalho numa área bem ventilada, são essenciais ao trabalhar com CH2Cl2.
| Símbolos de perigo | Xn,F |
| Descrição de segurança | Líquido e vapor altamente inflamáveis. Nocivo se ingerido, inalado ou absorvido pela pele. Causa irritação na pele e irritação ocular grave. Pode causar irritação respiratória. Pode causar sonolência ou tonturas. Pode ser mortal por ingestão e penetração nas vias respiratórias. |
| Identificadores AN | ONU 1593 |
| Código SH | 29031200 |
| Classe de perigo | 3 |
| Grupo de embalagem | II |
| Toxicidade | O diclorometano é classificado como cancerígeno de categoria 2 e tem sido associado ao câncer de fígado e pulmão. Também é conhecido por causar depressão do sistema nervoso central e pode ser fatal se ingerido ou inalado em altas concentrações. Devem sempre ser tomadas precauções de segurança adequadas ao trabalhar com diclorometano. |
Métodos de síntese de diclorometano
Existem vários métodos para sintetizar diclorometano (CH2Cl2), um líquido incolor usado como solvente e decapante. Um método comum envolve a reação do gás metano com gás cloro na presença de um catalisador, geralmente cloreto de alumínio ou cloreto férrico. A reação produz CH2Cl2 e gás cloreto de hidrogênio como subprodutos. Outro método envolve a cloração do metanol com gás cloreto de hidrogênio ou cloreto de tionila. Esta reação também produz CH2Cl2 como produto, bem como água ou dióxido de enxofre como subprodutos.
Outro método envolve a reação do clorofórmio com zinco na presença de ácido clorídrico. Esta reação produz CH2Cl2 e cloreto de zinco como produtos, com gás hidrogênio como subproduto.
A cloração de vários compostos orgânicos, como etano ou propano, na presença de um catalisador pode produzir CH2Cl2 como subproduto.
Independentemente do método utilizado, é importante manusear o CH2Cl2 com cuidado devido às suas propriedades perigosas. Ao sintetizar e manusear CH2Cl2, é importante tomar precauções de segurança adequadas, como usar equipamento de proteção individual adequado e trabalhar numa área bem ventilada.
Usos do diclorometano
O diclorometano, também conhecido como cloreto de metileno, encontra muitas aplicações na indústria e na pesquisa como um solvente orgânico versátil. Desempenha um papel crucial na produção de produtos farmacêuticos e revestimentos, como tintas e vernizes. Além disso, é um agente de limpeza útil nas indústrias de fabricação de eletrônicos e metalurgia para desengorduramento.
O diclorometano dissolve e remove muitos tipos de tintas e revestimentos, tornando-o um decapante popular. Destaca-se também a sua utilização como agente de expansão na produção de espumas de poliuretano, resinas de policarbonato e outros plásticos.
Além de seus usos industriais, o diclorometano é valioso na extração de produtos naturais como óleos essenciais e perfumes de materiais vegetais. É também um solvente eficaz para muitos compostos orgânicos utilizados em reagentes de laboratório em síntese orgânica.
No entanto, o diclorometano requer um manuseamento cuidadoso devido às suas propriedades perigosas, tais como inflamabilidade e toxicidade. É importante tomar precauções de segurança adequadas, incluindo trabalhar numa área bem ventilada e usar equipamento de proteção individual adequado ao trabalhar com diclorometano.
Questões:
P: O diclorometano é polar?
R: Sim, o diclorometano é um solvente polar.
P: Quais dos seguintes riscos estão associados ao diclorometano?
R: Os perigos associados ao diclorometano incluem sua inflamabilidade, toxicidade e potencial de irritação cutânea e respiratória.
P: O diclorometano é inflamável?
R: Sim, o diclorometano é inflamável e pode causar incêndios ou explosões se exposto ao calor ou chamas abertas.
P: O diclorometano é solúvel em água?
R: Sim, o diclorometano é ligeiramente solúvel em água. No entanto, é usado principalmente como solvente para compostos apolares e não é comumente usado em soluções aquosas.
