Butanal ou butiraldeído é um composto orgânico com a fórmula C4H8O. É um líquido incolor com odor pungente e comumente utilizado como matéria-prima para a síntese de outros produtos químicos.
| Nome IUPAC | Butanal |
| Fórmula molecular | C4H8O |
| Número CAS | 123-72-8 |
| Sinônimos | Butiraldeído, aldeído butírico, butanaldeído, butiral, N-butanal, butaldeído, hidreto de butirila, 1-butanal, 1-butiraldeído |
| InChI | InChI=1S/C4H8O/c1-2-3-4-5/h4H,2-3H2,1H3 |
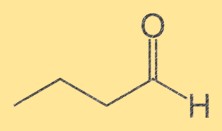
Estrutura butanal
A estrutura do Butanal consiste em uma cadeia de quatro carbonos com um grupo aldeído terminal (-CHO) anexado. Os átomos de carbono são numerados sequencialmente, com o grupo aldeído ligado ao primeiro carbono. A estrutura do Butanal é importante porque determina suas propriedades químicas e físicas.
Espectro IR do Butanal
O espectro infravermelho (IR) do Butanal é utilizado para identificar os grupos funcionais presentes na molécula. O espectro IR do Butanal mostra picos característicos para o grupo carbonila (-C=O) em aproximadamente 1730 cm-1, e para vibrações de estiramento de CH em aproximadamente 2800-3000 cm-1. O espectro IR é uma ferramenta poderosa em química orgânica para identificar e caracterizar compostos.
Massa molar do butanal
Butanal tem massa molar de 72,11 g/mol. A massa molar de um composto é a soma das massas atômicas de todos os átomos de uma molécula desse composto. No caso do Butanal, a massa molar é calculada somando as massas atômicas de quatro átomos de carbono, oito átomos de hidrogênio e um átomo de oxigênio.
Ponto de ebulição do butanal
O ponto de ebulição do Butanal é 75°C ou 167°F. Esta é a temperatura na qual a pressão de vapor do líquido se iguala à pressão atmosférica e o líquido começa a ferver. O butanal tem um ponto de ebulição relativamente baixo, o que o torna volátil e evapora facilmente à temperatura ambiente.
Ponto de fusão do butanal
O ponto de fusão do Butanal é -97°C ou -143°F. Esta é a temperatura na qual uma substância sólida passa para o estado líquido. O butanal tem um ponto de fusão muito baixo, o que significa que geralmente está no estado líquido à temperatura ambiente.
Densidade de butiraldeído g/ml
A densidade do butiraldeído é 0,81 g/mL. Densidade é a quantidade de massa por unidade de volume e geralmente é expressa em gramas por mililitro para líquidos. O butiraldeído tem densidade menor que a da água, o que significa que flutua na superfície da água.
Peso molecular do butiraldeído
O peso molecular do butiraldeído é 72,11 g/mol. É igual à massa molar e representa a massa de uma molécula de butiraldeído. O peso molecular é um parâmetro importante usado em cálculos e análises químicas.
Fórmula de Butiraldeído
A fórmula química do butiraldeído é C4H8O. Esta fórmula indica o número de átomos de cada elemento em uma molécula de butiraldeído. Existem quatro átomos de carbono, oito átomos de hidrogênio e um átomo de oxigênio no butiraldeído.
| Aparência | Líquido incolor |
| Gravidade Específica | 0,81g/ml |
| Cor | Incolor |
| Cheiro | Picante, picante |
| Massa molar | 72,11 g/mol |
| Densidade | 0,81g/ml |
| Ponto de fusão | -97°C (-143°F) |
| Ponto de ebulição | 75°C (167°F) |
| Ponto flash | -6,7°C (20°F) |
| Solubilidade em Água | Miscível |
| Solubilidade | Solúvel em etanol, éter, acetona |
| Pressão de vapor | 44 mmHg a 20°C |
| Densidade do vapor | 2,5 (ar=1) |
| pKa | 16,92 |
| pH | 4,5-6,5 |
Segurança e perigos do butanal
O butiraldeído é um líquido inflamável e pode apresentar risco de incêndio se exposto ao calor ou chamas. Também pode causar irritação nos olhos e na pele em contato, e a inalação de vapores pode causar irritação no trato respiratório. Portanto, é importante manusear o butiraldeído com cautela, utilizando equipamentos de proteção individual adequados, como luvas e óculos de proteção. Deve ser armazenado em local fresco, seco e bem ventilado, longe de fontes de calor e ignição. Se exposto ou ingerido, procure atendimento médico imediatamente. Também é importante seguir procedimentos adequados de descarte de resíduos de butiraldeído para evitar a contaminação do meio ambiente.
| Símbolos de perigo | Chama, Corrosivo, Irritante |
| Descrição de segurança | Manter afastado do calor/faísca/chama aberta/superfícies quentes. Use luvas de proteção/proteção ocular/proteção facial. SE ENTRAR EM CONTACTO COM A PELE (ou cabelo): Remova imediatamente todas as roupas contaminadas. Enxaguar a pele com água/tomar banho. Em caso de incêndio: Use pó químico seco para extinguir. |
| Números de identificação da ONU | ONU1125 |
| Código SH | 2912.19.00 |
| Classe de perigo | 3 |
| Grupo de embalagem | II |
| Toxicidade | O butanal é prejudicial se ingerido, inalado ou absorvido pela pele. Pode causar irritação nos olhos e na pele, e a exposição prolongada pode causar danos ao fígado e aos rins. Também foi demonstrado que é mutagênico e cancerígeno em estudos com animais. O manuseio e descarte adequados são importantes para evitar exposição e contaminação. |
Métodos de síntese de butanal
O butiraldeído pode ser sintetizado por vários métodos, incluindo oxidação de álcoois primários, ozonólise de alcenos e hidroformilação de alcenos.
Um método comum de síntese de butiraldeído é a oxidação de álcoois primários usando um agente oxidante como permanganato de potássio ou ácido crômico. O álcool primário é primeiro convertido no aldeído correspondente usando um agente redutor suave, como o clorocromato de piridínio, e depois oxidado em butiraldeído. Outro método envolve a ozonólise de alcenos para produzir aldeídos, que podem então ser reduzidos a butiraldeído usando um agente redutor como o borohidreto de sódio.
A hidroformilação de alcenos também é um método comumente usado para sintetizar butiraldeído. Isto envolve uma reação do alceno com monóxido de carbono e gás hidrogênio na presença de um catalisador como cobalto carbonil ou complexo de ródio. O aldeído resultante pode então ser reduzido a butiraldeído usando um agente redutor tal como hidreto de alumínio e lítio.
Outros métodos para sintetizar butiraldeído incluem a reação de reagentes de Grignard com formaldeído e a reação de cetonas com ácido fórmico e gás hidrogênio na presença de um catalisador.
No geral, a escolha do método de síntese depende de fatores como a disponibilidade de matérias-primas, o rendimento e a pureza desejados e a viabilidade das condições de reação.
Usos do butanal
O Butanal possui diversos usos industriais e comerciais devido à sua reatividade e odor distinto.
Um dos principais usos do Butanal é como matéria-prima para a produção de outros produtos químicos, como acrilato de butila e n-butanol. Esses produtos químicos são utilizados na fabricação de revestimentos, adesivos e plásticos.
O butanal também é utilizado como agente aromatizante na indústria alimentícia, proporcionando aroma frutado de maçã a diversos produtos, como assados, doces e bebidas. Também é usado como fragrância em perfumes e sabonetes.
Além disso, o Butanal é utilizado como solvente em síntese orgânica e como reagente em reações de química orgânica. Pode ser usado para converter aldeídos em álcoois secundários e para produzir ésteres por reação com ácidos carboxílicos.
O butanal também tem sido utilizado em pesquisas como ferramenta para compreender os mecanismos de ativação dos receptores olfativos no cérebro, devido ao seu forte odor.
Porém, é importante ressaltar que o Butanal pode representar riscos à segurança se não for manuseado corretamente, e devem ser tomados os devidos cuidados ao utilizá-lo e armazená-lo. No geral, a versatilidade e as propriedades únicas do Butanal o tornam um produto químico importante em diversas indústrias e áreas de pesquisa.
Questões:
Qual é a entalpia padrão de formação do butiraldeído líquido, ch3ch2ch2cho(l)?
A entalpia padrão de formação (∆H°f) de butiraldeído líquido (CH3CH2CH2CHO(l)) a 25°C é -146,6 kJ/mol.
Isto significa que a variação de entalpia associada à formação de 1 mol de butiraldeído líquido a partir dos seus elementos constituintes nos seus estados padrão (neste caso, carbono, hidrogénio e oxigénio nas suas formas elementares) é de -146,6 kJ/mol a 25°C. . e 1 atm de pressão.
O sinal negativo indica que a reação é exotérmica, o que significa que libera calor. Este valor é útil para calcular a variação de entalpia de reações envolvendo butiraldeído como reagente ou produto.
