O brometo de cobre (CuBr2) é um composto feito de cobre e bromo. Exibe uma cor azul esverdeada, frequentemente usada em síntese orgânica e como catalisador de ácido de Lewis.
| Nome IUPAC | Brometo de cobre (II) |
| Fórmula molecular | CuBr2 |
| Número CAS | 7789-45-9 |
| Sinônimos | Brometo cúprico, dibrometo de cobre |
| InChI | InChI=1S/Br2.Cu |
Propriedades do brometo de cobre
Fórmula de brometo de cobre
A fórmula do brometo cúprico é CuBr2. Representa um composto formado por um átomo de cobre e dois átomos de bromo. Essa combinação resulta em uma substância cristalina azul esverdeada, comumente usada em diversas reações químicas.
Massa molar de brometo de cobre
A massa molar do brometo cúprico é de aproximadamente 223,36 gramas por mol. Este valor é obtido somando as massas atômicas de um átomo de cobre (Cu) e dois átomos de bromo (Br) presentes na fórmula CuBr2.
Ponto de ebulição do brometo de cobre
O brometo cúprico tem um ponto de ebulição de cerca de 1.294 graus Celsius (cerca de 2.361 graus Fahrenheit). Esta temperatura indica o ponto em que a substância muda de líquido para gás sob pressão atmosférica padrão.
Ponto de fusão do brometo de cobre
O ponto de fusão do brometo cúprico é de cerca de 498 graus Celsius (cerca de 928 graus Fahrenheit). Esta temperatura representa o ponto em que a substância sólida muda para o estado líquido quando aquecida.
Densidade de brometo de cobre g/mL
A densidade do brometo cúprico é de aproximadamente 4,71 gramas por mililitro (g/mL) à temperatura ambiente e pressão atmosférica padrão. Este valor revela a quantidade de massa presente por unidade de volume da substância.
Peso molecular do brometo de cobre
O brometo cúprico tem um peso molecular de aproximadamente 223,36 gramas por mol. Este valor é crucial para diversos cálculos químicos e serve de referência para a quantidade de substância presente em uma determinada amostra.
Estrutura do brometo de cobre
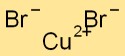
O brometo cúprico tem uma estrutura cristalina na qual os átomos de cobre são cercados por átomos de bromo e vice-versa. Este arranjo forma um padrão estável e ordenado, contribuindo para as propriedades físicas do composto.
Solubilidade do brometo de cobre
O brometo cúprico tem solubilidade limitada em água. É mais solúvel em solventes orgânicos. A solubilidade depende de fatores como temperatura e natureza do solvente utilizado. Compreender sua solubilidade é vital para diversas aplicações na química e na indústria.
| Aparência | Cristais azul esverdeados |
| Gravidade Específica | Não disponível |
| Cor | Azul verde |
| Cheiro | Inodoro |
| Massa molar | 223,36 g/mol |
| Densidade | 4,71g/ml |
| Ponto de fusão | 498°C (928°F) |
| Ponto de ebulição | 1294°C (2361°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solubilidade limitada |
| Solubilidade | Solúvel em solventes orgânicos como etanol, éter e benzeno |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Não disponível |
Segurança e perigos do brometo de cobre
O brometo cúprico apresenta certas considerações de segurança e perigo. É essencial manusear este composto com cautela devido à sua potencial toxicidade e propriedades irritantes. O contato direto com a pele ou os olhos pode causar irritação e desconforto. A inalação de poeira ou vapores pode irritar o trato respiratório. Portanto, deve-se usar equipamento de proteção individual adequado, como luvas e óculos de proteção, ao trabalhar com brometo cúprico. Além disso, deve ser armazenado longe de substâncias incompatíveis para evitar possíveis reações. Em caso de ingestão ou exposição acidental, procure imediatamente atendimento médico. O cumprimento das precauções de segurança é crucial para garantir o manuseio e uso seguros do brometo cúprico.
| Símbolos de perigo | Irritante, Corrosivo |
| Descrição de segurança | Manuseie com depósito. Evite o contato direto com a pele e os olhos. Utilize equipamento de proteção adequado. |
| Números de identificação da ONU | Não disponível |
| Código SH | Não disponível |
| Classe de perigo | Irritante |
| Grupo de embalagem | Não disponível |
| Toxicidade | Pode causar irritação na pele e nos olhos. A inalação de poeira ou vapores pode irritar o trato respiratório. |
Métodos para a síntese de brometo de cobre
Existem vários métodos para sintetizar o brometo cúprico (CuBr2). Uma abordagem comum envolve a combinação direta de cobre metálico ou óxido de cobre com ácido bromídrico . Nesse método, adicionamos cobre ao ácido, e ele sofre uma reação química, resultando na formação de brometo cúprico e na liberação de gás hidrogênio.
Outro método é a reação entre carbonato de cobre ou hidróxido de cobre com ácido bromídrico. O carbonato ou hidróxido reage com o ácido para produzir brometo cúprico, água e dióxido de carbono.
Além disso, para sintetizar o brometo cúprico, pode-se utilizar uma reação de duplo deslocamento. Este método envolve a reação entre um sal de cobre solúvel, como o sulfato de cobre, e um sal de brometo solúvel, como o brometo de sódio. A reação leva à formação de brometo cúprico e de um sal solúvel do outro metal ou metalóide presente na reação.
Além disso, para sintetizar o brometo cúprico, podemos utilizar métodos eletroquímicos. Esses métodos envolvem o uso de uma célula eletroquímica com eletrodos de cobre e uma fonte de íons brometo. Quando aplicamos uma corrente, o brometo cúprico se forma em um eletrodo, enquanto o gás bromo é liberado no outro eletrodo.
A escolha do método de síntese depende de fatores como disponibilidade de reagentes, pureza desejada e extensão da reação. O manuseio adequado e as precauções de segurança devem ser observadas durante todos os procedimentos sintéticos.
Usos do brometo de cobre
O brometo de cobre (CuBr2) encontra aplicações versáteis em diversas indústrias devido às suas propriedades únicas. Aqui estão alguns de seus usos notáveis:
- Síntese orgânica : O brometo cúprico serve como catalisador em muitas reações orgânicas, como o acoplamento de Ullmann e a reação de Wurtz-Fittig, permitindo a formação de ligações carbono-carbono e carbono-heteroátomo.
- Fotografia : É utilizado em processos fotográficos para sensibilizar emulsões e melhorar a sensibilidade de filmes e chapas, facilitando assim a captura de imagens de alta qualidade.
- Galvanoplastia : O brometo de cobre é utilizado em processos de galvanoplastia para depositar camadas de cobre nas superfícies, proporcionando resistência à corrosão e acabamentos decorativos.
- Indústria de semicondutores : No setor eletrônico é utilizado na síntese de nanocristais à base de brometo cúprico, que têm aplicações em optoeletrônica e fotônica.
- Corante de Chama : O brometo de cobre é usado em pirotecnia e fogos de artifício para produzir uma cor de chama verde, acrescentando apelo visual aos displays.
- Medicina : Embora limitada, tem sido explorada para potenciais aplicações terapêuticas devido às suas propriedades antibacterianas.
- Tecnologia Laser : Os lasers de brometo de cobre são usados em pesquisas científicas, estudos de fluorescência induzida por laser e para gerar pulsos de laser de alta energia.
- Análise química : É utilizada em química analítica para análises qualitativas e quantitativas.
- Reações de bromação : O brometo cúprico atua como agente de bromação, facilitando a adição de bromo a compostos orgânicos.
- Litografia : Em processos litográficos, compostos de brometo de cobre têm sido investigados para uso em técnicas de micro e nanofabricação.
As diversas aplicações do brometo cúprico demonstram sua importância em diversos campos, tornando-o um composto valioso em empreendimentos industriais e científicos.
Questões:
P: Qual é a massa molar do brometo de cobre (II)?
R: A massa molar do brometo cúprico (II) é de aproximadamente 223,36 g/mol.
P: Qual é a fórmula do brometo de cobre (II)?
R: A fórmula do brometo cúprico (II) é CuBr2.
P: O brometo de cobre (II) é solúvel em água?
R: O brometo cúprico (II) tem solubilidade limitada em água.
P: Para que é usado o brometo de cobre (II)?
R: O brometo de cobre (II) é usado como catalisador em síntese orgânica, fotografia, galvanoplastia e indústria de semicondutores.
P: O brometo de zinco e cobre é um substituto único?
R: Sim, o zinco e o brometo cúprico (II) sofrem uma única reação de substituição, produzindo brometo de zinco e Cu metálico.
P: Ocorre uma reação quando soluções aquosas de acetato de bário e brometo de cobre (II) são combinadas?
R: Sim, ocorre uma reação que resulta na formação de brometo de bário e acetato de cobre (II).
P: Quais íons, se houver, são formados quando o brometo de cobre (II) é adicionado à água?
R: Quando o brometo cúprico (II) é adicionado à água, ele se dissocia em íons Cu ^ 2 + e íons brometo (Br ^ -).
P: O CuBr2 forma uma ligação iônica?
R: Sim, o CuBr2 forma uma ligação iônica entre os íons cobre e bromo.
P: O CuBr2 forma uma ligação covalente?
R: Não, o CuBr2 não forma uma ligação covalente.
P: O CuBr2 é solúvel em água?
R: CuBr2 tem solubilidade limitada em água.
P: O que é CuBr2?
R: CuBr2 é a fórmula química do brometo cúprico (II), um composto cristalino azul esverdeado.
P: O CuBr2 é solúvel ou insolúvel?
R: CuBr2 é pouco solúvel em água.
P: Qual é a porcentagem em massa de cobre no CuBr2?
R: A porcentagem em massa de cobre no CuBr2 é de aproximadamente 47,5%.
