O bicarbonato de amônio é um composto cristalino branco usado na panificação como agente de saída. Ele libera dióxido de carbono quando aquecido, resultando em produtos assados leves e fofos.
| Nome IUPAC | Bicarbonato de amônio |
| Fórmula molecular | NH4HCO3 |
| Número CAS | 1066-33-7 |
| Sinônimos | Carbonato de amônio ácido; amônia de padaria; Sal de amônio de ácido carbônico (1:1); Hidrogenocarbonato de amônio |
| InChI | InChI=1S/CH2O3.H3N/c2-1(3)4;/h(H2,2,3,4);1H3 |
Observe que o valor InChI fornecido é uma representação simplificada e pode não estar completo.
Propriedades do bicarbonato de amônio
Fórmula de bicarbonato de amônio
A fórmula química do bicarbonato de amônio é NH4HCO3. Consiste em um íon amônio (NH4+) e um íon bicarbonato (HCO3-). Esta fórmula representa a composição do composto, indicando a presença de grupos amônio e bicarbonato.
Massa molar de bicarbonato de amônio
A massa molar do hidrogenocarbonato de amônio é calculada somando as massas atômicas de seus elementos constituintes. Para hidrogenocarbonato de amônio (NH4HCO3), a massa molar é de aproximadamente 79,06 gramas por mol. Este valor é importante para vários cálculos e conversões químicas.
Ponto de ebulição do bicarbonato de amônio
O hidrogenocarbonato de amônio não tem um ponto de ebulição distinto porque se decompõe em produtos gasosos quando aquecido. No entanto, o processo de decomposição começa por volta de 60 a 70 graus Celsius. À medida que a temperatura aumenta, o composto se decompõe em amônia (NH3), água (H2O) e dióxido de carbono (CO2).
Ponto de fusão do bicarbonato de amônio
O ponto de fusão do hidrogenocarbonato de amônio é de aproximadamente 41 a 60 graus Celsius. Quando aquecido, o composto sofre sublimação, passando diretamente do sólido para o gasoso sem passar pela fase líquida.
Densidade de bicarbonato de amônio g/mL
A densidade do hidrogenocarbonato de amônio é de aproximadamente 1,59 gramas por mililitro (g/mL) à temperatura ambiente. Este valor representa a massa do composto por unidade de volume. A densidade do hidrogenocarbonato de amônio afeta seu comportamento em diversas aplicações e sua solubilidade em diferentes solventes.
Peso molecular do bicarbonato de amônio
O peso molecular do hidrogenocarbonato de amônio é de aproximadamente 79,06 gramas por mol. Este valor é obtido somando as massas atômicas dos elementos presentes no composto (nitrogênio, hidrogênio, carbono e oxigênio). O peso molecular é essencial para calcular a quantidade de hidrogenocarbonato de amônio necessária para reações químicas.
Estrutura do bicarbonato de amônio
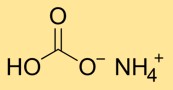
O hidrogenocarbonato de amônio tem uma estrutura cristalina composta por íons amônio (NH4+) e bicarbonato (HCO3-). O íon amônio é formado pela combinação de um átomo de nitrogênio e quatro átomos de hidrogênio, enquanto o íon bicarbonato consiste em um átomo de carbono ligado a três átomos de oxigênio.
Solubilidade do bicarbonato de amônio
O hidrogenocarbonato de amônio é muito solúvel em água. Dissolve-se facilmente em soluções aquosas, liberando íons de amônio e íons de bicarbonato. No entanto, a sua solubilidade diminui com a temperatura. É pouco solúvel em álcool e insolúvel na maioria dos solventes orgânicos.
| Aparência | Pó cristalino branco |
| Gravidade Específica | 1.586g/cm³ |
| Cor | Incolor |
| Cheiro | Cheiro de amônia |
| Massa molar | 79,06 g/mol |
| Densidade | 1,59g/ml |
| Ponto de fusão | 41-60°C |
| Ponto de ebulição | Decomposto |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solúvel |
| Solubilidade | Solúvel em água; pouco solúvel em álcool |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | Não aplicável |
| pH | ~7 |
Tenha em atenção que os valores fornecidos são aproximados e podem variar dependendo de fatores como pureza e condições ambientais.
Segurança e perigos do bicarbonato de amônio
O hidrogenocarbonato de amônio apresenta certas considerações de segurança e perigos. Pode irritar os olhos, a pele e o sistema respiratório por contato ou inalação. A exposição direta pode causar desconforto, incluindo sensações de queimação. É importante manusear o composto com cuidado e utilizar equipamentos de proteção individual adequados, como luvas e óculos de proteção. Além disso, o hidrogenocarbonato de amônio pode liberar gás amônia prejudicial quando aquecido, portanto, é necessária ventilação adequada em tais situações. O composto não é inflamável e não possui ponto de inflamação específico. O armazenamento adequado, a rotulagem e a adesão aos protocolos de segurança são essenciais para minimizar os riscos associados ao manuseio e uso do hidrogenocarbonato de amônio.
| Símbolos de perigo | Xi (irritante) |
| Descrição de segurança | – Evite contato com os olhos, pele e inalação.\n- Use equipamento de proteção individual adequado.\n- Garanta ventilação adequada durante o manuseio.\n- Armazene adequadamente e rotule os recipientes.\n – Siga os protocolos de segurança. |
| Números de identificação da ONU | Não aplicável |
| Código SH | 28369990 |
| Classe de perigo | Não classificado |
| Grupo de embalagem | Não classificado |
| Toxicidade | Baixa toxicidade; irritante para os olhos, pele e sistema respiratório. |
Observe que as informações fornecidas são de natureza geral e podem não cobrir todos os aspectos de segurança e perigos do hidrogenocarbonato de amônio. É importante consultar fichas de dados de segurança e regulamentos específicos para obter orientação completa.
Métodos para a síntese de bicarbonato de amônio
Existem vários métodos para sintetizar hidrogenocarbonato de amônio.
Um método comum envolve a reação entre amônia gasosa (NH3) e dióxido de carbono (CO2) em uma solução aquosa. Neste processo, você borbulha os dois gases diretamente na água e a água forma uma solução de hidrogenocarbonato de amônio. Então você concentra e cristaliza a solução para obter o composto sólido.
Outra abordagem é a reação entre amônia e dióxido de carbono em um solvente, como metanol ou etanol. A reação ocorre sob pressão e em alta temperatura, resultando na formação de cristais de hidrogenocarbonato de amônio.
O tratamento do carbonato de amônio com dióxido de carbono produz bicarbonato de amônio e água. O carbonato de amônio , seja na forma sólida ou em solução, reage com o dióxido de carbono para produzir bicarbonato de amônio.
Para sintetizar hidrogenocarbonato de amônio, a amônia pode ser combinada com ácido carbônico. O ácido carbônico é formado pela dissolução do dióxido de carbono em água, e a adição de amônia à solução de ácido carbônico resultante produz hidrogenocarbonato de amônio.
Certifique-se de que a síntese de hidrogenocarbonato de amônio ocorra em uma área bem ventilada devido à liberação de gás amônia durante as reações. Siga as precauções de segurança e protocolos de manuseio adequados para garantir um processo de síntese seguro e eficiente.
Usos do bicarbonato de amônio
O hidrogenocarbonato de amônio encontra vários usos em diferentes indústrias e aplicações. Aqui estão alguns de seus usos comuns:
- Panificação: O hidrogenocarbonato de amônio é usado como agente de saída na panificação, principalmente em biscoitos, bolachas e outros produtos assados. Libera dióxido de carbono quando aquecido, criando uma textura leve e crocante.
- Produção de amônia: Hidrogenocarbonato de amônio serve como composto intermediário na produção de amônia. Ele pode se decompor em amônia e dióxido de carbono, que podem então ser separados e usados para diversos fins.
- Agricultura: Os agricultores utilizam-no como fonte de nitrogênio em fertilizantes para fornecer nutrientes essenciais para o crescimento das plantas. As plantas absorvem-no facilmente graças à sua solubilidade em água.
- Controle de pH: As indústrias usam hidrogenocarbonato de amônio para ajustar os níveis de pH em processos como tratamento de água, fabricação de corantes e produção de pigmentos.
- Extintores de incêndio: Alguns extintores de pó seco usam este composto como extintor de incêndio. Ele abafa as chamas e interrompe o processo de combustão.
- Agente de limpeza: Algumas indústrias o utilizam como agente de limpeza para remover sujeira, graxa e contaminantes de superfícies.
- Indústria têxtil e de couro: Nos processos de tingimento e impressão de têxteis e artigos de couro, o hidrogenocarbonato de amônio ajuda a fixar os corantes e a melhorar a solidez da cor.
- Aplicações farmacêuticas: Encontra aplicação em certas formulações farmacêuticas como agente tamponante ou ingrediente em comprimidos medicinais.
As diversas aplicações do hidrogenocarbonato de amônio destacam sua versatilidade e utilidade em vários setores, incluindo panificação, agricultura, controle de pH, supressão de incêndio e vários processos de fabricação.
Questões:
P: O bicarbonato de amônio faz mal para você?
R: O hidrogenocarbonato de amônio pode ser prejudicial se ingerido ou inalado em grandes quantidades, causando irritação no sistema respiratório e na pele. Deve ser manuseado e usado com as devidas precauções.
P: Como separar o carbonato de amônio do bicarbonato de amônio?
R: O carbonato de amônio pode ser separado do hidrogenocarbonato de amônio aquecendo a mistura, porque o bicarbonato de amônio se decompõe em amônia, dióxido de carbono e água, deixando para trás o carbonato de amônio.
P: Como você calcula o pH do bicarbonato de amônio na água?
R: O pH do hidrogenocarbonato de amônio na água pode ser calculado usando a equação de Henderson-Hasselbalch: pH = pKa + log([A-]/[HA]), onde pKa é a constante de dissociação ácida e [A-]/[ HA] representa a razão entre a base conjugada e o ácido.
P: Como ajusto o pH do tampão de bicarbonato de amônio?
R: O pH de um tampão de hidrogenocarbonato de amônio pode ser ajustado adicionando um ácido forte para diminuir o pH ou uma base forte para aumentar o pH, mantendo a proporção apropriada de bicarbonato de amônio para sua base conjugada.
P: O bicarbonato de amônio é seguro nos alimentos?
R: O hidrogenocarbonato de amônio é geralmente reconhecido como seguro (GRAS) para uso em alimentos, mas deve ser usado de acordo com as diretrizes regulatórias e em quantidades apropriadas.
P: O que é um tampão de bicarbonato de amônio?
R: O tampão de hidrogenocarbonato de amônio é uma solução contendo hidrogenocarbonato de amônio e sua base conjugada (ou ácido), usada para manter um pH estável em diversas aplicações bioquímicas e biológicas.
P: Qual é a massa molecular do bicarbonato de amônio?
R: A massa molecular do hidrogenocarbonato de amônio é de aproximadamente 79,06 g/mol.
P: Qual é a composição percentual em massa do hidrogênio no NH4HCO3?
R: A composição percentual em massa de hidrogênio em NH4HCO3 é de aproximadamente 6,57%.
P: NH4HCO3 é um ácido ou uma base?
R: NH4HCO3 pode atuar tanto como ácido quanto como base, dependendo do contexto. Ele pode doar um próton (H+) para atuar como ácido ou aceitar um próton para atuar como base.
P: Qual é o nome do composto com a fórmula NH4HCO3?
R: O composto com a fórmula NH4HCO3 é denominado hidrogenocarbonato de amônio.
P: O NH4HCO3 é iônico ou covalente?
R: NH4HCO3 é considerado um composto iônico devido à presença do íon amônio (NH4+) e do íon hidrogenocarbonato (HCO3-) em sua estrutura.
