Azida de sódio (NaN3) é um composto químico. É altamente tóxico e explosivo. É usado em airbags para gerar rapidamente gás nitrogênio para inflar no momento do impacto.
| Nome IUPAC | Azida de sódio |
| Fórmula molecular | NaN3 |
| Número CAS | 26628-22-8 |
| Sinônimos | Azium, sal de sódio do ácido hidrazóico, trinitreto de sódio |
| InChI | InChI=1S/3HNO.Na/c1-4-2;2-1-3;/h3*1H;/q;;;+1/p-1 |
Propriedades da azida de sódio
Fórmula de Azida de Sódio
A fórmula da azida de sódio é NaN3. Consiste em um átomo de sódio (Na) e três átomos de nitrogênio (N). O átomo de sódio tem carga positiva, enquanto os átomos de nitrogênio têm carga negativa. A fórmula representa a proporção de átomos de sódio e nitrogênio no composto.
Massa molar de Azida de Sódio
A massa molar da azida sódica é calculada somando as massas atômicas de seus constituintes. O sódio tem massa molar de 22,99 g/mol e o nitrogênio tem massa molar de 14,01 g/mol. Como existem três átomos de nitrogênio na azida de sódio, multiplicamos a massa molar do nitrogênio por três. A adição desses valores dá uma massa molar de aproximadamente 65,01 g/mol para a azida sódica.
Ponto de ebulição da azida de sódio
A azida de sódio tem um ponto de ebulição elevado. Quando aquecido, sofre decomposição em vez de ferver. Em temperaturas acima de 275 graus Celsius (527 graus Fahrenheit), ele se decompõe rapidamente em sódio metálico e gás nitrogênio. Seu ponto de ebulição não está, portanto, bem definido.
Azida de sódio Ponto de fusão
O ponto de fusão da azida de sódio é relativamente baixo em comparação com o seu ponto de ebulição. Ele derrete a cerca de 275 graus Celsius (527 graus Fahrenheit). O composto muda de sólido para líquido nesta temperatura. No entanto, é importante manusear a azida sódica com cautela devido à sua natureza tóxica e explosiva.
Densidade de azida de sódio g/mL
A densidade da azida sódica é geralmente expressa em gramas por mililitro (g/mL). A densidade aproximada da azida de sódio sólida é de aproximadamente 1,85 g/mL. No entanto, deve-se notar que a densidade pode variar ligeiramente dependendo de fatores como temperatura e pressão.
Peso Molecular da Azida de Sódio
O peso molecular da azida de sódio é a soma das massas atômicas de seus elementos constituintes. Conforme mencionado anteriormente, a azida de sódio consiste em um átomo de sódio e três átomos de nitrogênio. A adição das massas atômicas desses elementos dá um peso molecular de aproximadamente 65,01 gramas por mol (g/mol).
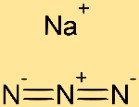
Estrutura da azida de sódio
A estrutura da azida de sódio consiste em cátions de sódio (Na+) e ânions azida (N3-) alternados. O íon sódio é cercado por três átomos de nitrogênio, cada um compartilhando um par de elétrons com o átomo de sódio. Este arranjo cria uma estrutura cristalina estável para a azida de sódio.
Solubilidade da azida de sódio
A sodiumazida é moderadamente solúvel em água. Dissolve-se em água para formar uma solução límpida. A solubilidade da azida de sódio aumenta com temperaturas mais elevadas. No entanto, é importante manusear a solução com cuidado devido à natureza tóxica e explosiva da azida sódica.
| Aparência | Sólido branco |
| Gravidade Específica | 1,85g/ml |
| Cor | Incolor |
| Cheiro | Inodoro |
| Massa molar | 65,01 g/mol |
| Densidade | 1,85g/ml |
| Ponto de fusão | 275ºC |
| Ponto de ebulição | Decomposto |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Moderadamente solúvel |
| Solubilidade | Solúvel em solventes polares como amônia |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | Não aplicável |
| pH | Neutro |
Segurança e perigos da azida sódica
A sodiumazida apresenta riscos de segurança significativos e deve ser manuseada com extremo cuidado. É altamente tóxico se ingerido, inalado ou absorvido pela pele. A exposição à azida sódica pode causar sérios riscos à saúde, incluindo problemas respiratórios, tonturas e até morte. Também representa um risco potencial de explosão, especialmente se exposto a calor, choque ou contato com certos metais. Ao trabalhar com azida sódica, as pessoas devem usar equipamento de proteção individual adequado, incluindo luvas e óculos de segurança. É fundamental armazenar e manusear este composto em áreas bem ventiladas, longe de fontes de ignição e substâncias incompatíveis para minimizar o risco de acidentes e garantir a segurança no local de trabalho.
| Símbolos de perigo | Tóxico, Explosivo |
| Descrição de segurança | Manuseie com extremo cuidado. Substância tóxica e explosiva. |
| Números de identificação da ONU | UN1687 (para azida sódica, sólidos tóxicos, inorgânicos, nos) |
| Código SH | 28500090 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | II (substância moderadamente perigosa) |
| Toxicidade | Muito tóxico |
Métodos para a síntese de azida de sódio
Existem alguns métodos comuns para sintetizar azida de sódio.
Um método envolve a reação entre amida de sódio (NaNH2) e ácido hidrazóico (HN3). Neste método, dissolva a amida de sódio em amônia líquida e adicione lentamente o ácido hidrazóico. A reação ocorre, resultando na formação de azida de sódio e cloreto de amônio como subprodutos.
Outro método de síntese envolve a reação entre nitrito de sódio (NaNO2) e azida de sódio (NaN3). Numa solução aquosa, a reacção controla cuidadosamente a adição de nitrito de sódio a uma solução de azida de sódio, conduzindo à formação de azida de sódio e nitrato de sódio.
Para sintetizar azida de sódio, o cianeto de sódio (NaCN) pode reagir com óxido nitroso (N2O) em alta temperatura. Durante esta reação, azida de sódio e cianato de sódio são formados como subprodutos.
Siga sempre as precauções de segurança adequadas para minimizar os riscos associados ao processo de síntese. Isso inclui o uso de equipamentos de proteção individual e o cumprimento dos protocolos de manuseio.
Usos da azida de sódio
A sodiumazida tem vários usos importantes em diversas indústrias. Aqui estão alguns aplicativos notáveis:
- Insuflação do airbag: A sodiumazida é um componente chave dos airbags dos automóveis. Durante uma colisão, uma pequena quantidade de azida de sódio reage rapidamente para gerar gás nitrogênio, inflando o airbag e protegendo os passageiros.
- Pesquisa bioquímica: Os pesquisadores usam azida sódica para inibir enzimas, como a citocromo oxidase, facilitando o estudo dos processos celulares e das vias metabólicas.
- Preservação de amostras biológicas: A sodiumazida preserva amostras biológicas, como anticorpos, prevenindo o crescimento bacteriano e mantendo a sua estabilidade.
- Iniciação Explosiva: A azida de sódio serve como explosivo primário em alguns dispositivos pirotécnicos, detonadores e iniciadores explosivos devido à sua natureza explosiva.
- Síntese química: A sódiozida atua como precursor em diversas reações químicas, possibilitando a síntese de compostos orgânicos, fármacos e corantes.
- Prevenção de corrosão: As indústrias usam azida de sódio como inibidor de corrosão para proteger as superfícies metálicas da degradação causada pela oxidação ou exposição a agentes corrosivos.
- Indústria de mineração: A azida de sódio ajuda a separar minerais valiosos de substâncias indesejadas nas operações de mineração como um depressor nos processos de flotação mineral.
- Indústria de Polímeros: A azida de sódio atua como agente de expansão na produção de espumas de poliuretano, facilitando a formação de bolhas de gás que conferem à espuma a estrutura desejada.
- Química Analítica: A azida de sódio serve como reagente para várias análises químicas, incluindo espectrofotometria, cromatografia gasosa e espectrometria de massa.
- Medicina Veterinária: Os veterinários usam azida de sódio como agente de eutanásia para animais em alguns casos na prática veterinária.
Estas aplicações destacam as diversas utilidades da azida sódica, mas é crucial manusear este composto com cuidado e seguir os protocolos de segurança devido à sua natureza tóxica e explosiva.
Questões
P: Como testar a azida de sódio?
R: A azida de sódio pode ser testada usando técnicas analíticas apropriadas, como espectroscopia, cromatografia ou testes de reatividade química.
P: A azida sódica ainda é usada em airbags?
R: Sim, a azida sódica ainda é usada em airbags como propulsor para inflar rapidamente após o impacto.
P: Quantos gramas de azida de sódio são necessários para produzir 30,5 g de nitrogênio?
R: São necessários aproximadamente 34 gramas de azida de sódio para produzir 30,5 gramas de gás nitrogênio.
P: Onde comprar azida de sódio?
R: A sodiumazida pode ser adquirida de fornecedores de produtos químicos, fornecedores de laboratórios ou mercados de produtos químicos online.
P: Como preparo uma solução de azida de sódio a 0,01% em PBS?
R: Para preparar uma solução de azida de sódio a 0,01% em PBS, dissolva 0,01 gramas de azida de sódio em 100 ml de solução salina tamponada com fosfato (PBS).
P: Qual é o papel da azida de sódio nos experimentos?
R: A sodiumazida é comumente usada como inibidor ou conservante em experimentos destinados a inibir a atividade enzimática ou prevenir o crescimento bacteriano.
P: Como faço para eliminar a azida de sódio de uma amostra?
R: A sodiumazida pode ser eliminada de uma amostra por meio de lavagem ou enxágue completo com solventes apropriados ou submetendo-a à decomposição em alta temperatura.
P: Como a azida sódica afeta a ETC?
R: A sodiumazida inibe a cadeia de transporte de elétrons (ETC) nas mitocôndrias, bloqueando a enzima citocromo oxidase, interrompendo assim o fluxo de elétrons e a produção de ATP.
P: Quantos gramas de sódio são formados quando 93 gramas de azida de sódio reagem?
R: 35,9 gramas de sódio são formados quando 93 gramas de azida de sódio reagem.
P: A decomposição explosiva da azida sódica é uma mudança física no acionamento do airbag?
R: Não, a decomposição explosiva da azida de sódio para inflar o airbag de um automóvel é uma alteração química.
P: Como preparar azida de sódio?
R: A sodiumazida é geralmente preparada por métodos de síntese química envolvendo reações entre precursores adequados, como amida de sódio e ácido hidrazóico.
P: Qual a quantidade de azida de sódio que é tóxica?
R: A sodiumazida é altamente tóxica e mesmo pequenas quantidades, como alguns gramas, podem representar riscos significativos à saúde se ingeridas, inaladas ou absorvidas pela pele.
P: Para que é usada a azida de sódio?
R: A sodiumazida é usada em uma variedade de aplicações, incluindo inflação de airbag, pesquisa bioquímica, síntese química e como conservante ou inibidor em amostras biológicas.
P: A azida de sódio reage com ácidos?
R: Sim, a azida de sódio pode reagir com ácidos, como o ácido clorídrico (HCl), formando gases tóxicos como a azida de hidrogênio (HN3). Devem ser tomadas precauções apropriadas ao manusear azida sódica e ácidos.
