O ácido maleico é um composto orgânico com a fórmula C4H4O4. É um sólido cristalino branco utilizado na produção de polímeros, adesivos e aditivos alimentares.
| Nome IUPAC | Ácido 2,3-dihidroxibutanodióico |
| Fórmula molecular | C₄H₄O₄ |
| Número CAS | 110-16-7 |
| Sinônimos | Ácido cis-butenodióico, ácido cis-1,2-etilenodicarboxílico, ácido tóxico |
| InChI | InChI=1S/C4H4O4/c5-3(6)1-2-4(7)8/h1-2H,(H,5,6)(H,7,8) |
Propriedades do ácido maleico
Fórmula de ácido maleico
A fórmula do ácido butenodióico é C4H4O4. Consiste em quatro átomos de carbono, quatro átomos de hidrogênio e quatro átomos de oxigênio. A fórmula representa o número exato e os tipos de átomos presentes em uma molécula de ácido butenodióico.
Massa molar de ácido maleico
A massa molar do ácido butenodióico é calculada somando as massas atômicas de todos os átomos de sua fórmula. O ácido butenodióico tem uma massa molar de aproximadamente 116,07 gramas por mol. Este valor permite determinar a quantidade de ácido butenodióico em uma determinada quantidade, utilizando o conceito de moles.
Ponto de ebulição do ácido maleico
O ácido butenodióico tem um ponto de ebulição em torno de 160 a 162 graus Celsius. Esta temperatura indica o ponto em que o ácido butenodióico muda do estado líquido para o gasoso sob pressão atmosférica padrão.
Ponto de fusão do ácido maleico
O ponto de fusão do ácido butenodióico é de aproximadamente 139 a 140 graus Celsius. Isso significa a temperatura na qual o ácido butenodióico muda da forma sólida para a forma líquida. Esta característica pode ser útil em diversas aplicações e processos envolvendo ácido butenodióico.
Densidade de ácido maleico g/mL
O ácido butenodióico tem uma densidade de aproximadamente 1,59 gramas por mililitro. A densidade mede a massa de uma substância por unidade de volume. A densidade do ácido butenodióico determina seu comportamento em diferentes processos físicos e químicos, como mistura com outras substâncias ou separação delas.
Peso molecular do ácido maleico
O peso molecular do ácido butenodióico é 116,07 gramas por mol. É a soma dos pesos atômicos de todos os átomos de uma molécula de ácido butenodióico. O peso molecular é essencial em vários cálculos, como na determinação da concentração ou quantidade de ácido butenodióico em uma solução.
Estrutura do ácido maleico
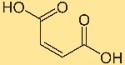
O ácido butenodióico tem uma estrutura que consiste em dois grupos carboxila (COOH) ligados a uma estrutura de ligação dupla carbono-carbono (C = C). Este arranjo confere ao ácido butenodióico suas propriedades e reatividade características. A estrutura desempenha um papel crucial na compreensão do seu comportamento em reações químicas e interações com outros compostos.
Solubilidade do ácido maleico
O ácido butenodióico é muito solúvel em água, com solubilidade de aproximadamente 633 gramas por litro a 20 graus Celsius. Essa alta solubilidade torna o ácido butenodióico facilmente solúvel em soluções aquosas e permite seu uso em diversas aplicações, como na produção de polímeros e produtos farmacêuticos.
| Aparência | Sólido cristalino branco |
| Gravidade Específica | 1,59g/ml |
| Cor | Incolor |
| Cheiro | Inodoro |
| Massa molar | 116,07 g/mol |
| Densidade | 1,59g/ml |
| Ponto de fusão | 139-140°C |
| Ponto de ebulição | 160-162°C |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | É altamente solúvel em solventes polares, como água e álcool. |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | 1,92 |
| pH | ~1-2 |
Segurança e perigos do ácido maleico
O ácido butenodióico tem certas considerações de segurança e perigos. Pode causar irritação na pele, olhos e sistema respiratório por contato ou inalação. É aconselhável usar equipamentos de proteção, como luvas e óculos de proteção, ao manusear o ácido butenodióico. Em caso de ingestão acidental, deve-se procurar atendimento médico imediato. O ácido butenodióico também é combustível e deve-se tomar cuidado para evitar a exposição a chamas abertas ou altas temperaturas. Uma boa ventilação é crucial para evitar a acumulação de vapores. É importante armazenar o ácido butenodióico em uma área segura e bem ventilada, longe de substâncias incompatíveis. Seguir práticas de segurança adequadas é essencial ao trabalhar com ácido butenodióico.
| Símbolos de perigo | Corrosivo (C) |
| Descrição de segurança | – Evite o contato com a pele e os olhos, – Use em uma área bem ventilada, – Use luvas e óculos de proteção, – Armazene em uma área segura e bem ventilada |
| Identificadores das Nações Unidas | UN3265 |
| Código SH | 2917.11.00 |
| Classe de perigo | 8 (Corrosivo) |
| Grupo de embalagem | III |
| Toxicidade | Pode causar irritação na pele, olhos e sistema respiratório. Perigoso se ingerido. |
Métodos de síntese de ácido
Vários métodos permitem a síntese do ácido butenodióico. Uma abordagem popular é oxidar o anidrido maleico com um agente oxidante, tal como permanganato de potássio ou peróxido de hidrogênio, na presença de um catalisador. A reação dá ácido butenodióico como produto.
Outro método é hidrolisar o anidrido maleico fazendo-o reagir com água, resultando na formação de ácido butenodióico. Dependendo das condições desejadas e da taxa de reação, esta reação pode ocorrer sob condições ácidas ou alcalinas.
A oxidação catalítica do butano ou do benzeno produz ácido butenodióico, oxidando-os com ar ou oxigênio usando um catalisador como o pentóxido de vanádio. A mistura de reação resultante passa por etapas adicionais de purificação para isolar o ácido butenodióico.
Além disso, os microrganismos podem fermentar carboidratos específicos para sintetizar o ácido butenodióico. Este método biológico envolve o uso de bactérias ou fungos específicos que produzem ácido butenodióico como subproduto metabólico.
Cada um desses métodos de síntese tem vantagens e considerações relativas às condições de reação, escalabilidade e impacto ambiental. A escolha do método depende de fatores como rendimento desejado, requisitos de pureza e viabilidade geral do processo.
Usos do ácido maleico
O ácido butenodióico encontra diversas aplicações devido às suas propriedades versáteis. Aqui estão alguns de seus usos:
- Produção de polímeros: A produção de polímeros, como poliésteres e resinas alquídicas, utiliza o ácido butenodióico como precursor, conferindo a esses materiais propriedades desejáveis como durabilidade e flexibilidade.
- Formulação adesiva: As formulações adesivas contêm ácido butenodióico para melhorar a sua capacidade de ligação, promovendo assim a adesão entre diferentes substratos. Isso o torna útil em setores como construção e automotivo.
- Indústria de Alimentos e Bebidas: Na indústria de alimentos e bebidas, o ácido butenodióico atua como acidulante e intensificador de sabor, adicionando sabor amargo a diversos produtos, como doces, refrigerantes e sucos de frutas.
- Indústria Têxtil: A indústria têxtil utiliza ácido butenodióico em processos de tingimento e acabamento, onde atua como agente nivelador de corante, garantindo distribuição uniforme da cor nos tecidos.
- Aplicações farmacêuticas: O ácido butenodióico encontra aplicações na indústria farmacêutica para a síntese de princípios farmacêuticos ativos (API) e como ajustador de pH em formulações de medicamentos.
- Tratamento de Água: O ácido butenodióico controla incrustações e corrosão em processos de tratamento de água, evitando a formação de depósitos minerais em tubulações e equipamentos.
- Cosméticos e produtos de higiene pessoal: O ácido butenodióico regula o pH e atua como agente quelante em cosméticos e produtos de higiene pessoal, estabilizando formulações e melhorando sua eficácia.
- Aplicações agrícolas: Os derivados do ácido butenodióico funcionam como reguladores do crescimento das plantas e herbicidas na agricultura, ajudando a controlar o crescimento de ervas daninhas e a melhorar o rendimento das colheitas.
A diversificada gama de aplicações do ácido butenodióico destaca sua importância em diversas indústrias, contribuindo para o desenvolvimento de inúmeros produtos e processos.
Questões:
P: Quantos átomos de H ionizáveis existem em cada molécula de ácido maleico, C4H4O4?
R: Existem dois átomos de H ionizáveis em cada molécula de ácido butenodióico.
P: O ácido maleico tem um momento dipolar?
R: Sim, o ácido butenodióico tem um momento dipolar devido à presença de ligações polares em sua estrutura.
P: Quais são as fórmulas moleculares do glioxil, ácido maleico e ácido acônico?
R: As fórmulas moleculares são: glioxil (C2H2O2), ácido butenodióico (C4H4O4), ácido acôntico (C6H6O6).
P: O ácido maleico ou o ácido fumárico são mais reativos com o bromo?
R: O ácido butenodióico é mais reativo com o bromo do que o ácido fumárico.
P: Ocorreria a isomerização do ácido maleico se a reação fosse realizada em água neutra?
R: Não, a isomerização do ácido butenodióico não ocorreria em água neutra.
P: Quão próximos estavam seus valores de pKa1 e pKa2 para o ácido maleico?
R: O valor pKa1 do ácido butenodióico é aproximadamente 1,92, enquanto o valor pKa2 é aproximadamente 6,07.
P: Como dissolver o ácido maleico?
R: O ácido butenodióico pode ser dissolvido em água agitando-o em temperatura ambiente até que se dissolva completamente.
P: Quando o ácido maleico foi encontrado?
R: O ácido butenodióico foi descoberto em 1834 pelo químico alemão August Wilhelm von Hofmann.
P: Como o etanol reage com o ácido málico para formar o ácido maleico?
R: O etanol reage com o ácido málico na presença de um agente desidratante, como o ácido sulfúrico, para formar o ácido butenodióico.
P: O ácido maleico, quando misturado com HCl e aquecido, forma ácido fumárico?
R: Sim, o ácido butenodióico, quando misturado com HCl e aquecido, sofre uma reação de isomerização para formar ácido fumárico.
