O cianeto de hidrogênio é um composto altamente tóxico utilizado nas indústrias, conhecido por seus efeitos mortais no sistema respiratório. É incolor, tem odor distinto e apresenta riscos significativos à saúde humana.
| Nome IUPAC | Cianeto de hidrogenio |
| Fórmula molecular | HCN |
| Número CAS | 74-90-8 |
| Sinônimos | Ácido Prússico, Formonitrila, Ácido Hidrociânico, Ácido Hidrociânico |
| InChI | InChI=1S/CHN/c1-2/h1H |
Propriedades do cianeto de hidrogênio
Fórmula de cianeto de hidrogênio
A fórmula do ácido cianídrico é HCN. Consiste em um átomo de hidrogênio (H) ligado a um átomo de carbono (C) por meio de uma ligação tripla, e o átomo de carbono está ainda ligado a um átomo de nitrogênio (N). Esta fórmula molecular simples representa a composição do ácido cianídrico.
Massa molar de cianeto de hidrogênio
A massa molar do ácido cianídrico é de aproximadamente 27,03 gramas por mol. É calculado somando as massas atômicas de hidrogênio (H), carbono (C) e nitrogênio (N) presentes em uma molécula de ácido cianídrico.
Ponto de ebulição do cianeto de hidrogênio
O cianeto de hidrogênio tem um ponto de ebulição de cerca de 25,7 graus Celsius (78,3 graus Fahrenheit). Nessa temperatura, o ácido cianídrico passa do estado líquido para o gasoso, emitindo vapores tóxicos.
Ponto de fusão do cianeto de hidrogênio
O ponto de fusão do ácido cianídrico é de aproximadamente -13,4 graus Celsius (7,9 graus Fahrenheit). A esta temperatura, o ácido cianídrico muda do estado sólido para o estado líquido.
Densidade de cianeto de hidrogênio g/mL
A densidade do ácido cianídrico é de aproximadamente 0,687 gramas por mililitro. Este valor de densidade representa a massa de ácido cianídrico por unidade de volume.
Peso molecular do cianeto de hidrogênio
O peso molecular do ácido cianídrico é de aproximadamente 27,03 gramas por mol. É determinado somando os pesos atômicos de seus elementos constituintes.
Estrutura do cianeto de hidrogênio
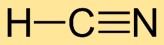
O cianeto de hidrogênio tem uma estrutura molecular linear, com o átomo de hidrogênio (H) ligado ao átomo de carbono (C) e o átomo de carbono (C) ligado ao átomo de nitrogênio (N). A ligação tripla entre carbono e nitrogênio dá estabilidade à molécula.
Solubilidade do cianeto de hidrogênio
O ácido cianídrico é muito solúvel em água. Dissolve-se facilmente em água, formando uma solução incolor. Essa solubilidade permite que o ácido cianídrico se misture e interaja facilmente com outras substâncias em diversas aplicações e ambientes.
| Aparência | Gás incolor |
| Gravidade Específica | 0,687 |
| Cor | Incolor |
| Cheiro | Cheiro distinto |
| Massa molar | 27,03 g/mol |
| Densidade | 0,687g/ml |
| Ponto de fusão | -13,4°C (-7,9°F) |
| Ponto de ebulição | 25,7°C (78,3°F) |
| Ponto flash | -17,8°C (0°F) |
| Solubilidade em Água | Miscível com água |
| Solubilidade | Solúvel em solventes orgânicos como éter e álcool etílico |
| Pressão de vapor | 500 mmHg a 20°C |
| Densidade do vapor | 0,95 |
| pKa | 9.3 |
| pH | 5.6 (ácido cianídrico diluído) |
Segurança e perigos do cianeto de hidrogênio
O cianeto de hidrogênio apresenta riscos significativos à segurança e deve ser manuseado com extremo cuidado. É altamente tóxico quando inalado, ingerido ou absorvido pela pele. A exposição ao ácido cianídrico pode causar dificuldade respiratória grave, parada cardíaca e até morte. É importante garantir ventilação adequada e usar equipamento de proteção individual ao trabalhar com ou próximo ao ácido cianídrico. Além disso, o composto é inflamável e pode formar misturas explosivas com o ar. O armazenamento deve ser realizado em recipientes bem fechados, longe de fontes de ignição. Protocolos de emergência, como a prestação de cuidados médicos imediatos e a evacuação das áreas afetadas, devem ser implementados para mitigar os riscos associados à exposição ao ácido cianídrico.
| Símbolos de perigo | Caveira e ossos cruzados |
| Descrição de segurança | Muito tóxico; manuseie com extremo cuidado |
| Números de identificação da ONU | UN1051 (ácido cianídrico) |
| Código SH | 2811.11.00 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | Eu (grande perigo) |
| Toxicidade | Extremamente tóxico; pode ser fatal mesmo em pequenas quantidades |
Métodos de síntese de cianeto de hidrogênio
Vários métodos podem sintetizar ácido cianídrico.
Um método comum é o processo Andrussow. Neste processo, os catalisadores de platina ou ródio facilitam a reação da amônia (NH₃) e do metano (CH₄) com o oxigênio (O₂) para sintetizar o ácido cianídrico. A reação ocorre em altas temperaturas, geralmente em torno de 1000 a 1200°C. O metano atua como agente redutor, convertendo oxigênio em água (H₂O), enquanto a amônia fornece a fonte de nitrogênio. A mistura resultante sofre uma série de reações que levam à formação de ácido cianídrico (HCN) e vapor d’água.
Outro método de síntese de ácido cianídrico é o processo BMA. Isto envolve a reação do metano (CH₄) com amônia (NH₃) na presença de um catalisador, como cobre ou níquel, em alta temperatura. Este processo gera ácido cianídrico e outros subprodutos.
O processo Andrussov-Noddack produz ácido cianídrico pela reação do cianeto de sódio (NaCN) com um ácido forte, como o ácido sulfúrico (H₂SO₄).
Vale ressaltar que o ácido cianídrico é um composto altamente tóxico e sua síntese deve ser realizada com muito cuidado em instalações bem equipadas, seguindo protocolos de segurança adequados. A utilização de equipamentos especializados, ventilação adequada e cumprimento das instruções de segurança são essenciais para garantir o bem-estar do pessoal envolvido no processo de síntese.
Usos do cianeto de hidrogênio
O cianeto de hidrogênio encontra aplicações em diversas indústrias devido às suas propriedades únicas. Aqui estão alguns de seus usos:
- Fabricação química: O ácido cianídrico desempenha um papel crucial na síntese de vários produtos químicos importantes, incluindo adiponitrila (um componente chave na produção de náilon), metacrilato de metila (usado em plásticos acrílicos) e cianeto de sódio (usado na mineração de ouro).
- Produtos farmacêuticos: A produção de produtos farmacêuticos, como vitaminas, aminoácidos sintéticos e alguns antibióticos, depende do ácido cianídrico.
- Fumigação: As indústrias usam ácido cianídrico como fumigante para controlar pragas, especialmente em espaços fechados como estufas, porões de navios e instalações de armazenamento de grãos.
- Chapeamento de metal: As indústrias metalúrgicas usam ácido cianídrico em processos de galvanoplastia para fornecer uma camada protetora nas superfícies metálicas.
- Fabricação de polímeros: O cianeto de hidrogênio participa ativamente da produção de fibras sintéticas, borracha e resinas.
- Inseticidas: Alguns inseticidas contêm ingredientes ativos derivados do ácido cianídrico para fornecer controle eficaz de pragas na agricultura e na silvicultura.
- Reagente de Laboratório: O cianeto de hidrogênio serve como reagente em diversas reações químicas e procedimentos laboratoriais.
- Mineração: Na mineração de ouro e prata, o ácido cianídrico atua como reagente químico para extrair metais preciosos dos minérios.
- Produção de borracha sintética: O cianeto de hidrogênio serve como matéria-prima na produção de borracha sintética, como a borracha de estireno-butadieno (SBR).
- Corantes e pigmentos: A fabricação de corantes e pigmentos envolve a utilização de ácido cianídrico, contribuindo para suas propriedades corantes.
Embora o ácido cianídrico tenha suas utilizações, é importante manuseá-lo com muito cuidado devido à sua alta toxicidade. Protocolos de segurança rígidos e procedimentos de manuseio adequados são essenciais para minimizar os riscos associados ao seu uso.
Questões:
P: Para que é usado o cianeto de hidrogênio?
R: O cianeto de hidrogênio é usado na fabricação de produtos químicos, produção farmacêutica, fumigação, revestimento de metais, inseticidas e como reagente de laboratório, entre outras aplicações.
P: Qual é a fórmula química do cianeto de hidrogênio?
R: A fórmula química do ácido cianídrico é HCN.
P: Quais são os “usos permitidos” do cianeto de hidrogênio?
R: Os “fins permitidos” do HCN incluem seu uso aprovado e regulamentado em processos industriais específicos, pesquisas e outras aplicações permitidas.
P: Em que é encontrado o cianeto de hidrogênio?
R: O cianeto de hidrogênio pode ser encontrado em vários produtos químicos, ambientes industriais e fontes naturais, como certas plantas e sementes.
P: Onde você pode comprar cianeto de hidrogênio?
R: A compra de cianeto de hidrogênio é altamente restrita e regulamentada devido à sua toxicidade e potencial uso indevido.
P: O que é cianeto de hidrogênio?
R: O cianeto de hidrogênio é um composto altamente tóxico e volátil com odor distinto, comumente usado em processos industriais.
P: O cianeto de hidrogênio é polar ou apolar?
R: O cianeto de hidrogênio é uma molécula polar devido à presença de ligações polares e uma distribuição assimétrica de densidade eletrônica.
P: Qual palavra ou frase de duas palavras descreve melhor a forma da molécula de cianeto de hidrogênio (HCN)?
R: A forma da molécula de HCN é linear.
P: Para que é usado o cianeto de hidrogênio?
R: O cianeto de hidrogênio é usado em diversas indústrias para síntese química, fumigação, revestimento de metal, inseticidas e produção farmacêutica.
P: O cianeto de hidrogênio foi usado em um ataque terrorista?
R: Sim, o HCN foi utilizado no passado como arma química em ataques terroristas.
P: Quais são os outros nomes químicos associados ao cianeto de hidrogênio?
R: Outros nomes químicos associados ao HCN incluem ácido prússico, formonitrila, ácido cianídrico e ácido cianídrico.
P: Qual é o diagrama de pontos de Lewis correto para o cianeto de hidrogênio?
R: O diagrama de pontos de Lewis correto para HCN inclui o átomo de hidrogênio (H) ligado ao átomo de carbono (C) por meio de uma ligação simples, e o átomo de carbono (C) ligado ao átomo de nitrogênio (N) por uma ligação tripla.
P: Qual é a carga dos átomos de cianeto de hidrogênio?
R: No HCN, o átomo de hidrogênio (H) tem carga parcial positiva, o átomo de carbono (C) tem carga parcial negativa e o átomo de nitrogênio (N) tem carga parcial negativa.
P: O que uma cápsula de cianeto de hidrogênio faz com você?
R: Em ambientes altamente regulamentados e controlados, uma cápsula de HCN pode ser usada como um meio rápido e letal de autoadministração, geralmente para fins secretos ou de emergência.
P: Que tipo de ligação é a ligação carbono-nitrogênio em uma molécula de cianeto de hidrogênio (HCN)?
R: A ligação carbono-nitrogênio em uma molécula de HCN é uma ligação tripla.
