O acetato de magnésio (Mg(C2H3O2)2) é um composto composto por íons Mg2+ e C2H3O2-. É comumente usado como agente secante em síntese orgânica e como aditivo alimentar.
| Nome IUPAC | Acetato de magnésio |
| Fórmula molecular | Mg(C2H3O2)2 |
| Número CAS | 142-72-3 |
| Sinônimos | Diacetato de magnésio, sal de magnésio de ácido acético, etanoato de magnésio, CAS 73567-85-6, EINECS 240-882-6, UNII-RS92S4G29A |
| InChI | InChI=1S/2C2H4O2.Mg/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
Propriedades do acetato de magnésio
Fórmula de acetato de magnésio
A fórmula química do acetato de magnésio é Mg(C2H3O2)2. Esta fórmula representa a composição do composto, com um íon Mg2+ e dois C2H3O2-. A fórmula é importante para determinar a quantidade de composto necessária para uma reação específica. Também é útil para identificar o composto em diferentes contextos.
Massa molar de acetato de magnésio
A massa molar de Mg(C2H3O2)2 é 142,39 g/mol. Este valor é obtido somando as massas atômicas dos íons Mg2+ (24,31 g/mol) e C2H3O2- (58,08 g/mol). A massa molar é uma propriedade importante na determinação da quantidade de Mg(C2H3O2)2 necessária para uma reação específica.
Ponto de ebulição do acetato de magnésio
Mg(C2H3O2)2 tem um ponto de ebulição relativamente alto de 117,5°C (243,5°F). Esta propriedade se deve à natureza iônica do composto e à forte atração eletrostática entre os íons magnésio e acetato. A esta temperatura, o composto começará a vaporizar, mas permanecerá no estado líquido, a menos que seja submetido a temperaturas mais elevadas.
Ponto de fusão de acetato de magnésio
O ponto de fusão do Mg(C2H3O2)2 é 160°C (320°F). Este valor é obtido aquecendo o composto até que ele passe de sólido para líquido. O ponto de fusão é uma propriedade importante que determina a temperatura na qual o composto mudará do estado sólido para o líquido. Esta propriedade é essencial para o correto manuseio e armazenamento do composto.
Densidade de acetato de magnésio g/mL
A densidade do Mg(C2H3O2)2 é 1,45 g/mL. Este valor é obtido dividindo a massa do composto pelo seu volume. A densidade é uma propriedade importante que determina a massa de um determinado volume do composto. É também uma propriedade útil para determinar a pureza do composto, pois as impurezas podem afetar a densidade.
Peso molecular do acetato de magnésio
O peso molecular do Mg(C2H3O2)2 é 142,39 g/mol. Este valor é obtido somando as massas atômicas do magnésio e de dois íons acetato. O peso molecular é uma propriedade importante que determina a quantidade de um composto necessária para uma reação específica. Também é útil na determinação da pureza do composto.
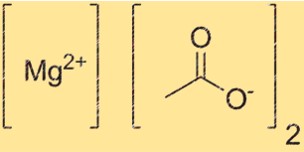
Estrutura do acetato de magnésio
O Mg(C2H3O2)2 possui uma estrutura iônica na qual os cátions Mg2+ são circundados por dois ânions C2H3O2. O cátion Mg2+ tem carga de +2, enquanto o ânion C2H3O2- tem carga de -1. A estrutura é mantida unida pela atração eletrostática entre íons de carga oposta.
| Aparência | Sólido cristalino branco |
| Gravidade Específica | 1,45g/ml |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 142,39 g/mol |
| Densidade | 1,45g/ml |
| Ponto de fusão | 160°C (320°F) |
| Ponto de ebulição | 117,5°C (243,5°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em etanol, metanol, acetona |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | 4,76 |
| pH | 7,5 – 9,0 |
Segurança e perigos do acetato de magnésio
Mg(C2H3O2)2 é geralmente considerado seguro para uso nas aplicações pretendidas, mas como acontece com qualquer composto químico, existem alguns perigos potenciais dos quais você deve estar ciente. Pode irritar a pele, os olhos e o sistema respiratório se inalado ou engolido. A exposição prolongada ou repetida pode causar efeitos mais graves à saúde. O Mg(C2H3O2)2 deve ser manuseado com cuidado e medidas de proteção apropriadas devem ser tomadas ao manusear este composto. Também é importante seguir protocolos adequados de armazenamento e descarte para evitar exposição acidental ou danos ambientais.
| Símbolos de perigo | Nenhum |
| Descrição de segurança | S22 – Não respirar as poeiras; S24/25 – Evitar contato com pele e olhos; S36/37/39 – Usar vestuário de proteção, luvas e proteção ocular/facial adequados; S45 – Em caso de acidente ou indisposição, consulte imediatamente um médico (se possível mostre o rótulo ao médico) |
| Números de identificação da ONU | Não aplicável |
| Código SH | 29152900 |
| Classe de perigo | Não classificado como perigoso |
| Grupo de embalagem | Não aplicável |
| Toxicidade | Baixa toxicidade, mas pode irritar a pele, os olhos e o sistema respiratório se não for manuseado adequadamente |
Métodos de síntese de acetato de magnésio
Sintetize Mg(C2H3O2)2 usando vários métodos, incluindo a reação de óxido de magnésio ou hidróxido de magnésio com ácido acético .
Em um método comum, adicione óxido de magnésio a uma solução de ácido acético para formar Mg(C2H3O2)2 e água. Filtre a solução resultante e evapore-a para obter um produto sólido Mg(C2H3O2)2.
Outro método envolve a reação do magnésio metálico com ácido acético na presença de um catalisador, tal como cloreto de cobre ou sulfato de cobre. A reação produz Mg(C2H3O2)2, gás hidrogênio e cobre metálico como subproduto.
Sintetize Mg(C2H3O2)2 através de uma reação de metátese, reagindo cloreto de magnésio com acetato de sódio na presença de água para produzir Mg(C2H3O2)2 e cloreto de sódio.
No geral, a escolha do método de síntese depende de fatores como a pureza desejada do produto Mg(C2H3O2)2, a disponibilidade de matérias-primas e a escala do processo de produção.
Usos do acetato de magnésio
O Mg(C2H3O2)2 possui uma ampla gama de aplicações em diversas indústrias devido às suas propriedades únicas. Aqui estão alguns usos comuns de Mg(C2H3O2)2:
- Aditivos alimentares: Utilizados como aditivos alimentares para melhorar o valor nutricional dos alimentos e prevenir a deterioração.
- Medicina: Usado medicinalmente como fonte de magnésio, um mineral essencial que desempenha um papel fundamental em muitos processos fisiológicos.
- Têxteis: Utilizado na indústria têxtil como mordente, substância que ajuda a fixar corantes nos tecidos.
- Tratamento de Água: Usado em aplicações de tratamento de água para remover impurezas da água e evitar o acúmulo de incrustações em tubulações e equipamentos.
- Concreto: Utilizado na produção de concreto para melhorar sua resistência e durabilidade.
- Síntese química: utilizada como matéria-prima para a síntese de outros compostos químicos, como fármacos, aromas e perfumes.
Questões:
P: O que é formado quando o ácido acético e o carbonato de magnésio reagem?
R: Quando o ácido acético e o carbonato de magnésio reagem, formam-se Mg(C2H3O2)2, dióxido de carbono e água.
P: Onde comprar acetato de cálcio e magnésio?
R: Cálcio Mg(C2H3O2)2 pode ser adquirido em vários fornecedores de produtos químicos e mercados online.
P: O acetato de magnésio é solúvel em água?
R: Sim, o Mg(C2H3O2)2 é solúvel em água, com solubilidade de aproximadamente 54 g/L à temperatura ambiente.
P: Qual é a concentração molar de uma solução de 5,00 L contendo 0,800 moles de acetato de magnésio?
R: A concentração molar de uma solução de 5,00 L contendo 0,800 moles de Mg(C2H3O2)2 é 0,160 M.
