O acetato de chumbo (Pb(OAc)₂) é um composto cristalino branco. É usado em tinturas de cabelo devido à sua capacidade de escurecer os cabelos. No entanto, apresenta riscos à saúde e deve ser manuseado com cuidado.
| Nome IUPAC | Acetato de chumbo (II) |
| Fórmula molecular | Pb(OAc)₂ |
| Número CAS | 301-04-2 |
| Sinônimos | Etanolato de chumbo (II), acetato de chumbo, diacetato de chumbo |
| InChI | InChI=1S/2C2H4O2.Pb/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
Propriedades do acetato de chumbo
Fórmula de acetato de chumbo
A fórmula química do diacetato de chumbo é Pb(OAc)₂, onde Pb representa o símbolo do chumbo e OAc denota o íon CH₃COO⁻. É um composto cristalino branco com dois íons CH₃COO⁻ por átomo de chumbo.
Massa molar de acetato de chumbo
O diacetato de chumbo tem massa molar de aproximadamente 325,29 g/mol. Para calcular isso, somamos as massas atômicas de um átomo de Pb e dois íons CH₃COO⁻ presentes em sua fórmula química.
Ponto de ebulição do acetato de chumbo
O ponto de ebulição do diacetato de chumbo é de aproximadamente 280°C (536°F). Quando exposto a altas temperaturas, passa por uma transição de fase sólida para líquida, sendo fundamental manuseá-lo com cautela.
Ponto de fusão de acetato de chumbo
O diacetato de chumbo tem um ponto de fusão de aproximadamente 280°C (536°F). A esta temperatura, o composto sólido se transforma em líquido, tornando-o adequado para certas aplicações, como tinturas de cabelo.
Densidade de acetato de chumbo g/mL
A densidade do diacetato de chumbo é de aproximadamente 3,25 g/mL. Este valor representa a massa do composto por unidade de volume e é importante para a compreensão de suas propriedades físicas e aplicações.
Peso molecular do acetato de chumbo
O peso molecular do diacetato de chumbo é de aproximadamente 325,29 g/mol. Ele fornece informações essenciais para vários cálculos químicos e ajuda os pesquisadores a compreender seu comportamento e reatividade.
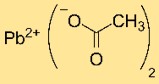
Estrutura de acetato de chumbo
O diacetato de chumbo tem uma estrutura cristalina com cátions Pb²⁺ coordenados a dois íons CH₃COO⁻. O arranjo dos átomos e ligações na rede cristalina determina sua estabilidade e propriedades.
Solubilidade do acetato de chumbo
O diacetato de chumbo é pouco solúvel em água. Dissolve-se até certo ponto para formar uma solução límpida e incolor. Sua solubilidade varia com a temperatura, tornando fundamental seu armazenamento e manuseio adequado para evitar contaminação ambiental.
| Aparência | Cristalino branco |
| Gravidade Específica | ~3,25g/mL |
| Cor | Incolor |
| Cheiro | Inodoro |
| Massa molar | ~325,29 g/mol |
| Densidade | ~3,25g/mL |
| Ponto de fusão | ~280°C (536°F) |
| Ponto de ebulição | ~280°C (536°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Pouco solúvel |
| Solubilidade | Solubilidade limitada, varia com a temperatura |
| Pressão de vapor | Insignificante |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Não disponível |
Segurança e perigos do acetato de chumbo
O diacetato de chumbo apresenta riscos de segurança significativos e deve ser manuseado com muito cuidado. É tóxico se ingerido, inalado ou absorvido pela pele. A exposição prolongada pode levar ao envenenamento por chumbo, causando efeitos adversos à saúde, incluindo o sistema nervoso e os rins. Evite o contato com os olhos, pele e roupas. Use ventilação adequada e equipamento de proteção individual durante o manuseio. Impedir sua liberação no meio ambiente, pois pode contaminar o solo e a água, impactando os ecossistemas. Mantenha-o fora do alcance de crianças e animais. Descarte-o adequadamente de acordo com os regulamentos locais. No geral, a adesão estrita às diretrizes de segurança é crucial para minimizar os riscos.
| Símbolos de perigo | Risco para a saúde, risco ambiental |
| Descrição de segurança | Tóxico e prejudicial ao meio ambiente |
| Números de identificação da ONU | ONU1616 |
| Código SH | 29152900 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | II |
| Toxicidade | Muito tóxico |
Métodos para a síntese de acetato de chumbo
Existem vários métodos para sintetizar diacetato de chumbo.
Uma abordagem comum é reagir o chumbo metálico com ácido acético . Neste método, você normalmente adiciona chumbo a um recipiente e despeja lentamente ácido acético no recipiente enquanto controla condições como agitação e regulação de temperatura. A reação prossegue, formando diacetato de chumbo como um precipitado branco.
Outro método envolve a reação de óxido de chumbo (PbO) ou carbonato de chumbo (PbCO₃) com ácido acético glacial. Você mistura óxido de chumbo ou carbonato de chumbo com ácido acético e aquece a mistura, causando uma reação que resulta em diacetato de chumbo.
Outra rota de síntese consiste em realizar a reação de duplo deslocamento de Pb(NO₃)₂ com CH3COONa em solução aquosa. Esta reação produz diacetato de chumbo como precipitado.
É essencial manusear estes métodos sintéticos com cautela devido à toxicidade dos compostos de chumbo. Você deve seguir medidas de segurança apropriadas e conduzir processos em áreas bem ventiladas e com equipamentos de proteção adequados. Além disso, seguir os regulamentos de eliminação de resíduos é crucial para prevenir a contaminação ambiental.
Usos do acetato de chumbo
O diacetato de chumbo encontra diversas aplicações devido às suas propriedades únicas. Aqui estão alguns usos:
- Tintura de cabelo : Algumas tinturas de cabelo usam diacetato de chumbo para escurecer gradualmente o cabelo ao longo do tempo. Porém, devido à sua toxicidade, seu uso em produtos cosméticos tem sido restringido em muitos países.
- Reagente de Laboratório : É utilizado como reagente em laboratórios para diversas reações e análises químicas.
- Fotografia: No passado, os fotógrafos usavam diacetato de chumbo para sensibilizar filmes e papéis fotográficos ao fotografar em preto e branco.
- Açúcar de Chumbo: Historicamente, as pessoas usavam diacetato de chumbo, conhecido como “açúcar de chumbo”, para conservar vinho e outras bebidas.
- Química Analítica: Na química analítica, os cientistas usam diacetato de chumbo para detectar a presença de gás sulfeto de hidrogênio.
- Mordente no tingimento : Atua como mordente no tingimento e estamparia de têxteis.
- Síntese química : Serve como precursor para a síntese de outros compostos de chumbo.
Apesar de seus diversos usos, é fundamental ter cuidado com o diacetato de chumbo devido à sua alta toxicidade. Minimize a exposição a compostos de chumbo e siga rigorosamente as precauções de segurança adequadas ao manuseá-los e descartá-los para proteger a saúde humana e o meio ambiente. Limite ou substitua muitos de seus aplicativos por alternativas mais seguras.
Questões:
P: O acetato de chumbo II é solúvel em água?
R: O diacetato de chumbo II é pouco solúvel em água.
P: O acetato de chumbo é solúvel?
R: O diacetato de chumbo é pouco solúvel em água.
P: Quais tinturas de cabelo contêm acetato de chumbo?
R: Em alguns países, algumas tinturas capilares progressivas contêm diacetato de chumbo como ingrediente, embora seu uso seja restrito devido a preocupações com toxicidade.
P: A exposição crônica ao ácido acético pode causar quais problemas?
R: A exposição crônica ao ácido acético pode causar irritação respiratória e cutânea.
P: Qual é a fórmula do diacetato de chumbo II?
R: A fórmula do diacetato de chumbo II é Pb(OAc)₂.
P: Qual acetato de chumbo é usado no catalisador Lindlar?
R: O diacetato de chumbo (II) geralmente não é usado no catalisador Lindlar; em vez disso, é usado acetato de paládio.
P: O que é acetato de chumbo?
R: O diacetato de chumbo é um composto cristalino branco usado em diversas aplicações, como tinturas de cabelo e síntese química.
P: Como fazer acetato de chumbo?
R: O diacetato de chumbo pode ser preparado pela reação do chumbo metálico com ácido acético ou por outros métodos de síntese química.
P: Existem tinturas de cabelo sem acetato de chumbo?
R: Sim, muitas tinturas de cabelo modernas não contêm diacetato de chumbo, pois seu uso em produtos cosméticos foi restringido em muitos países devido à sua toxicidade.
P: Ocorre uma reação quando soluções aquosas de iodeto de alumínio e acetato de chumbo (II) são combinadas?
R: Sim, ocorre uma reação e PbI2 e acetato de alumínio são formados como produtos.
P: O cromato de sódio e o acetato de chumbo (II) reagem?
R: Sim, ocorre uma reação que resulta na formação de PbCrO4 e acetato de sódio.
P: Qual produto químico reage com o sulfato de cobre (II) para produzir azul e com o acetato de chumbo (II) para produzir branco?
R: O hidróxido de amônio reage com o sulfato de cobre (II) para formar precipitados azuis (hidróxido de cobre). Em contraste, o sulfeto de hidrogênio reage com o diacetato de chumbo(II) para criar o sulfeto de chumbo branco.
