O 1-pentanol é um álcool líquido incolor com cinco átomos de carbono. É utilizado como solvente e intermediário em síntese química e possui diversas aplicações industriais.
| Nome IUPAC | Pentan-1-ol |
| Fórmula molecular | C₅H₁₁OH |
| Número CAS | 71-41-0 |
| Sinônimos | Álcool amílico, álcool n-amílico, 1-hidroxipentano, álcool n-pentílico, pentanol, álcool pentílico |
| InChI | InChI=1S/C5H12O/c1-2-3-4-5-6/h6H,2-5H2,1H3 |
Propriedades do 1-pentanol
Fórmula 1-pentanol
A fórmula do pentanol é C₅H₁₁OH. Consiste em cinco átomos de carbono, onze átomos de hidrogênio e um grupo hidroxila (-OH). A fórmula representa o arranjo específico e os tipos de átomos em uma molécula de pentanol.
Massa molar de 1-Pentanol
A massa molar do pentanol é calculada somando as massas atômicas de seus átomos constituintes. A massa molar do pentanol é de aproximadamente 88,15 gramas por mol (g/mol). Ele fornece informações sobre a massa de um mol de moléculas de pentanol.
Ponto de ebulição do 1-pentanol
O pentanol tem um ponto de ebulição de cerca de 138 graus Celsius (280 graus Fahrenheit). A esta temperatura, o pentanol líquido se transforma em estado gasoso. O ponto de ebulição indica a temperatura na qual uma substância passa da fase líquida para a gasosa.
Ponto de fusão de 1-pentanol
O ponto de fusão do pentanol é de aproximadamente -79 graus Celsius (-110 graus Fahrenheit). Esta é a temperatura na qual o pentanol sólido se transforma na forma líquida. O ponto de fusão representa a transição do estado sólido para o estado líquido.
Densidade de 1-pentanol g/mL
A densidade do pentanol é de aproximadamente 0,81 gramas por mililitro (g/mL). Densidade é a medida de massa por unidade de volume. Isso indica o quão firmemente as moléculas de uma substância estão compactadas.
Peso Molecular de 1-Pentanol
O peso molecular do 1-pentanol é de aproximadamente 88,15 gramas por mol (g/mol). É a soma dos pesos atômicos de todos os átomos de uma molécula. O peso molecular é usado em vários cálculos, como na determinação do número de moles ou da massa de uma substância.
Estrutura do 1-pentanol
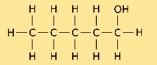
A estrutura do pentanol consiste em uma cadeia linear de cinco átomos de carbono, com um grupo hidroxila (-OH) ligado a uma extremidade. Tem a fórmula química CH₃(CH₂)₃CH₂OH. A estrutura do pentanol desempenha um papel crucial na determinação de suas propriedades físicas e químicas.
Solubilidade de 1-pentanol
O pentanol é solúvel em solventes orgânicos, como éter e acetona, mas tem solubilidade limitada em água. Forma ligações de hidrogênio com moléculas de água devido à presença do grupo hidroxila. A solubilidade do pentanol influencia seu comportamento em diferentes ambientes.
| Aparência | Líquido incolor |
| Gravidade Específica | 0,809-0,814g/mL |
| Cor | Incolor |
| Cheiro | Odor característico |
| Massa molar | 88,15 g/mol |
| Densidade | 0,81g/ml |
| Ponto de fusão | -79°C (-110°F) |
| Ponto de ebulição | 138°C (280°F) |
| Ponto flash | 54°C (129°F) |
| Solubilidade em Água | Ligeiramente solúvel |
| Solubilidade | Solúvel em solventes orgânicos como éter e acetona |
| Pressão de vapor | 2,5 mmHg (25°C) |
| Densidade do vapor | 3,0 (ar = 1) |
| pKa | 16.2 |
| pH | 6,5-8,5 |
1-Pentanol Segurança e perigos
Pentanol apresenta certas considerações de segurança e perigo. Deve ser manuseado com cautela devido à sua natureza inflamável, com ponto de inflamação de 54°c (129°f). Evite contato com chamas abertas ou fontes de ignição. A inalação de vapores de pentanol pode causar irritação do sistema respiratório. O contato direto com a pele pode causar irritação ou ressecamento da pele. Se ingerido acidentalmente, pode causar desconforto gastrointestinal. Ventilação adequada deve ser mantida ao trabalhar com pentanol para minimizar a exposição aos vapores. Equipamentos de proteção individual, como luvas e óculos de segurança, devem ser usados para garantir um manuseio seguro. É importante revisar a ficha de dados de segurança e seguir os protocolos de segurança adequados ao trabalhar com pentanol.
| Símbolos de perigo | Inflamável (F) |
| Descrição de segurança | Manter afastado do calor/faísca/chama aberta/superfícies quentes. Use equipamento elétrico/de ventilação/iluminação à prova de explosão. Evite respirar vapores. Use luvas de proteção/proteção ocular/proteção facial. |
| Números de identificação da ONU | ONU 1105 |
| Código SH | 2905.16.00 |
| Classe de perigo | Classe 3 (líquidos inflamáveis) |
| Grupo de embalagem | GE II |
| Toxicidade | Pode causar irritação. |
Métodos para a síntese de 1-pentanol
Vários métodos permitem a síntese de pentanol.
Um método comum é a hidroformilação de 1-buteno , que envolve a reação de 1-buteno com monóxido de carbono e hidrogênio na presença de um catalisador de ródio. Este processo leva à formação de uma mistura de intermediários aldeídos, seguida de hidrogenação para produzir pentanol.
Outro método envolve a redução do pentanal, um composto aldeído, utilizando um agente redutor como o borohidreto de sódio . Esta reação de redução converte pentanal em pentanol.
Os químicos podem hidratar o 1-penteno, um alceno, para produzir pentanol. Esta reação envolve a adição de água através da ligação dupla carbono-carbono do 1-penteno, resultando na formação de pentanol.
Além disso, o pentanol pode ser sintetizado pela hidrogenação do ácido pentanóico, um ácido carboxílico. A reação ocorre na presença de um catalisador adequado, como paládio sobre carbono e gás hidrogênio, levando à conversão do ácido pentanóico em pentanol.
Esses métodos de síntese oferecem diferentes rotas para obtenção do pentanol, proporcionando flexibilidade de produção dependendo das matérias-primas disponíveis e das condições de reação desejadas.
Usos do 1-pentanol
O pentanol tem diversas utilizações em diferentes indústrias devido às suas propriedades e versatilidade. Aqui estão algumas de suas aplicações notáveis:
- Solvente: O Pentanol serve como solvente em indústrias como farmacêutica, revestimentos e cosméticos, dissolvendo efetivamente muitos compostos orgânicos. Desempenha um papel crucial na formulação de tintas, vernizes e produtos de higiene pessoal.
- Síntese Química: Serve como um importante intermediário na síntese de vários produtos químicos. Pode sofrer reações para produzir ésteres, éteres e outros derivados, que encontram aplicação na produção de perfumes, aromas e ingredientes farmacêuticos.
- Extração: Nos processos de extração, o pentanol é utilizado para separar certos compostos de produtos naturais. Ajuda a extrair substâncias valiosas de materiais vegetais, contribuindo assim para a produção de óleos essenciais, perfumes e aromas.
- Agente de limpeza: Indústrias como eletrônica, óptica e fabricação de precisão usam pentanol como agente de limpeza devido à sua capacidade de dissolver óleos, graxas e outros contaminantes. Garante uma limpeza profunda removendo resíduos das superfícies.
- Aditivo de combustível: Em alguns casos, o pentanol é usado como aditivo de combustível para melhorar a eficiência da combustão e reduzir as emissões. Melhora o desempenho e o impacto ambiental dos combustíveis quando misturados com gasolina ou outros combustíveis.
- Aplicações Industriais: O Pentanol é usado em vários processos industriais, incluindo decapagem, desengorduramento de metais e limpeza industrial. Suas propriedades o tornam eficaz na remoção de revestimentos e contaminantes de superfícies.
- Pesquisa e Laboratório: O Pentanol é usado como reagente ou solvente em pesquisas científicas e laboratórios. Facilita reações, extrações e purificações em diversos procedimentos experimentais.
As diversas aplicações do Pentanol destacam sua importância em diversas indústrias, onde suas propriedades únicas contribuem para o desenvolvimento de inúmeros produtos e processos.
Questões:
P: Qual dos seguintes é mais solúvel em água: ácido acético, pentanol, ácido butanóico ou pentanal?
R: O ácido acético é o mais solúvel em água entre os compostos fornecidos.
P: O pentanol é solúvel em água?
R: Pentanol tem solubilidade limitada em água.
P: Qual é a função do catalisador ácido na promoção da desidratação do 4-metil-2-pentanol?
R: O catalisador ácido facilita a remoção de uma molécula de água do 4-metil-2-pentanol, promovendo sua desidratação.
P: Qual produto é obtido da reação do ácido sulfúrico, ácido acético e 1-pentanol?
R: A reação entre ácido sulfúrico, ácido acético e pentanol resulta na formação de compostos éster.
P: O pentanol tem uma ligação de hidrogênio?
R: Sim, o pentanol pode apresentar ligações de hidrogênio devido à presença do grupo hidroxila.
P: Como preparar o ácido pentanóico a partir do 1-pentanol?
R: O ácido pentanóico pode ser obtido pela oxidação do 1-pentanol usando agentes oxidantes adequados ou pela hidrólise do seu éster correspondente.
P: Que produto orgânico você obteria da reação do 1-pentanol com CrO3, H2O e H2SO4?
R: A reação do 1-pentanol com CrO3, H2O e H2SO4 dá origem à formação do ácido carboxílico correspondente.
P: Qual é menos solúvel em água, 1-pentanol ou 1-heptanol? Explicar.
R: O pentanol é menos solúvel em água do que o 1-heptanol devido à sua cadeia de hidrocarbonetos mais curta, resultando em interações mais fracas com as moléculas de água.
P: Que produto orgânico você obteria da reação do 1-pentanol com o PBr3?
R: A reação do pentanol com PBr3 leva à substituição do grupo hidroxila, resultando na formação de 1-bromopentano.
