O éter vinílico (C4H6O) é um composto químico utilizado em diversas aplicações. Possui propriedades únicas, como reatividade e baixa toxicidade, que o tornam valioso em indústrias como farmacêutica e de síntese orgânica.
| Nome IUPAC | Etoxietileno |
| Fórmula molecular | C4H6O |
| Número CAS | 109-93-3 |
| Sinônimos | éter divinílico; 1,1′-oxibiseteno; Oxirano, óxido de divinila, vinagre |
| InChI | InChI=1S/C4H6O/c1-2-5-4-3-1/h1-4H2 |
Propriedades do éter vinílico
Fórmula de Éter Vinílico
A fórmula do éter vinílico é C4H6O. Consiste em quatro átomos de carbono, seis átomos de hidrogênio e um átomo de oxigênio. Esta fórmula molecular representa a composição do éter vinílico, fornecendo informações sobre os tipos e números de átomos presentes em uma única molécula.
Massa molar de éter vinílico
A massa molar do éter divinílico é calculada somando as massas atômicas de todos os átomos de sua fórmula. A massa molar de C4H6O (éter divinílico) é de aproximadamente 70,09 gramas por mol. Este valor é crucial para vários cálculos, como a determinação da quantidade de éter divinílico necessária para as reações.
Ponto de ebulição do éter vinílico
O éter divinílico tem um ponto de ebulição de cerca de 34,6 graus Celsius (94,3 graus Fahrenheit). Esta temperatura indica o ponto em que o éter divinílico sofre uma mudança de fase de líquido para gás sob pressão atmosférica padrão. O ponto de ebulição relativamente baixo torna o éter divinílico útil em certas aplicações e processos.
Ponto de fusão do éter vinílico
O ponto de fusão do éter divinílico é de aproximadamente -116 graus Celsius (-177 graus Fahrenheit). Esta temperatura indica o ponto em que o éter divinílico muda do estado sólido para o estado líquido. O baixo ponto de fusão é importante porque afeta o manuseio e armazenamento do éter divinílico.
Densidade do éter vinílico g/mL
A densidade do éter divinílico é de aproximadamente 0,734 gramas por mililitro (g/mL). Densidade refere-se à massa de uma substância por unidade de volume. A densidade do éter divinílico fornece informações sobre sua compactação ou concentração, o que pode ser útil para uma variedade de aplicações, incluindo cálculos de formulação e dosagem.
Peso molecular do éter vinílico
O peso molecular do éter divinílico é de aproximadamente 70,09 gramas por mol. Representa a massa de um mol de moléculas de éter divinílico. O peso molecular é crucial para vários cálculos, incluindo a determinação do número de moléculas ou moles presentes em uma determinada quantidade de éter divinílico.
Estrutura do éter vinílico
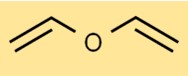
A estrutura do éter divinílico consiste em duas ligações duplas carbono-carbono (C = C) e um átomo de oxigênio ligado a dois dos carbonos (CO). Este arranjo confere ao éter divinílico suas propriedades e reatividade únicas. Compreender a estrutura é importante para estudar seu comportamento em reações químicas e interações com outras substâncias.
Solubilidade do éter vinílico
O éter divinílico é pouco solúvel em água, mas pode dissolver-se em solventes orgânicos como etanol, acetona e clorofórmio. Sua solubilidade depende de fatores como temperatura e natureza do solvente. O conhecimento da solubilidade do éter divinílico é crucial quando se considera suas aplicações, formulações e compatibilidade com outras substâncias.
| Aparência | Líquido incolor |
| Gravidade Específica | 0,734g/ml |
| Cor | N / D |
| Cheiro | Cheiro doce e etéreo |
| Massa molar | 70,09 g/mol |
| Densidade | 0,734g/ml |
| Ponto de fusão | -116°C (-177°F) |
| Ponto de ebulição | 34,6°C (94,3°F) |
| Ponto flash | -40°C (-40°F) |
| Solubilidade em Água | Pouco solúvel |
| Solubilidade | Solúvel em solventes orgânicos |
| Pressão de vapor | 155 mmHg a 20°C |
| Densidade do vapor | 2,50 (ar = 1) |
| pKa | N / D |
| pH | N / D |
Segurança e perigos do éter vinílico
O éter divinílico apresenta alguns riscos de segurança que precisam ser considerados. É inflamável e pode formar misturas explosivas com o ar. Portanto, deve ser armazenado e manuseado longe de chamas ou fontes de ignição. Os vapores de éter divinílico podem causar irritação no sistema respiratório e nos olhos. O contato direto com a pele pode causar dermatites ou queimaduras químicas. Ventilação adequada e equipamento de proteção individual devem ser usados ao trabalhar com éter divinílico. Além disso, é essencial seguir procedimentos de descarte adequados para evitar contaminação ambiental. No geral, seguir os protocolos de segurança é crucial para minimizar os riscos associados ao éter divinílico.
| Símbolos de perigo | Inflamável, prejudicial |
| Descrição de segurança | Mantenha-se afastado de chamas abertas. Usar em uma área bem ventilada. Evite o contato direto com a pele e os olhos. Descarte os resíduos de maneira adequada. |
| Números de identificação da ONU | ONU 1159 |
| Código SH | 2909.19.00 |
| Classe de perigo | Classe 3 (líquidos inflamáveis) |
| Grupo de embalagem | GE II |
| Toxicidade | Nocivo por ingestão ou inalação. Pode causar irritação ou queimaduras na pele e nos olhos. |
Métodos para sintetizar éter vinílico
Existem vários métodos para sintetizar éter divinílico.
Uma abordagem comum é a reação entre etanol e acetileno na presença de um catalisador ácido, como ácido sulfúrico ou ácido p-toluenossulfônico. Isto resulta na formação de éter divinílico como produto. Outro método envolve a adição de um íon alcóxido ao acetileno , que gera um intermediário éter divinílico que pode então ser convertido em éter divinílico por protonação.
O éter divinílico pode ser preparado pela reação de um álcool com haletos de vinil, como cloreto de vinil ou brometo de vinil, por meio de uma reação de eterificação. Esta reacção requer a presença de uma base, tal como carbonato de sódio ou de potássio, para facilitar a formação do éter divinílico desejado.
Para sintetizar o éter divinílico, os alcinos podem reagir com haletos de alquila na presença de uma base forte, como a amida de sódio. Este processo, conhecido como rearranjo de Favorskii, resulta na conversão do halogeneto de alquila em éter divinílico.
A reação de aldeídos ou cetonas com éter etil divinílico, utilizando catalisadores ácidos de Lewis, como cloreto de zinco ou cloreto de alumínio, permite a preparação de derivados de éter divinílico. Este processo, conhecido como reação de Prins, permite a formação de vários derivados do éter divinílico.
Usos do éter vinílico
O éter divinílico é utilizado em diversas aplicações devido às suas propriedades únicas. Aqui estão alguns usos comuns:
- O éter divinílico desempenha um papel crucial como precursor na síntese de compostos farmacêuticos e auxilia na produção de agentes anestésicos, relaxantes musculares e outras substâncias medicinais.
- A síntese orgânica se beneficia muito da versatilidade do éter divinílico, pois serve como um bloco de construção versátil em diversas reações, incluindo reações de acoplamento cruzado, polimerizações e cicloadições, dando origem a compostos orgânicos valiosos.
- O éter divinílico atua como intermediário na produção de uma ampla gama de produtos químicos, como solventes, adesivos, revestimentos e plastificantes, possibilitando a criação de compostos sob medida para aplicações específicas.
- A rápida polimerização do éter divinílico sob luz ultravioleta o torna um componente valioso em revestimentos e adesivos curáveis por UV, fornecendo revestimentos duráveis e de cura rápida para aplicações nos setores automotivo, eletrônico e de impressão.
- A copolimerização do éter divinílico com outros monômeros gera copolímeros com propriedades únicas para diversas aplicações, como sistemas de distribuição de medicamentos, biomateriais e revestimentos.
- Ao funcionar como agente de reticulação, o éter divinílico aumenta a produção de polímeros reticulados, que apresentam resistência mecânica, resistência química e estabilidade térmica melhoradas, provando-se assim úteis em diversas indústrias.
- O éter divinílico fornece uma ferramenta essencial na pesquisa e desenvolvimento laboratorial, permitindo aos cientistas explorar novas reações, desenvolver novos materiais e avançar na compreensão científica, devido à sua reatividade e versatilidade.
Questões:
P: Os éteres vinílicos são estáveis?
R: Os éteres divinílicos são geralmente compostos estáveis, mas sua estabilidade pode variar dependendo de características estruturais específicas e condições de reação.
P: Como desenhar a estrutura do éter vinílico?
A: Para desenhar a estrutura do éter divinílico, represente uma ligação dupla carbono-carbono (C = C) com um carbono ligado a um átomo de oxigênio (CO).
P: O que é éter vinílico/ácido maleico no Polygrip?
R: O copolímero de éter divinílico/ácido maleico é usado no Polygrip como dente adesivo. Ajuda a garantir a adesão entre a prótese e a gengiva.
P: Como fazer éter vinílico?
R: O éter divinílico pode ser produzido por vários métodos, como a reação entre etanol e acetileno ou a eterificação de álcoois com haletos de vinil.
P: Como sintetizar éteres vinílicos?
R: Os éteres divinílicos podem ser sintetizados por várias rotas, incluindo reações envolvendo álcoois, alcinos e haletos de alquila, bem como reações de Prins e rearranjos de Favorskii.
P: O éter de vinil é um aceitador de Michael?
R: Os éteres divinílicos geralmente não são considerados aceitadores de Michael porque não possuem o grupo carbonila α,β-insaturado característico dos aceitadores de Michael.
P: Qual é o papel do éter etilvinílico nas reações ROMP?
R: O éter etilvinílico pode servir como comonômero em reações de polimerização por metátese com abertura de anel (ROMP), contribuindo para a formação de cadeias poliméricas com propriedades específicas.
P: Álcool éter etílico vinílico?
R: O álcool éter etilvinílico não existe como um composto separado. O éter etil divinílico é um composto distinto e não um álcool.
