O etilbenzeno (C8H10) é um composto orgânico com cheiro adocicado. É usado como solvente em diversas indústrias, incluindo plásticos e borracha. Também é encontrado na gasolina e é utilizado na composição de alguns produtos domésticos.
| Nome IUPAC | Etilbenzeno |
| Fórmula molecular | C8H10 |
| Número CAS | 100-41-4 |
| Sinônimos | Etilbenzol, EB, feniletano, etilfenil, 2-feniletano, alfa-metiltolueno, 1-feniletano, etilbenzeno, diluente estireno |
| InChI | InChI=1S/C8H10/c1-2-8-6-4-3-5-7-8/h3-7H,2H2,1H3 |
Propriedades do etilbenzeno
Fórmula de etilbenzeno
A fórmula molecular do etilbenzeno é C8H10, o que significa que consiste em oito átomos de carbono e dez átomos de hidrogênio. A estrutura química do etilbenzeno apresenta um anel de benzeno ligado a um grupo etil.
Massa molar de etilbenzeno
A massa molar de C8H10 é 106,17 g/mol. Isso é calculado adicionando as massas atômicas de todos os átomos de uma molécula C8H10.
Ponto de ebulição do etilbenzeno
O ponto de ebulição do C8H10 é 136,2°C (277,2°F). Esta é a temperatura na qual a forma líquida do C8H10 se transforma em gás. O C8H10 tem um ponto de ebulição relativamente baixo em comparação com outros hidrocarbonetos aromáticos, tornando-o útil como solvente em diversas indústrias.
Ponto de fusão do etilbenzeno
O ponto de fusão do C8H10 é -95,2°C (-139,4°F). Esta é a temperatura na qual a forma sólida do C8H10 se transforma em líquido. O C8H10 tem um ponto de fusão relativamente baixo em comparação com outros hidrocarbonetos aromáticos, o que o torna útil como matéria-prima para a produção de outros produtos químicos.
Densidade de etilbenzeno g/mL
A densidade do C8H10 é 0,867 g/mL a 20°C (68°F). Isto significa que um mililitro de C8H10 pesa 0,867 gramas a esta temperatura. C8H10 é menos denso que a água, o que significa que flutuará na superfície da água se os dois líquidos forem misturados.
Peso molecular do etilbenzeno
O peso molecular de C8H10 é 106,17 g/mol. Esta é a massa de uma molécula C8H10, que pode ser calculada somando as massas atômicas de todos os átomos da molécula.
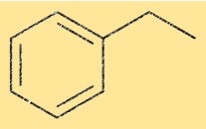
Estrutura do etilbenzeno
A estrutura do C8H10 consiste em um anel benzênico ligado a um grupo etil. O grupo etil está ligado a um dos átomos de carbono do anel benzeno. Essa estrutura também é conhecida como feniletano.
Solubilidade do etilbenzeno
C8H10 é insolúvel em água, mas solúvel em solventes orgânicos como álcoois, éteres e clorofórmio. Isto significa que o C8H10 não se dissolverá em água, mas sim em outros líquidos com propriedades químicas semelhantes. A solubilidade do C8H10 em vários solventes depende de fatores como temperatura, pressão e propriedades químicas do solvente.
| Aparência | Líquido incolor |
| Gravidade Específica | 0,867 g/ml a 20°C |
| Cor | Incolor |
| Cheiro | Aroma doce |
| Massa molar | 106,17 g/mol |
| Densidade | 0,867 g/ml a 20°C |
| Ponto de fusão | -95,2°C (-139,4°F) |
| Ponto de ebulição | 136,2°C (277,2°F) |
| Ponto flash | 11,1°C (52°F) |
| Solubilidade em Água | 0,30 g/L a 20°C |
| Solubilidade | Solúvel em solventes orgânicos como álcoois, éteres e clorofórmio |
| Pressão de vapor | 10,7 mmHg a 20°C |
| Densidade do vapor | 3.7 |
| pKa | 10.17 |
| pH | Não aplicável |
Segurança e perigos do etilbenzeno
O C8H10 pode ser perigoso se não forem tomadas as devidas precauções ao manuseá-lo e usá-lo. É classificado como um líquido inflamável e pode pegar fogo se exposto ao calor ou chama. O C8H10 também pode ser prejudicial se inalado ou ingerido. A exposição a altas concentrações de C8H10 pode causar tonturas, dores de cabeça e irritação respiratória. A exposição prolongada ao C8H10 tem sido associada a danos no fígado e nos rins. Devem ser tomadas precauções de segurança ao trabalhar com o C8H10, como usar roupas e luvas de proteção, trabalhar em áreas bem ventiladas e armazená-lo em local seguro, fresco e seco.
| Símbolos de perigo | Inflamável, prejudicial |
| Descrição de segurança | Manter afastado do calor, faíscas, chamas abertas e superfícies quentes. Utilize equipamento à prova de explosão. Evite respirar poeiras/fumos/gases/névoas/vapores/aerossóis. Lave bem após o manuseio. |
| Números de identificação da ONU | ONU 1175 |
| Código SH | 2902.90.20 |
| Classe de perigo | 3 (Líquidos inflamáveis) |
| Grupo de embalagem | II (Perigo Médio) |
| Toxicidade | O etilbenzeno é considerado uma substância moderadamente tóxica. Pode causar irritação nos olhos e na pele, problemas respiratórios e danos ao sistema nervoso se a exposição for prolongada ou em altas concentrações. |
Métodos para a síntese de etilbenzeno
O método mais comumente usado para sintetizar C8H10 é a desidrogenação catalítica do etilciclohexano. Este processo envolve o aquecimento de uma mistura de etilciclohexano e gás hidrogênio sobre um catalisador em alta temperatura, o que faz com que os átomos de hidrogênio se separem do grupo etil, resultando na formação de C8H10.
Outro método de síntese de C8H10 envolve a alquilação do benzeno com gás etileno . Esta reação requer um catalisador, geralmente cloreto de alumínio, e resulta na formação de C8H10 e cloreto de hidrogênio como subproduto.
Um método alternativo para produzir C8H10 envolve a reação do benzeno com cloreto de etila na presença de um catalisador ácido de Lewis, como o cloreto de alumínio. Este processo resulta na formação de C8H10 e cloreto de hidrogênio como subproduto.
Além dos métodos mencionados, os pesquisadores também estão desenvolvendo novos métodos para sintetizar o C8H10, como o uso de líquidos iônicos como solvente para a alquilação do etileno do benzeno . Estes métodos têm o potencial de oferecer benefícios em termos de eficiência e sustentabilidade ambiental. Entretanto, seu uso industrial ainda não está difundido.
Usos do etilbenzeno
O C8H10 tem vários usos importantes em diversos setores. Alguns de seus principais usos são:
- Produção de estireno: A produção de estireno, que é usado para fabricar uma variedade de plásticos, resinas e borracha sintética, ligado ao C8H10 como um intermediário chave.
- Solvente: Comumente usado como solvente para diversas aplicações, incluindo tintas, revestimentos, adesivos e produtos de limpeza.
- Aditivo de combustível: Adicionado à gasolina para melhorar sua octanagem, o que pode melhorar o desempenho do motor.
- Intermediário químico: utilizado como matéria-prima para a síntese de outros produtos químicos, como feniletanol e dietilbenzeno.
- Produção de polímeros: utilizados na produção de diversos tipos de polímeros, como poliestireno e resinas de acrilonitrila-butadieno-estireno (ABS).
- Agricultura: Também usado como pesticida e herbicida.
- Aplicações Médicas: Utilizado como anestésico local, bem como solvente para produtos farmacêuticos.
Questões:
P: Quantos sinais você esperaria ver no espectro de RMN de 1H para o etilbenzeno?
R: O espectro de RMN de 1H para C8H10 teria quatro sinais: dois para os prótons no anel de benzeno (que apareceria como um dupleto) e dois para os prótons do grupo etil (que apareceria como um tripleto).
P: Que proporções de benzeno e etilbenzeno devem ser misturadas?
R: As proporções de benzeno e C8H10 a serem misturadas dependem da concentração desejada de C8H10 na mistura. A relação benzeno/C8H10 pode variar de 10:1 a 1:1, dependendo da aplicação.
P: O que é nitração de etilbenzeno?
R: A nitração de C8H10 envolve a reação de C8H10 com uma mistura de ácido nítrico e ácido sulfúrico, resultando na introdução de um ou mais grupos nitro no anel benzênico de C8H10. Esta reação é comumente usada na produção de produtos químicos industriais, como nitrobenzeno e feniletilaminas.
P: O etilbenzeno é polar?
R: C8H10 é um composto apolar devido à estrutura simétrica do anel benzênico, que nega qualquer polaridade do grupo etil. Como resultado, o C8H10 tem baixa solubilidade em água e é geralmente solúvel em solventes apolares, como hexano e tolueno.
P: Como mudar de etilbenzeno para estireno?
R: C8H10 pode ser convertido em estireno através do processo de desidrogenação, que envolve a remoção de dois átomos de hidrogênio do grupo etil usando um catalisador como óxido de ferro ou óxido de cromo. Este processo resulta na formação de estireno e gás hidrogênio como subproduto. O estireno resultante pode então ser purificado e utilizado na produção de diversos materiais industriais, como plásticos, resinas e borracha sintética.
