O tetrahidrofurano (THF) é um composto orgânico incolor. É comumente usado como solvente em diversas indústrias devido à sua capacidade de dissolver uma ampla gama de substâncias.
| Nome IUPAC | Oxolano |
| Fórmula molecular | C4H8O |
| Número CAS | 109-99-9 |
| Sinônimos | THF, oxaciclopentano, óxido de butileno, óxido de dietileno, óxido de ciclotetrametileno |
| InChI | InChI=1S/C4H8O/c1-2-4-5-3-1/h1-4H2 |
Propriedades do tetrahidrofurano
Fórmula de Tetrahidrofurano
O tetrahidrofurano (THF) tem fórmula química C4H8O. É um éter cíclico com um anel de cinco membros contendo quatro átomos de carbono e um átomo de oxigênio. O THF tem baixo ponto de ebulição e é comumente usado como solvente em diversas indústrias.
Massa molar de tetraidrofurano
A massa molar do THF é de aproximadamente 72,11 g/mol. Este valor é calculado somando as massas atômicas dos átomos constituintes da fórmula molecular. A massa molar relativamente baixa do THF contribui para o seu baixo ponto de ebulição e baixa volatilidade, tornando-o um solvente eficaz para uma ampla gama de compostos orgânicos.
Ponto de ebulição do tetrahidrofurano
O ponto de ebulição do THF é 66°C (151°F) à pressão atmosférica padrão. O baixo ponto de ebulição do THF o torna útil como solvente para reações químicas que requerem altas temperaturas, como as reações de Grignard. No entanto, o baixo ponto de ebulição também significa que o THF é muito volátil, por isso deve-se ter cuidado ao manuseá-lo.
Ponto de fusão do tetrahidrofurano
O ponto de fusão do THF é de aproximadamente −108,5°C (−163,3°F). O THF é líquido à temperatura ambiente, mas pode solidificar a baixas temperaturas. O baixo ponto de fusão do THF o torna útil como solvente criogênico para aplicações em baixas temperaturas.
Densidade de tetrahidrofurano g/mL
A densidade do THF é de aproximadamente 0,889 g/mL a 20°C (68°F). Este valor é relativamente baixo em comparação com outros solventes comuns. A baixa densidade do THF torna-o útil como solvente para reações sensíveis à densidade porque pode diminuir a densidade geral da mistura de reação.
Peso Molecular do Tetrahidrofurano
O peso molecular do THF é de aproximadamente 72,11 g/mol. Este valor é calculado somando as massas atômicas dos átomos constituintes da fórmula molecular. O peso molecular relativamente baixo do THF contribui para o seu baixo ponto de ebulição e volatilidade.
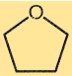
Estrutura do tetrahidrofurano
O THF tem uma estrutura de anel de cinco membros com quatro átomos de carbono e um átomo de oxigênio. Os átomos de carbono estão dispostos em uma geometria tetraédrica, com cada átomo de carbono ligado a outros dois átomos de carbono e um átomo de hidrogênio. O átomo de oxigênio está ligado a um átomo de carbono e a um átomo de hidrogênio.
Solubilidade do tetrahidrofurano
O THF é um solvente polar aprótico capaz de dissolver uma ampla gama de compostos orgânicos. O THF é miscível com água e é comumente usado como co-solvente em várias reações químicas. Porém, o THF pode não ser compatível com alguns materiais, por isso é importante verificar sua compatibilidade antes de utilizá-lo.
| Aparência | Líquido incolor |
| Densidade específica | 0,889 |
| Cor | Incolor |
| Cheiro | cheiro de éter |
| Massa molar | 72,11 g/mol |
| Densidade | 0,889g/ml |
| Ponto de fusão | −108,5°C (−163,3°F) |
| Ponto de ebulição | 66°C (151°F) |
| Ponto flash | −14°C (7°F) |
| Solubilidade em Água | Miscível |
| Solubilidade | Solúvel em etanol, éter, acetona, benzeno |
| Pressão de vapor | 200 mmHg a 20°C |
| Densidade do vapor | 2,5 (ar = 1) |
| pKa | 25.3 |
| pH | Neutro (7) |
Segurança e perigos do tetrahidrofurano
O tetrahidrofurano (THF) apresenta vários riscos à segurança e à saúde. O THF é altamente inflamável e pode inflamar-se à temperatura ambiente. Também pode liberar vapores tóxicos quando aquecido ou queimado. A exposição ao THF pode causar irritação na pele e nos olhos, e a exposição prolongada pode causar danos ao fígado e aos rins. O THF também é conhecido por causar tonturas e dores de cabeça, e a inalação repetida pode causar problemas respiratórios. Deve-se ter cuidado ao manusear o THF e devem ser usados equipamentos de proteção, como luvas e óculos de segurança. O THF deve ser armazenado em local fresco e bem ventilado, longe de fontes de calor e materiais incompatíveis.
| Símbolos de perigo | Inflamável, Tóxico |
| Descrição de segurança | Líquido e vapor altamente inflamáveis. Causa irritação ocular grave. Pode causar sonolência ou tonturas. Pode ser prejudicial se ingerido ou inalado. |
| Números de identificação da ONU | ONU2056 |
| Código SH | 29321100 |
| Classe de perigo | 3 (Líquidos inflamáveis) |
| Grupo de embalagem | II |
| Toxicidade | LD50 (oral, rato) – 5.410 mg/kg |
Métodos para a síntese de tetrahidrofurano
Vários métodos podem ser usados para sintetizar Tetrahidrofurano (THF).
Um método comum envolve a hidrogenação catalítica do furano. Isto envolve a passagem de vapor de furano sobre um catalisador de níquel ou paládio na presença de gás hidrogênio. A reação resultante produz THF e água como subprodutos.
Outro método envolve a reação do 1,4-butanodiol com ácido sulfúrico , seguida de destilação para produzir THF. Os perigos do ácido sulfúrico concentrado tornam este método menos comum.
A desidratação catalisada por ácido do 1,4-butanodiol é outra forma de sintetizar o THF. Este método envolve o aquecimento do 1,4-butanodiol com um ácido forte, como o ácido sulfúrico , para remover água e produzir THF.
Além disso, o THF pode ser obtido por hidrogenólise catalítica de celulose ou outros açúcares derivados de biomassa. Este método é de interesse crescente devido ao potencial de fontes renováveis de produção de THF.
Cada método tem suas vantagens e desvantagens, e o método específico escolhido dependerá de fatores como custo, disponibilidade de matéria-prima e pureza desejada do produto final.
Usos do tetrahidrofurano
O tetrahidrofurano (THF) tem diversas aplicações industriais e laboratoriais, incluindo:
- Solvente: Comumente utilizado como solvente para diversos compostos orgânicos devido ao seu alto poder solvente e baixo ponto de ebulição.
- Polimerização: Utilizado como co-solvente na polimerização de poliestireno e cloreto de polivinila, bem como na produção de espumas de poliuretano.
- Síntese química: utilizado como solvente de reação em síntese química orgânica, como na preparação de reagentes de Grignard.
- Extração: Utilizado como solvente de extração para diversos produtos naturais, como alcalóides e esteróides.
- Adesivos: Utilizados como componente em formulações adesivas, como aquelas utilizadas na fabricação de calçados e couro.
- Revestimentos: Utilizados na produção de revestimentos e vernizes, bem como na formulação de tintas e lacas.
- Química Analítica: Usado como solvente de fase móvel em análises de cromatografia líquida de alta eficiência (HPLC) e cromatografia gasosa (GC).
Questões:
P: Qual é o principal produto orgânico formado quando o tetrahidrofurano é tratado com excesso de HBr?
R: Quando o THF é tratado com excesso de HBr, o principal produto orgânico formado é o 3-bromo-1,4-dioxano.
P: O tetrahidrofurano é miscível com água?
R: Sim, o THF é miscível com água. Possui alta solubilidade em solventes polares, principalmente água.
P: O tetrahidrofurano danificará a borracha?
R: Sim, o THF pode danificar a borracha. Isso pode causar inchaço, amolecimento e rachaduras nos materiais de borracha.
P: O tetrahidrofurano é polar ou apolar?
R: THF é um solvente polar. Possui momento dipolar devido ao átomo de oxigênio presente em sua estrutura em anel, o que o torna um bom solvente para compostos polares.
P: O tetrahidrofurano explodirá na água?
R: Não, o THF não explode na água. No entanto, pode formar um peróxido explosivo se exposto ao ar por períodos prolongados. O armazenamento e o manuseio adequados são necessários para evitar a formação de peróxidos.
P: Qual é o SDS do tetrahidrofurano?
R: A FDS (Ficha de Dados de Segurança) do THF fornece informações sobre suas propriedades físicas e químicas, instruções de manuseio e armazenamento, precauções de saúde e segurança e procedimentos de resposta a emergências. É importante revisar e seguir as informações fornecidas na FDS ao trabalhar com THF.
