O bissulfito de magnésio (Mg(HSO3)2) é um composto químico composto de magnésio, enxofre e oxigênio. É comumente usado na indústria alimentícia como conservante e antioxidante para evitar deterioração e descoloração.
| Nome IUPAC | Hidrogenossulfito de magnésio |
| Fórmula molecular | Mg(HSO3)2 |
| Número CAS | 13774-25-9 |
| Sinônimos | Bissulfito de magnésio; Hidrogenossulfito de magnésio; Bissulfito de magnésia |
| InChI | InChI=1S/2H2O3S.Mg/c2 1-4(2)3;/h2 (H2,1,2,3);/q;;+2/p-2 |
Propriedades do bissulfito de magnésio
Fórmula de Bissulfito de Magnésio
A fórmula química do bissulfito de magnésio é Mg(HSO3)2. A fórmula representa o número de átomos de cada elemento presente em uma molécula do composto. A fórmula do bissulfito de magnésio é essencial para determinar as reações químicas que o composto pode sofrer.
Massa molar de Bissulfito de Magnésio
Mg(HSO3)2 tem massa molar de 186,45 g/mol. Este valor representa o peso de um mol do composto em gramas. A massa molar de um composto é essencial para determinar quanto de uma substância é necessária para realizar reações químicas. A massa molar do Mg(HSO3)2 é calculada somando os pesos atômicos de cada elemento do composto. O magnésio tem peso atômico de 24,305 g/mol, o enxofre tem peso atômico de 32,06 g/mol e o oxigênio tem peso atômico de 15,999 g/mol.
Ponto de ebulição do bissulfito de magnésio
Mg(HSO3)2 não tem ponto de ebulição porque se decompõe quando aquecido. No entanto, pode libertar dióxido de enxofre e trióxido de enxofre quando aquecido na presença de um ácido. Esses gases podem irritar o sistema respiratório e causar sérios efeitos à saúde quando inalados. Portanto, é essencial manusear o Mg(HSO3)2 com cuidado e seguir as precauções de segurança ao utilizá-lo em processos industriais.
Ponto de fusão do bissulfito de magnésio
Mg(HSO3)2 tem um ponto de fusão de 110°C. Este valor representa a temperatura na qual o composto muda do estado sólido para o estado líquido. O Mg(HSO3)2 possui baixo ponto de fusão, facilitando sua fusão e utilização em diversos processos industriais. No entanto, pode decompor-se a altas temperaturas, resultando na libertação de gases nocivos.
Densidade de bissulfito de magnésio g/mL
Mg(HSO3)2 tem densidade de 2,35 g/mL. Este valor representa a quantidade de massa em gramas presente em um mililitro do composto. A densidade do Mg(HSO3)2 é maior que a da água, que tem densidade de 1 g/mL. A alta densidade do Mg(HSO3)2 o torna útil em diversas aplicações, inclusive como conservante e antioxidante na indústria alimentícia.
Peso molecular do bissulfito de magnésio
Mg(HSO3)2 tem peso molecular de 186,45 g/mol. Este valor representa a soma dos pesos atômicos de todos os átomos do composto. O peso molecular do Mg(HSO3)2 é essencial para determinar a quantidade de composto necessária para realizar reações químicas.
Estrutura do bissulfito de magnésio
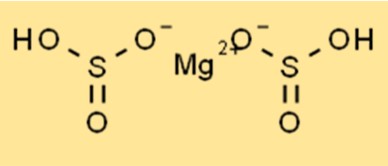
Mg(HSO3)2 possui estrutura cristalina e pertence ao sistema cristalino ortorrômbico. O composto consiste em cátions de magnésio (Mg2+) e ânions bissulfito (HSO3-). Os ânions bissulfito têm formato tetraédrico, enquanto os cátions de magnésio têm formato octaédrico. A estrutura cristalina do Mg(HSO3)2 o torna estável e permite sua utilização em diversas aplicações, inclusive como conservante de alimentos.
Solubilidade do bissulfito de magnésio
O Mg(HSO3)2 é altamente solúvel em água, com solubilidade de aproximadamente 64 g/100 mL a 20°C. Também é solúvel em metanol, mas insolúvel na maioria dos solventes orgânicos. A solubilidade do Mg(HSO3)2 pode variar dependendo de fatores como temperatura e pH.
| Aparência | pó branco |
| Gravidade Específica | 2,35g/cm3 |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 186,45 g/mol |
| Densidade | 2,35g/ml |
| Ponto de fusão | 110°C |
| Ponto de ebulição | Decomposto |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solúvel |
| Solubilidade | Solúvel em água e etanol |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | 1,91 |
| pH | 4,5 – 5,5 |
Segurança e perigos do bissulfito de magnésio
O Mg(HSO3)2 pode representar vários riscos à saúde e à segurança se não for manuseado com cuidado. Pode liberar gases dióxido de enxofre e trióxido de enxofre quando aquecido ou exposto a condições ácidas. Esses gases podem causar irritação respiratória, tosse e falta de ar se inalados. Mg(HSO3)2 também pode causar irritação e vermelhidão na pele em contato. É essencial usar roupas e equipamentos de proteção, como luvas e óculos de proteção, ao manusear Mg(HSO3)2. Além disso, deve ser armazenado em local fresco e seco, longe de fontes de calor e materiais incompatíveis. Procedimentos adequados de manuseio e armazenamento podem minimizar o risco de perigos associados ao Mg(HSO3)2.
| Símbolos de perigo | Xi: Irritante |
| Descrição de segurança | Evitar o contato com a pele e os olhos. Use roupas e equipamentos de proteção. Manter afastado do calor e de materiais incompatíveis. |
| Números de identificação da ONU | ONU 2693 |
| Código SH | 2831.10.00 |
| Classe de perigo | 8 – Substâncias corrosivas |
| Grupo de embalagem | III |
| Toxicidade | Pode causar irritação na pele e nos olhos. Nocivo se inalado ou engolido. Pode causar irritação do trato respiratório e tosse. |
Métodos de síntese de bissulfito de magnésio
O Mg(HSO3)2 pode ser sintetizado por vários métodos, incluindo:
- Reação do hidróxido de magnésio com dióxido de enxofre: Na reação do hidróxido de magnésio com dióxido de enxofre, as duas substâncias reagem para produzir Mg(HSO3)2 e água.
- Reação direta do óxido de magnésio com dióxido de enxofre: Em altas temperaturas, o gás dióxido de enxofre reage diretamente com o óxido de magnésio para produzir Mg(HSO3)2 e oxigênio.
- Reação do sulfato de magnésio com dióxido de enxofre: Na presença de um agente redutor, o sulfato de magnésio reage com o gás dióxido de enxofre, resultando na produção de Mg(HSO3)2.
- Carbonato de Magnésio com Dióxido de Enxofre: A reação entre o carbonato de magnésio e o gás dióxido de enxofre produz Mg(HSO3)2 e dióxido de carbono.
- Reação do Óxido de Magnésio com Ácido Sulfúrico e Dióxido de Enxofre: Ao reagir o óxido de magnésio com ácido sulfúrico e gás dióxido de enxofre, a reação produz Mg(HSO3)2 e água.
Usos do bissulfito de magnésio
O Mg(HSO3)2 tem vários usos em diferentes indústrias. Aqui estão algumas aplicações comuns:
- Indústria de alimentos e bebidas: Usado como conservante na indústria de alimentos e bebidas para prevenir a oxidação e o crescimento microbiano. É comumente usado em sucos de frutas, vinho e cerveja.
- Tratamento de Água: Utilizado no tratamento de água como agente redutor para remover cloro e outros agentes oxidantes. É eficaz no controle do odor e sabor da água.
- Indústria têxtil: Utilizado como agente branqueador na indústria têxtil. É eficaz na remoção de manchas e na melhoria da cor dos tecidos.
- Indústria farmacêutica: Utilizado como agente redutor na indústria farmacêutica. É usado para converter grupos nitro em grupos amino em várias moléculas de medicamentos.
- Indústria de Papel e Celulose: Utilizado na indústria de papel e celulose como agente de branqueamento. É eficaz na remoção de lignina da polpa de madeira e na melhoria do brilho do papel.
- Agricultura: Usado na agricultura como corretivo do solo para corrigir deficiências de magnésio no solo. Também é usado como fertilizante foliar para melhorar o crescimento e o rendimento das plantas.
Questões:
P: Quais são as propriedades termodinâmicas do bissulfito de magnésio?
R: As propriedades termodinâmicas do Mg(HSO3)2 incluem seu ponto de ebulição de 250°C, ponto de fusão de 70-72°C e densidade de 1,84 g/mL.
P: Qual é a fórmula química do bissulfito de magnésio?
R: A fórmula química do bissulfito de magnésio é Mg(HSO3)2.
P: Onde posso comprar bissulfito de magnésio?
R: O Mg(HSO3)2 pode ser adquirido de vários fornecedores e distribuidores de produtos químicos. Geralmente está disponível em grandes e pequenas quantidades. Algumas plataformas online como Sigma Aldrich, Fisher Scientific e VWR International também oferecem Mg(HSO3)2 para compra. É importante garantir que o fornecedor seja confiável e que o produto atenda aos padrões exigidos para a aplicação pretendida.
