O bissulfito de sódio (NaHSO3) é um composto químico utilizado como conservante de alimentos e em diversas aplicações industriais. Atua inibindo o crescimento de bactérias e prevenindo a oxidação.
| Nome IUPAC | Hidrogenossulfito de sódio |
| Fórmula molecular | NaHSO3 |
| Número CAS | 7631-90-5 |
| Sinônimos | Bissulfito de sódio, Sulfito ácido de sódio, Hidrogenossulfito de sódio, Hidrogenossulfito de sódio, Sulfito de sódio monohidratado |
| InChI | InChI=1S/Na.H2O3S/c;1-4(2)3/h;(H2,1,2,3)/q+1;/p-1 |
Propriedades do bissulfito de sódio
Fórmula de bissulfito de sódio
A fórmula química do bissulfito de sódio é NaHSO3. Esta fórmula indica o número e tipo de átomos presentes em uma única molécula de bissulfito de sódio. A fórmula é crucial para determinar o comportamento do bissulfito de sódio sob diferentes reações químicas e condições físicas.
Massa molar de bissulfito de sódio
NaHSO3 tem massa molar de 104,06 g/mol. Esta é a soma das massas atômicas dos elementos constituintes de uma única molécula de NaHSO3. A massa molar é uma propriedade física importante que ajuda a determinar a quantidade de uma substância em uma determinada amostra.
Ponto de ebulição do bissulfito de sódio
O ponto de ebulição do NaHSO3 é 150°C. Esta é a temperatura na qual a forma líquida do NaHSO3 começa a se transformar em gás. O ponto de ebulição é uma propriedade física crucial que determina como uma substância se comporta sob diferentes condições de temperatura.
Ponto de fusão do bissulfito de sódio
O ponto de fusão do NaHSO3 é 150°C. Esta é a temperatura na qual a forma sólida do NaHSO3 começa a se transformar em líquido. O ponto de fusão é uma propriedade física essencial que ajuda a determinar o comportamento de uma substância sob diferentes condições de temperatura.
Densidade de bissulfito de sódio g/mL
A densidade do NaHSO3 é 1,48 g/mL. Refere-se à quantidade de massa presente em um determinado volume de NaHSO3. A densidade é uma propriedade física importante que ajuda a determinar como uma substância se comporta sob diferentes condições de pressão e temperatura.
Peso molecular do bissulfito de sódio
O peso molecular do NaHSO3 é 104,06 g/mol. Esta é a soma dos pesos atômicos dos elementos constituintes de uma única molécula de NaHSO3. O peso molecular é uma propriedade física essencial que ajuda a determinar a quantidade de uma substância em uma determinada amostra.
Estrutura do bissulfito de sódio
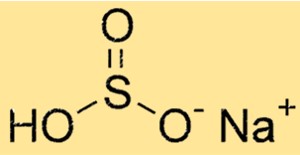
O NaHSO3 possui uma estrutura molecular composta por um cátion sódio (Na+) e um ânion HSO3-. O ânion consiste em um átomo de enxofre, três átomos de oxigênio e um átomo de hidrogênio. A estrutura do NaHSO3 determina suas propriedades químicas e físicas.
Solubilidade do bissulfito de sódio
O NaHSO3 é altamente solúvel em água, com solubilidade de 62 g/100 mL a 20°C. Também é solúvel em glicerol e ligeiramente solúvel em álcool. Sua solubilidade em água o torna um reagente útil em diversas reações químicas.
| Aparência | Pó cristalino branco |
| Gravidade Específica | 1,48 |
| Cor | Branco a ligeiramente amarelo |
| Cheiro | Cheiro sulfuroso |
| Massa molar | 104,06 g/mol |
| Densidade | 1,48g/ml |
| Ponto de fusão | 150ºC |
| Ponto de ebulição | 150ºC |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em etanol |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | 6,97 |
| pH | 4,5-5,5 (solução a 5%) |
Segurança e perigos do bissulfito de sódio
O NaHSO3 pode ser prejudicial se ingerido, inalado ou entrar em contato com a pele ou os olhos. Isso pode causar irritação na pele, lesões oculares e problemas respiratórios e digestivos. A exposição prolongada pode levar a problemas de saúde mais graves. É importante manusear e armazenar o NaHSO3 com cuidado, utilizando equipamentos de proteção individual como luvas, óculos de proteção e respiradores. Deve ser mantido afastado de materiais combustíveis e substâncias incompatíveis. Em caso de contato ou ingestão acidental, deve-se procurar atendimento médico imediato. Procedimentos adequados de armazenamento e manuseio devem ser seguidos para evitar perigos potenciais.
| Símbolos de perigo | Caveira e Ossos Cruzados, Corrosivos |
| Descrição de segurança | Evite contato com a pele, olhos e roupas. Não ingerir ou inalar. Utilize equipamento de proteção adequado. |
| Números de identificação da ONU | UN2693 |
| Código SH | 28321000 |
| Classe de perigo | 8 |
| Grupo de embalagem | III |
| Toxicidade | Muito tóxico por ingestão ou inalação. Pode causar irritação na pele e nos olhos, problemas respiratórios e digestivos. A exposição prolongada pode causar sérios problemas de saúde. |
Métodos para a síntese de bissulfito de sódio
Existem diferentes métodos para sintetizar NaHSO3, mas o mais comum envolve a reação de carbonato de sódio e dióxido de enxofre.
Para produzir uma solução de NaHSO3, misture uma solução de carbonato de sódio com dióxido de enxofre gasoso. A reação libera calor e requer um recipiente de reação com ventilação adequada.
Outro método envolve a reação do hidróxido de sódio com gás dióxido de enxofre para produzir uma solução de sulfito de sódio, que é então acidificada para produzir uma solução de NaHSO3. Para grandes quantidades de NaHSO3 este método se mostra útil.
Para sintetizar NaHSO3, o ácido sulfúrico reage com o sulfito de sódio , criando uma solução de NaHSO3. Este método é benéfico quando é necessária uma solução mais concentrada de NaHSO3.
Usos do bissulfito de sódio
O NaHSO3 tem uma ampla gama de utilizações em diversas indústrias. Aqui estão alguns de seus usos comuns:
- Indústria Alimentícia – Usado como conservante de alimentos para prevenir o crescimento de bactérias e prolongar a vida útil de produtos alimentícios, como frutas e vegetais enlatados, sucos e vinho.
- Tratamento de Água – Usado como agente redutor para remover o excesso de cloro da água potável e dos sistemas de tratamento de águas residuais.
- Indústria Têxtil – Usado como alvejante para remover corantes residuais dos têxteis.
- Indústria Fotográfica – Utilizado como agente revelador no processamento fotográfico.
- Perfuração de Petróleo – Usado como inibidor de corrosão e em sistemas de recuperação para remover oxigênio e prevenir a corrosão durante operações de perfuração de petróleo e gás.
- Produtos Farmacêuticos – Utilizados como antioxidante e agente redutor na fabricação de determinados produtos farmacêuticos.
- Cuidados Pessoais – Utilizado como alisador de cabelos e na produção de alguns produtos de cuidados pessoais como xampus e condicionadores.
- Outros usos – Utilizado na produção de papel e celulose, como reagente de laboratório e como agente quelante de íons metálicos.
Questões:
P: O que é NaHSO3?
R: NaHSO3 é a fórmula química do bissulfito de sódio, um sal usado para diversos fins em diferentes indústrias.
P: Qual é o pH aproximado de 0,015 M NaHSO3?
R: O pH aproximado de NaHSO3 0,015 M é aproximadamente 7. Esta solução é neutra porque não é um ácido nem uma base.
P: O NaHSO3 é ácido ou básico?
R: O NaHSO3 é ligeiramente ácido porque pode doar íons hidrogênio na água para formar íons HSO3- e H+.
P: Qual é o número de oxidação do enxofre (S) no NaHSO3, um dos reagentes usados neste experimento?
R: O número de oxidação do enxofre (S) em NaHSO3 é +4.
P: O que o NaHSO3 faz?
R: O NaHSO3 é usado como agente redutor e fonte de dióxido de enxofre. Também pode atuar como antioxidante e conservante em alimentos e produtos farmacêuticos.
P: Se você deseja preparar 1,00 kg de I2, quais massas de NaIO3 e NaHSO3 são necessárias?
R: A equação química balanceada para a reação entre NaIO3 e NaHSO3 para formar I2 é: 5NaIO3 + NaHSO3 + 3H2O → 3I2 + 5NaSO4 + 3H2SO4. Usando estequiometria, seriam necessários 3,33 kg de NaIO3 e 1,00 kg de NaHSO3 para preparar 1,00 kg de I2. .
P: Por que adicionamos bissulfito de sódio no final da reação?
R: O NaHSO3 é adicionado ao final de algumas reações químicas para remover o excesso de bromo, que pode ser prejudicial ou interferir nas etapas posteriores do processo.
P: O que é bissulfito de sódio?
R: NaHSO3 é um sal usado por suas propriedades redutoras, antioxidantes e conservantes em diversas indústrias, incluindo alimentícia, farmacêutica e tratamento de água.
P: Como o bissulfito de sódio remove o bromo?
R: O NaHSO3 reage com o bromo para formar brometo de sódio e gás dióxido de enxofre, removendo efetivamente o excesso de bromo de uma solução.
P: O que é complexo de menadiona bissulfito de sódio?
R: O complexo menadiona bissulfito de sódio é um composto sintético usado como fonte de vitamina K em alguns suplementos dietéticos e produtos de ração para animais de estimação.
P: Para que é usado o bissulfito de sódio?
R: O NaHSO3 é usado como agente redutor, antioxidante e conservante em diversas indústrias, incluindo alimentícia, farmacêutica, tratamento de água e perfuração de petróleo. Também pode ser utilizado como alisador de cabelos e em processamento fotográfico.
