O propileno (C3H6) é um gás incolor e inflamável comumente usado na produção de plásticos e fibras sintéticas. Também é utilizado como combustível em maçaricos de soldagem e corte.
| Nome da IUPAC | Propeno |
| Fórmula molecular | C3H6 |
| Número CAS | 115-07-1 |
| Sinônimos | Propileno, metiletileno, prop-1-eno, metiletileno |
| InChI | InChI=1S/C3H6/c1-3-2/h3H,1-2H3 |
Propriedades do propileno
Fórmula de Propileno
A fórmula química do propileno é C3H6. Isto significa que cada molécula de propileno contém três átomos de carbono e seis átomos de hidrogênio. A fórmula é importante nas reações químicas porque indica o número e os tipos de átomos presentes em cada molécula. A fórmula do propileno é frequentemente utilizada na produção de plásticos, fibras sintéticas e outros materiais industriais.
Massa molar de propileno
O propeno, também chamado de propeno, tem massa molar de 42,08 g/mol. Isso significa que um mol de moléculas de propeno pesa 42,08 gramas. A massa molar é importante nos cálculos químicos porque nos permite converter entre a massa e os moles de uma substância. Para calcular a massa molar do propeno, somamos as massas atômicas de seus átomos constituintes: três átomos de carbono, cada um com massa de 12,01 u, e seis átomos de hidrogênio, cada um com massa de 1,01 u.
Ponto de ebulição do propileno
O ponto de ebulição do propeno é -47,6°C (-53,7°F). Isto significa que à pressão atmosférica normal, o propeno ferve e se transforma em gás a -47,6°C. O ponto de ebulição é uma propriedade física importante do propeno porque determina as condições sob as quais a substância mudará de líquido para gás. O baixo ponto de ebulição do propeno o torna útil como refrigerante e na produção de produtos químicos.
Ponto de fusão do propileno
O propeno não tem um ponto de fusão bem definido porque sofre uma transição gradual de sólido para líquido quando aquecido. No entanto, a faixa de fusão do propeno é de aproximadamente -185 a -135 °C (-301 a -211 °F). Isto significa que o propeno começará a derreter por volta de -185°C e derreterá completamente por volta de -135°C. O ponto de fusão é importante para determinar as condições sob as quais o propeno mudará de sólido para líquido.
Densidade de propileno g/mL
A densidade do propeno é 0,74 g/mL à temperatura ambiente (25°C). Isto significa que um mililitro de propeno pesa 0,74 gramas. A densidade é uma propriedade física importante do propeno porque ajuda a determinar a massa de um determinado volume da substância. A baixa densidade do propeno o torna útil em aplicações onde é necessário um material leve.
Peso molecular do propileno
O peso molecular do propeno é 42,08 g/mol. Este valor é a soma dos pesos atômicos de todos os átomos em uma única molécula de propeno. O peso molecular é uma propriedade importante porque nos permite calcular a quantidade de uma substância em moles a partir da sua massa ou vice-versa.
Estrutura do propileno
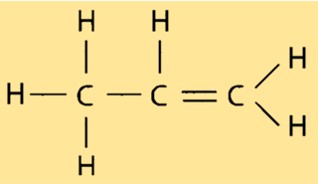
O propeno tem uma estrutura molecular linear, com cada átomo de carbono ligado a dois átomos de hidrogênio e um outro átomo de carbono. A ligação dupla entre os dois átomos de carbono confere ao propeno sua natureza reativa e o torna útil em diversas aplicações industriais. A estrutura do propeno é importante na determinação de suas propriedades, como ponto de ebulição e ponto de fusão.
| Aparência | Gás incolor |
| Gravidade Específica | 0,97 |
| Cor | Incolor |
| Cheiro | Cheiro levemente adocicado, semelhante ao de gasolina |
| Massa molar | 42,08 g/mol |
| Densidade | 0,74 g/mL (a 25°C) |
| Ponto de fusão | -185 a -135°C (-301 a -211°F) |
| Ponto de ebulição | -47,6°C (-53,7°F) |
| Ponto flash | -108°C (-162°F) |
| Solubilidade em Água | 0,075 g/100 ml (a 20°C) |
| Solubilidade | Solúvel em acetona, etanol, éter |
| Pressão de vapor | 50,6kPa (a 25°C) |
| Densidade do vapor | 1,45 (em relação ao ar) |
| pKa | 44 |
| pH | Não aplicável (o propileno não é ácido nem básico) |
Segurança e perigos do propileno
O propeno é geralmente considerado um composto relativamente seguro de manusear, mas apresenta alguns perigos. É altamente inflamável e pode pegar fogo facilmente. Portanto, deve ser armazenado e manuseado longe de fontes de ignição. O contato com a pele ou os olhos pode causar irritação e a inalação de altas concentrações de propeno pode causar tonturas e até perda de consciência. Tal como acontece com qualquer produto químico, é importante seguir os procedimentos de segurança adequados ao manusear o propeno, como usar equipamentos de proteção como luvas e óculos de proteção e garantir ventilação adequada. Em caso de exposição ou ingestão acidental, procure atendimento médico imediatamente.
| Símbolos de perigo | Altamente inflamável (F+) |
| Descrição de segurança | Manter afastado de fontes de ignição. Use em áreas bem ventiladas. |
| Números de identificação da ONU | ONU 1077 |
| Código SH | 2901.10.00 |
| Classe de perigo | 2.1 (gás inflamável) |
| Grupo de embalagem | grupo A |
| Toxicidade | Não é considerado tóxico |
Métodos de síntese de propileno
Vários métodos podem sintetizar propeno, incluindo craqueamento a vapor de hidrocarbonetos, desidrogenação de propano e craqueamento catalítico fluido.
O craqueamento a vapor é o método mais comum de síntese de propeno. Isto envolve o aquecimento de matérias-primas de hidrocarbonetos, como etano, propano ou nafta, a altas temperaturas na presença de vapor. O processo envolve o resfriamento e a separação da mistura de hidrocarbonetos resultante para isolar o propeno como um produto separado.
A desidrogenação do propano é outro método de síntese do propeno. Isto envolve a reação do propano com um catalisador para remover o hidrogênio e produzir propeno. Este método é atraente porque o propano está facilmente disponível e é barato.
O processo de craqueamento catalítico fluido utiliza um catalisador para transformar hidrocarbonetos pesados em produtos mais leves, incluindo propeno, quebrando moléculas maiores em moléculas menores.
Usos do propileno
O propeno é um produto químico versátil que tem muitos usos em diversas indústrias. Aqui estão alguns dos usos mais comuns do propeno:
- Produção de Polipropileno: Desempenha papel crucial como matéria-prima primária na produção de polipropileno, material versátil utilizado em diversas aplicações, como embalagens, têxteis e peças automotivas.
- Combustível: Usado como combustível em muitas aplicações industriais, como corte e soldagem com oxicorte.
- Solvente: Serve como um solvente útil para uma variedade de produtos químicos e as pessoas o utilizam em muitas aplicações, incluindo a extração de óleos essenciais.
- Refrigerante: Utilizado como refrigerante em alguns sistemas, especialmente em aplicações onde o uso de outros refrigerantes é restrito.
- Intermediário químico: Usado como intermediário químico na produção de muitos outros produtos químicos, como óxido de propileno, acrilonitrila e butiraldeído.
- Embalagens para alimentos: utilizadas na produção de materiais para embalagens de alimentos, como filmes e recipientes.
- Produtos de higiene pessoal: Muitos produtos de higiene pessoal, como hidratantes e produtos para os cabelos, usam propilenoglicol, um derivado do propeno.
Questões:
P: Qual reação deve ser usada para converter propeno em halogeneto de alquila?
R: O propeno pode ser convertido em um halogeneto de alquila usando uma reação com halogenetos de hidrogênio, como cloreto de hidrogênio (HCl) ou brometo de hidrogênio (HBr).
P: Qual é a fórmula empírica do propeno (c3h6)?
R: A fórmula empírica do propeno (C3H6) é CH2.
P: O propeno é solúvel em água?
R: O propeno não é solúvel em água porque é um composto apolar e a água é um solvente polar.
P: Quais são as massas da fórmula do propeno, C3H6?
R: A massa da fórmula do propeno (C3H6) é de aproximadamente 42,08 g/mol.
P: Qual é a fórmula empírica para a seguinte fórmula molecular: C3H6?
R: A fórmula empírica para C3H6 é CH2.
P: Como você poderia mostrar experimentalmente que a fórmula molecular do propeno é C3H6, não CH2?
R: Um método experimental para determinar a fórmula molecular do propeno é analisar seus produtos de combustão. Se o propeno for queimado com excesso de oxigênio, os produtos serão dióxido de carbono e água. Medindo as quantidades de dióxido de carbono e água produzidas, a fórmula molecular do propeno pode ser determinada como C3H6 em vez de CH2.
