Acetofenona ou metilfenil cetona é um composto orgânico aromático com a fórmula C8H8O. É utilizado na produção de perfumes e resinas, e como solvente e intermediário em produtos farmacêuticos.
| Nome IUPAC | 1-feniletanona |
| Fórmula molecular | C8H8O |
| Número CAS | 98-86-2 |
| Sinônimos | Metilfenilcetona, fenilmetilcetona, AP, acetilbenzeno, benzoilmetil, etilfenilcetona, Hypnon |
| InChI | InChI=1S/C8H8O/c1-7(9)8-5-3-2-4-6-8/h2-6H,1H3 |
Estrutura da acetofenona
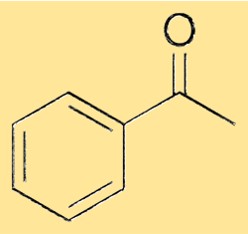
A estrutura da acetofenona consiste em um grupo fenil ligado a um grupo carbonila por meio de uma ligação simples. O grupo carbonila consiste em um átomo de carbono duplamente ligado a um átomo de oxigênio. O grupo fenil é um anel de átomos de carbono de seis membros com cinco átomos de hidrogênio ligados, e a sexta posição é ocupada pelo átomo de carbono carbonila. Essa estrutura confere à acetofenona suas propriedades características e permite que ela sirva como matéria-prima versátil para a síntese de diversos produtos químicos.
Ponto de fusão da acetofenona
A acetofenona tem um ponto de fusão de -15,7°C. O ponto de fusão é a temperatura na qual um sólido se transforma em líquido a pressão constante. A acetofenona é um sólido cristalino à temperatura ambiente e tem um ponto de fusão relativamente baixo em comparação com outros compostos semelhantes. O ponto de fusão de um composto é determinado pela sua estrutura molecular e pela força das suas forças intermoleculares.
Espectro IR da acetofenona
O espectro IR da acetofenona mostra picos característicos em 1705 cm^-1, que corresponde ao grupo carbonila, e em 3030-3100 cm^-1, que corresponde ao estiramento do CH aromático. Esses picos fornecem informações importantes sobre os grupos funcionais presentes na molécula.
Massa molar da acetofenona:
A acetofenona tem massa molar de 120,15 g/mol. É um composto orgânico aromático com um grupo carbonila ligado a um anel fenil. A massa molar é a soma das massas atômicas dos átomos contidos em um mol do composto. No caso da acetofenona, ela possui 8 átomos de carbono, 8 átomos de hidrogênio e um átomo de oxigênio, totalizando 17 átomos em uma molécula. A massa molar é uma propriedade importante de um composto porque é usada para calcular a quantidade de substância em uma determinada amostra, necessária para diversas aplicações na química e na indústria.
Ponto de ebulição da acetofenona
A acetofenona tem um ponto de ebulição de 202°C. O ponto de ebulição é a temperatura na qual um líquido se transforma em gás a pressão constante. A acetofenona é um composto orgânico volátil e tem um ponto de ebulição relativamente alto em comparação com outros compostos semelhantes. O ponto de ebulição de um composto é determinado pela força de suas forças intermoleculares, que são as forças que mantêm as moléculas unidas no estado líquido ou sólido. No caso da acetofenona, possui um grupo carbonila polar que pode formar ligações de hidrogênio com outras moléculas de acetofenona, o que fortalece as forças intermoleculares e aumenta o ponto de ebulição.
Densidade de metilfenil cetona g/ml
A metilfenil cetona tem uma densidade de 1,03 g/mL à temperatura ambiente. Densidade é a massa de uma substância por unidade de volume. A metilfenil cetona é um líquido à temperatura ambiente e tem uma densidade relativamente alta em comparação com outros compostos semelhantes. A densidade de um composto é determinada pelo seu peso molecular e pela densidade de suas moléculas em um determinado volume. No caso da metilfenil cetona, ela possui peso molecular relativamente alto e estrutura molecular relativamente compacta, o que torna o empacotamento de suas moléculas mais eficiente e aumenta a densidade.
Peso molecular de metilfenil cetona
A metilfenil cetona tem um peso molecular de 120,15 g/mol. O peso molecular é a soma dos pesos atômicos de todos os átomos de uma molécula. A metilfenil cetona tem 8 átomos de carbono, 8 átomos de hidrogênio e um átomo de oxigênio, totalizando 17 átomos em uma molécula. O peso molecular é uma propriedade importante de um composto porque é usado para calcular a quantidade de substância em uma determinada amostra, necessária para diversas aplicações na química e na indústria.
| Aparência | Líquido incolor a amarelo pálido |
| Gravidade Específica | 1.028-1.031 a 25°C |
| Cor | Incolor a amarelo pálido |
| Cheiro | Doce, floral, mel |
| Massa molar | 120,15 g/mol |
| Densidade | 1,03 g/mL a 25°C |
| Ponto de fusão | -15,7ºC |
| Ponto de ebulição | 202°C |
| Ponto flash | 78ºC |
| Solubilidade em Água | 3,3 g/L a 25°C |
| Solubilidade | Solúvel em álcool, éter, clorofórmio e benzeno |
| Pressão de vapor | 0,27 mmHg a 25°C |
| Densidade do vapor | 4,15 (ar = 1) |
| pKa | 10.01 |
| pH | Não aplicável (metilfenil cetona não é um ácido nem uma base) |
Segurança e perigos da metilfenil cetona
A metilfenil cetona pode ser perigosa se não for manuseada corretamente. Pode causar irritação na pele, olhos e sistema respiratório por contato ou inalação. A exposição direta a altas concentrações de vapor de metilfenilcetona pode causar dor de cabeça, tontura ou náusea. A ingestão de metilfenil cetona pode causar irritação gastrointestinal, vômito ou diarréia. A metilfenil cetona também é inflamável e pode formar misturas explosivas com o ar. Deve ser armazenado em local fresco, seco e bem ventilado, longe de fontes de ignição. Equipamentos de proteção individual, como luvas, óculos de segurança e respirador, devem ser usados ao manusear metilfenil cetona.
| Símbolos de perigo | Xi: Irritante, F: Altamente inflamável |
| Descrição de segurança | S16: Manter afastado de fontes de ignição – Não fumar, S26: Em caso de contacto com os olhos, lavar imediata e abundantemente com água e consultar um médico, S36: Usar vestuário de protecção adequado, S37: Usar luvas adequadas, S39: Usar vestuário adequado roupa de proteção. proteção facial |
| Números de identificação da ONU | ONU 2319 |
| Código SH | 291439 |
| Classe de perigo | 3 (Líquidos inflamáveis) |
| Grupo de embalagem | III |
| Toxicidade | A metilfenilcetona é classificada como irritante ocular de categoria 3 e irritante cutâneo de categoria 4. Não é considerado cancerígeno ou mutagênico. A LD50 oral (dose letal para 50% dos indivíduos testados) em ratos é de aproximadamente 3.000 mg/kg. Não é considerado um risco ambiental significativo. |
Métodos para a síntese de metilfenil cetona
Existem vários métodos para sintetizar metilfenil cetona.
Um método comum é a acilação de Friedel-Crafts do benzeno com cloreto de acetila na presença de um catalisador ácido de Lewis, como o cloreto de alumínio. Esta reação produz metilfenil cetona e cloreto de hidrogênio como subprodutos.
Outro método é a oxidação do etilbenzeno usando ar ou oxigênio na presença de um catalisador metálico como cobalto ou manganês. Esta reação produz metilfenil cetona e ácido acético como subprodutos.
A metilfenilcetona pode ser sintetizada reduzindo a fenilacetona usando agentes redutores como borohidreto de sódio ou hidreto de alumínio e lítio. Esta reação produz metilfenil cetona e o álcool correspondente como subprodutos.
Outro método envolve a reação de cloreto de benzoíla com etilbenzeno na presença de um catalisador de cloreto de alumínio para produzir metilfenil cetona e cloreto de hidrogênio como subprodutos.
Usos da metilfenil cetona
A metilfenil cetona tem diversos usos em diversas indústrias.
- A metilfenil cetona é amplamente utilizada como solvente para diversas resinas, ésteres de celulose e plásticos.
- A indústria alimentícia utiliza metilfenil cetona como agente aromatizante, principalmente para sabores de cereja e amêndoa.
- A indústria de perfumes utiliza a metilfenilcetona como matéria-prima para a produção de perfumes e outros produtos perfumados.
- Vários produtos químicos, como produtos farmacêuticos, agroquímicos e corantes, são sintetizados usando metilfenil cetona.
- A metilfenilcetona serve como intermediário na produção de fenilacetona, precursor da síntese de anfetaminas.
- A cumarina, fragrância usada em sabonetes e detergentes, é sintetizada a partir da metilfenil cetona.
- Os reagentes de química orgânica usam metilfenil cetona como reagente para a síntese de vários compostos.
- A metilfenilcetona serve como matéria-prima para a produção de outros produtos químicos, como estireno e metilestireno.
No geral, a metilfenilcetona tem uma ampla gama de aplicações em diversas indústrias devido às suas propriedades e usos versáteis.
Questões:
P: A acetofenona é polar?
R: Sim, a acetofenona é polar devido à presença de um grupo carbonila (C = O) e um anel fenil, que cria um momento dipolar.
P: O benzaldeído ou a acetofenona são mais polares?
R: O benzaldeído é mais polar que a acetofenona porque possui um momento dipolar maior devido à presença de um grupo aldeído (CHO) além do anel fenil.
P: Espectro IR da acetofenona?
R: O espectro IR da acetofenona mostra uma banda de absorção forte e ampla em torno de 1700 cm^-1, que é característica da vibração de estiramento da carbonila (C=O). Também mostra picos em torno de 3.000-3.100 cm^-1, o que corresponde às vibrações de estiramento do CH aromático.
P: Da acetofenona ao ácido benzóico?
R: A acetofenona pode ser convertida em ácido benzóico por oxidação usando um agente oxidante como permanganato de potássio ou ácido crômico. Esta reação resulta na clivagem da ligação carbono-carbono adjacente ao grupo carbonila, seguida pela oxidação do intermediário resultante para produzir ácido benzóico.
P: Do benzeno à acetofenona?
R: O benzeno pode ser convertido em acetofenona por acilação de Friedel-Crafts usando cloreto de acetila ou anidrido acético na presença de um catalisador ácido de Lewis, como cloreto de alumínio. Esta reação resulta na substituição de um átomo de hidrogênio do benzeno por um grupo acetil (-COCH3), seguido de rearranjo para formar acetofenona.
