O 1-bromobutano é um composto orgânico líquido incolor com fórmula molecular C4H9Br. É utilizado como agente alquilante em síntese orgânica e como solvente na indústria.
| Nome IUPAC | Brometo de butila |
| Fórmula molecular | C4H9Br |
| Número CAS | 109-65-9 |
| Sinônimos | 1-bromobutano, brometo de n-butila, brometo de butila, bromobutano, butano, 1-bromo-, 109-65-9, 1-brombutano, 1-bromobutano, n-C4H9Br |
| InChI | InChI=1S/C4H9Br/c1-2-3-4-5/h2-4H2.1H3 |
Massa molar de 1-bromobutano
A massa molar do 1-bromobutano é 137,03 g/mol. Para obter a massa molar do 1-bromobutano, somamos as massas atômicas do carbono, hidrogênio e bromo em uma única molécula. Os cálculos químicos muitas vezes exigem a conversão da massa de uma substância em seu número de moles, e a massa molar é essencial para essa conversão.
Densidade de 1-bromobutano g/ml
A densidade do 1-bromobutano é 1,27 g/mL a 25°C (77°F). Esta é a massa por unidade de volume da substância. A densidade do 1-bromobutano é maior que a da água, permitindo que seja facilmente separado de soluções aquosas.
Ponto de ebulição do 1-bromobutano
O ponto de ebulição do 1-bromobutano é 101°C (214°F). É a temperatura na qual a pressão de vapor do líquido é igual à pressão externa. É uma medida da força das forças intermoleculares no líquido. O ponto de ebulição do 1-bromobutano o torna um solvente e reagente útil em química orgânica.
Ponto de fusão de C4H9Br
O ponto de fusão do C4H9Br é -112°C (-170°F). É a temperatura na qual as fases sólida e líquida da substância estão em equilíbrio. O ponto de fusão depende da intensidade das forças intermoleculares presentes no sólido. O baixo ponto de fusão do C4H9Br o torna líquido à temperatura ambiente e permite seu fácil manuseio.
Peso molecular C4H9Br
O peso molecular de C4H9Br é 137,03 g/mol. É a soma dos pesos atômicos de todos os átomos da molécula. O peso molecular é usado para calcular a quantidade de uma substância necessária para uma reação ou para determinar a quantidade de produto obtido.
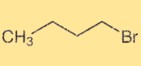
Estrutura 1-bromobutano
O 1-bromobutano tem uma estrutura alquílica de cadeia linear com um átomo de bromo ligado ao quarto átomo de carbono. É um composto orgânico com a fórmula química C4H9Br. A estrutura do 1-bromobutano determina suas propriedades físicas e químicas e sua reatividade em reações orgânicas.
Fórmula 1-Bromobutano
A fórmula do 1-bromobutano é C4H9Br. Isso mostra o número e o tipo de átomos presentes na molécula. A fórmula do 1-bromobutano é importante na determinação de sua reatividade e comportamento em reações químicas.
| Aparência | Líquido incolor |
| Gravidade Específica | 1,27 a 25°C |
| Cor | Incolor |
| Cheiro | Cheiro característico e doce |
| Massa molar | 137,03 g/mol |
| Densidade | 1,27 g/mL a 25°C |
| Ponto de fusão | -112ºC |
| Ponto de ebulição | 101°C |
| Ponto flash | 25°C |
| Solubilidade em Água | Ligeiramente solúvel |
| Solubilidade | Solúvel em etanol, éter, clorofórmio |
| Pressão de vapor | 10 mmHg a 25°C |
| Densidade do vapor | 4.6 |
| pKa | 16,5 |
| pH | Neutro |
1-Bromobutano Segurança e perigos
O 1-bromobutano é um produto químico perigoso que deve ser manuseado com cautela. É tóxico se ingerido ou inalado e pode causar irritação na pele e nos olhos em contato. O produto químico também é inflamável e pode representar risco de incêndio se exposto ao calor, faíscas ou chamas. É importante usar equipamento de proteção adequado, como luvas, óculos de proteção e jaleco ao manusear o 1-bromobutano. O produto químico deve ser armazenado em local fresco, seco e bem ventilado e afastado de fontes de ignição. Em caso de exposição acidental, lavar imediatamente a área afetada com água e procurar atendimento médico.
| Símbolos de perigo | T,F |
| Descrição de segurança | Manter afastado do calor, faíscas e chamas. Use luvas de proteção/proteção ocular/proteção facial. EM CASO DE INALAÇÃO: Remover a vítima para um local ao ar livre e mantê-la em repouso numa posição confortável para respirar. EM CASO DE INGESTÃO: Contacte um CENTRO DE INFORMAÇÃO ANTIVENENOS ou um médico se não se sentir bem. Enxágue a boca. Armazene em uma área bem ventilada. Fique calmo. Descarte o conteúdo/recipiente de acordo com os regulamentos locais/regionais/nacionais/internacionais. |
| Identificadores AN | ONU1126 |
| Código SH | 290339 |
| Classe de perigo | 3 |
| Grupo de embalagem | II |
| Toxicidade | Tóxico se ingerido ou inalado. Pode causar irritação na pele e nos olhos. |
Métodos para a síntese de 1-bromobutano
O C4H9Br pode ser sintetizado pela reação de 1-butanol e ácido bromídrico (HBr) na presença de ácido sulfúrico (H2SO4) como catalisador. Isso é chamado de reação de halogenação catalisada por ácido. A reação prossegue da seguinte forma:
- O HBr é adicionado ao 1-butanol na presença de ácido sulfúrico.
- O HBr protona o grupo hidroxila do 1-butanol, criando um bom grupo de saída (água).
- O grupo de saída (água) é substituído pelo íon brometo (Br-) do HBr, formando C4H9Br.
- A mistura de reação é então aquecida para destilar o C4H9Br.
Outro método de síntese de C4H9Br envolve a reação de buteno com brometo de hidrogênio na presença de um iniciador de peróxido, como peróxido de benzoíla ou peróxido de t-butila. Isso é chamado de reação de halogenação de radical livre. A reação prossegue da seguinte forma:
- Buteno é adicionado a uma mistura de brometo de hidrogênio e um iniciador de peróxido.
- O iniciador peróxido sofre clivagem homolítica, produzindo dois radicais reativos.
- Os radicais atacam a ligação dupla do buteno, formando um radical brometo e um radical centrado no carbono.
- O radical brometo então reage com o radical centrado no carbono, formando C4H9Br.
Ambos os métodos são amplamente utilizados para a síntese de C4H9Br e podem ser otimizados para produzir altos rendimentos do produto. No entanto, é importante seguir as precauções de segurança adequadas ao trabalhar com produtos químicos perigosos, como HBr e peróxidos.
Usos do 1-bromobutano
C4H9Br é um produto químico versátil utilizado em diversas aplicações industriais e laboratoriais.
- Os químicos orgânicos utilizam o C4H9Br como matéria-prima para sintetizar outros compostos orgânicos, especialmente para a produção de produtos farmacêuticos e agroquímicos.
- As reações químicas requerem C4H9Br como solvente e atua como reagente na síntese orgânica.
- Os fabricantes incorporam C4H9Br em sabores, fragrâncias e outros compostos aromáticos. Além disso, é um componente da produção de surfactantes, amplamente utilizado em agentes de limpeza como detergentes e sabões.
- O C4H9Br funciona como intensificador de octanas em aditivos de gasolina e é utilizado na produção de refrigerantes e polímeros.
- Técnicas analíticas como cromatografia gasosa requerem C4H9Br como material de referência laboratorial padrão. Laboratórios de ensino e pesquisa em química orgânica a utilizam como matéria-prima para diversos experimentos.
No geral, as propriedades versáteis do C4H9Br tornam-no um produto químico importante nas áreas química, farmacêutica e industrial, com uma ampla gama de aplicações em síntese orgânica, fabricação e pesquisa.
Questões:
Sua tarefa é converter 2-bromobutano em 1-buteno com o maior rendimento. Quais reagentes você usaria?
Para converter 2-bromobutano em 1-buteno com o maior rendimento, eu usaria uma base forte como o etóxido de sódio (NaOEt) em etanol como reagente. A reação prosseguiria como uma reação de eliminação conhecida como reação de desidrohalogenação.
A reação seria a seguinte:
- 2-bromobutano é adicionado a uma solução de etóxido de sódio em etanol.
- A base forte extrai um próton do carbono beta adjacente ao bromo, formando um íon alcóxido intermediário.
- O íon alcóxido intermediário sofre eliminação do grupo de saída (bromo), resultando na formação do alceno (1-buteno) e do brometo de sódio.
- A mistura reaccional é então destilada para remover o produto 1-buteno.
Usando uma base forte como NaOEt, a reação pode ser conduzida para a formação de 1-buteno, e usando etanol como solvente, a reação pode ser realizada de forma relativamente segura e econômica. Além disso, o uso de uma base forte e etanol como solvente pode levar a altos rendimentos de 1-buteno.
Por que começar com 1-bromobutano para o seu teste de acetona?
Começar com C4H9Br para o NAI no teste de acetona é uma forma útil de determinar se um determinado composto orgânico contém ou não um átomo de halogênio. O teste envolve a adição de iodeto de sódio (NaI) ao composto orgânico dissolvido em acetona, seguido da adição de uma pequena quantidade de cloro ou iodo.
A reação ocorre de acordo com o seguinte mecanismo:
- NaI é adicionado ao composto orgânico dissolvido em acetona, levando à formação do sal haleto de sódio e do haleto orgânico correspondente.
- A adição de uma pequena quantidade de cloro ou iodo leva à formação de uma pequena quantidade de gás halogênio, que reage com o haleto de sódio para formar o gás halogênio correspondente.
- O gás halogênio reage então com o halogeneto orgânico para formar um precipitado colorido, indicando a presença do halogênio no composto orgânico original.
C4H9Br é um composto comumente usado para este teste porque é um composto orgânico simples e facilmente acessível que contém um átomo de halogênio (bromo). Ele também reage facilmente com iodeto de sódio e gás halogênio para formar um precipitado colorido, tornando-o um composto de teste útil para detectar a presença de halogênio em outros compostos orgânicos.
