Ciclohexanol ou C6H11OH é um líquido oleoso incolor com leve odor. É comumente usado como solvente e na produção de náilon e outros produtos químicos.
| Nome IUPAC | Ciclohexanol |
| Fórmula molecular | C6H12O ou C6H11OH |
| Número CAS | 108-93-0 |
| Sinônimos | Hexahidrofenol; Hidrofenol; Álcool ciclohexílico; Hexalina; Ciclohexanolol |
| Estrutura química | InChI=1S/C6H12O/c7-6-4-2-1-3-5-6/h6-7H,1-5H2 |
Estrutura do ciclohexanol
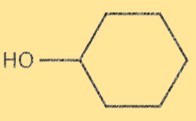
O ciclohexanol possui um anel de carbono de seis membros com um grupo hidroxila (-OH) ligado a um dos átomos de carbono. A fórmula molecular do ciclohexanol é C6H12O. O anel ciclohexano possui conformação carnuda com o grupo hidroxila localizado na posição axial. A estrutura do ciclohexanol é importante porque determina suas propriedades físicas e químicas.
Fórmula Ciclohexanol
A fórmula química do ciclohexanol é C6H12O. Isso representa o número e os tipos de átomos em uma molécula de ciclohexanol. A fórmula é importante porque é usada para calcular a quantidade de ciclohexanol necessária em uma reação. Além disso, é usado para determinar a estequiometria de uma reação.
Espectro IR do ciclohexanol
O espectro IR do ciclohexanol mostra um pico amplo e forte em aproximadamente 3400 cm-1 devido à presença do grupo hidroxila (-OH). Este pico é indicativo da presença de álcool. Além disso, o espectro mostra vários picos na faixa de 1000–1300 cm-1 devido à presença do anel ciclohexano. O espectro IR do ciclohexanol é importante porque pode ser usado para identificar e caracterizar a substância.
Massa molar de Ciclohexanol
A soma das massas atômicas de todos os átomos de uma molécula de ciclohexanol permite calcular sua massa molar, que é 100,16 g/mol. A massa molar desempenha um papel crucial na determinação da quantidade de ciclohexanol necessária em uma reação e na conversão entre gramas e moles em cálculos estequiométricos.
Ponto de ebulição do ciclohexanol
O ponto de ebulição do ciclohexanol é 161,5°C (322,7°F). Esta é a temperatura na qual a fase líquida do ciclohexanol se transforma na fase gasosa. O ponto de ebulição é uma propriedade física importante porque é usado para purificar e separar o ciclohexanol de outras substâncias em uma mistura. O ponto de ebulição relativamente alto do ciclohexanol o torna útil como solvente em reações que requerem altas temperaturas.
Ponto de fusão C6H11OH
C6H11OH tem um ponto de fusão de 25,93°C (78,67°F). Esta é a temperatura na qual a fase sólida do C6H11OH se transforma na fase líquida. O ponto de fusão é uma propriedade física importante porque é usado para identificar e caracterizar C6H11OH. Também é usado para determinar a pureza de C6H11OH.
Densidade C6H11OH g/mL
C6H11OH tem uma densidade de 0,962 g/mL a 25°C (77°F). Esta é a massa de C6H11OH por unidade de volume da substância. A densidade é uma propriedade física importante porque é usada para determinar a massa de C6H11OH necessária para uma reação. Além disso, é usado para calcular a concentração de C6H11OH em uma solução.
Peso molecular de C6H11OH
C6H11OH tem um peso molecular de 100,16 g/mol. É a soma dos pesos atômicos de todos os átomos de uma molécula C6H11OH. O peso molecular é uma propriedade importante porque é usado para calcular a quantidade de C6H11OH necessária em uma reação. Além disso, é usado para converter gramas e moles em cálculos estequiométricos.
| Aparência | Líquido incolor |
| Gravidade Específica | 0,962g/ml |
| Cor | Incolor |
| Cheiro | Cheiro leve |
| Massa molar | 100,16 g/mol |
| Densidade | 0,962g/ml |
| Ponto de fusão | 25,93°C (78,67°F) |
| Ponto de ebulição | 161,5°C (322,7°F) |
| Ponto flash | 70°C (158°F) |
| Solubilidade em Água | Miscível |
| Solubilidade | Solúvel em muitos solventes orgânicos |
| Pressão de vapor | 0,14kPa (a 25°C) |
| Densidade do vapor | 3,5 (ar = 1) |
| pKa | 16.1 |
| pH | 6 a 8 |
Nota: Os valores apresentados nesta tabela são aproximados e podem variar dependendo da fonte de informação.
Segurança e perigos do ciclohexanol
O C6H11OH deve ser manuseado com cautela, pois apresenta certos riscos e perigos à segurança. A exposição a este produto químico pode causar irritação na pele, olhos e sistema respiratório. Também pode causar dores de cabeça, tonturas e náuseas se inalado. A ingestão de C6H11OH pode causar dor abdominal, vômito e diarreia. Este produto químico é inflamável e pode pegar fogo quando exposto ao calor ou chama. É importante armazenar e manusear em local fresco e seco, longe do calor e de fontes de ignição. Equipamentos de proteção como luvas, óculos de proteção e respiradores devem ser usados ao manusear C6H11OH. Se exposto, procure atendimento médico imediatamente.
| Símbolos de perigo | XI |
| Descrição de segurança | S26 – Em caso de contacto com os olhos, lavar imediata e abundantemente com água e consultar um médico.<br> S36/37/39 – Usar vestuário de proteção, luvas e equipamento de proteção ocular/ocular adequados. rosto.<br>S45 – Em caso de acidente ou indisposição, consulte imediatamente um médico (se possível mostre o rótulo ao médico). |
| Identificadores AN | ONU1986 |
| Código SH | 2907.13.00 |
| Classe de perigo | 3 |
| Grupo de embalagem | III |
| Toxicidade | Toxicidade baixa a moderada |
Métodos de síntese de ciclohexanol
C6H11OH pode ser sintetizado por vários métodos.
- Um método comum para produzir C6H11OH é hidrogenar cataliticamente o fenol na presença de um catalisador metálico, como níquel ou platina. Este método envolve a redução do anel aromático do fenol para formar C6H11OH.
- Outro método envolve a oxidação do ciclohexano usando ar ou oxigênio na presença de um catalisador como cobre ou cobalto. Este processo produz C6H11OH como um produto intermediário que pode ser posteriormente oxidado para formar ciclohexanona.
- C6H11OH também pode ser obtido por hidrólise de acetato de ciclohexila usando um catalisador ácido ou básico. Este método envolve a clivagem da ligação éster em acetato de ciclohexila para formar C6H11OH e ácido acético.
- O rearranjo de Beckmann da ciclohexanona oxima usando ácido sulfúrico como catalisador é outro método para sintetizar C6H11OH. Este processo envolve a reorganização do grupo oxima na ciclohexanona oxima para formar um intermediário amida, que pode ser hidrolisado para produzir C6H11OH.
No geral, a síntese de C6H11OH requer que os indivíduos realizem vários processos químicos e utilizem precauções e equipamentos de segurança adequados.
Usos do ciclohexanol
C6H11OH tem muitas aplicações em diferentes indústrias.
- As indústrias utilizam o C6H11OH como solvente para produzir lacas, vernizes e resinas, e como solvente para preparar medicamentos na indústria farmacêutica.
- C6H11OH serve como um importante intermediário na produção de ácido adípico, um componente necessário na fabricação de náilon. Também atua como matéria-prima para a síntese de diversos produtos químicos, incluindo bisfenol A, ciclohexanona e caprolactama.
- A indústria petrolífera adiciona C6H11OH como inibidor de corrosão ao petróleo bruto para evitar a corrosão em oleodutos e tanques de armazenamento.
- Os fabricantes usam C6H11OH para produzir plastificantes que melhoram a flexibilidade e durabilidade dos plásticos. É também um ingrediente comum em perfumes e cosméticos.
- C6H11OH é usado como fluido de transferência de calor, lubrificante e pesticida. Além disso, serve como reagente em síntese orgânica e experimentos de laboratório.
No geral, o C6H11OH tem uma ampla gama de aplicações em diversas indústrias e suas propriedades versáteis o tornam um produto químico importante em muitos processos industriais.
Questões:
O ciclohexanol é solúvel em água?
O ciclohexanol é moderadamente solúvel em água, mas sua solubilidade diminui com o aumento da temperatura. É mais solúvel em solventes orgânicos como etanol, éter dietílico e acetona. A solubilidade do C6H11OH em água se deve à formação de ligações de hidrogênio entre o grupo hidroxila do C6H11OH e as moléculas de água. No entanto, o anel ciclohexano hidrofóbico do C6H11OH reduz a sua polaridade global, tornando-o menos solúvel em água do que outros álcoois mais polares, como o metanol e o etanol. A solubilidade do C6H11OH em água é uma consideração importante na sua utilização como solvente e em processos industriais que envolvem água como meio.
Qual das seguintes séries de reações converteria o ciclohexanol em 1,2-epoxiciclohexano?
Para converter ciclohexanol em 1,2-epoxiciclohexano, a seguinte série de reações pode ser realizada:
- O ciclohexanol é primeiro tratado com um catalisador ácido forte, como o ácido sulfúrico, para formar o ciclohexeno por meio de desidratação.
- O ciclohexeno resultante reage então com um perácido como o ácido m-cloroperbenzóico (MCPBA) para formar um epóxido, particularmente 1,2-epoxiciclohexano.
Portanto, a série correta de reações para converter ciclohexanol em 1,2-epoxiciclohexano envolve a desidratação do ciclohexanol para formar ciclohexeno seguida pela epoxidação do ciclohexeno para formar 1,2-epoxiciclohexano usando um perácido.
Por que o ciclohexanol não precisa de um prefixo numérico?
O ciclohexanol não precisa de um prefixo numérico em seu nome porque é um isômero único do ciclohexanol. Isômeros são moléculas com a mesma fórmula molecular, mas com diferentes arranjos estruturais de átomos. O ciclohexanol possui um único grupo funcional hidroxila (-OH) ligado a um anel ciclohexano e sua fórmula molecular é C6H12O. Como existe apenas um arranjo possível de átomos no ciclohexanol, não é necessário um prefixo numérico para especificar sua posição ou o número de grupos funcionais. Em contraste, outros compostos como a ciclohexanona e a ciclohexanodiona têm múltiplos isômeros com diferentes posições e números de grupos carbonila e, portanto, requerem prefixos numéricos para especificar a localização dos grupos funcionais.
