O bicarbonato de sódio (NaHCO3), também conhecido como bicarbonato de sódio, é um pó cristalino branco com leve sabor alcalino. É comumente usado como agente de saída na panificação, como agente de limpeza e no tratamento de indigestão ácida e azia.
| Nome IUPAC | Carbonato de hidrogénio de sódio |
| Fórmula molecular | NaHCO3 |
| Número CAS | 144-55-8 |
| Sinônimos | Bicarbonato de sódio, hidrogenocarbonato de sódio, hidrogenocarbonato de sódio |
| InChI | InChI=1S/CHNaO3/c2-1(3)4/h(H,2,3)(H2,1,2,3)/p-1 |
Propriedades do bicarbonato de sódio
Massa molar de bicarbonato de sódio
A massa molar do NaHCO3 é 84,007 g/mol. É a soma das massas atômicas dos seus elementos constituintes: sódio, hidrogênio, carbono e oxigênio.
Ponto de ebulição do bicarbonato de sódio
O hidrogenocarbonato de sódio não tem um ponto de ebulição definido porque se decompõe antes de ser fervido. A temperatura de decomposição do bicarbonato de sódio é 851°C, altura em que se decompõe em carbonato de sódio, dióxido de carbono e água.
Ponto de fusão do bicarbonato de sódio
O hidrogenocarbonato de sódio tem um ponto de fusão de 50°C, altura em que muda de um sólido para um pó cristalino branco.
Densidade de bicarbonato de sódio g/ml
A densidade do hidrogenocarbonato de sódio é de aproximadamente 2,165 g/mL. Este valor pode variar ligeiramente dependendo do tamanho do grão e do grau de compactação do material.
Peso molecular do bicarbonato de sódio
O peso molecular do bicarbonato de sódio é 84,007 g/mol, calculado a partir de sua fórmula molecular NaHCO3.
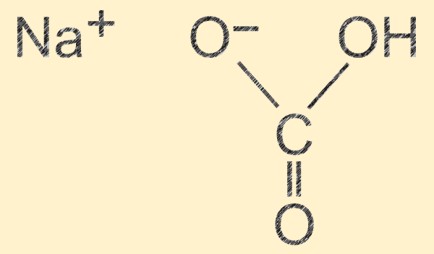
Estrutura do bicarbonato de sódio
O hidrogenocarbonato de sódio tem uma estrutura molecular composta por um íon sódio (Na+), um íon hidrogênio (H+), um íon carbonato (CO32-) e três íons oxigênio (O2-). Os íons estão dispostos em uma unidade repetitiva que forma uma estrutura cristalina, com uma ligação de hidrogênio entre as moléculas. A natureza iónica do composto confere-lhe as suas propriedades fundamentais e a ligação de hidrogénio contribui para a sua estabilidade física.
| Aparência | Pó cristalino branco |
| Gravidade Específica | 2.165g/ml |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 84,007 g/mol |
| Densidade | 2.165g/ml |
| Ponto de fusão | 50°C |
| Ponto de ebulição | Decompõe-se a 851°C |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solúvel em água |
| Solubilidade | Solúvel em água |
| Pressão de vapor | Não aplicável |
| Densidade do vapor | Não aplicável |
| pKa | 8.1 |
| pH | 8,1 (10g/L, 25°C) |
Segurança e perigos do bicarbonato de sódio
O bicarbonato de sódio é um composto seguro e comumente usado com baixo nível de toxicidade. Geralmente é considerado não perigoso, não inflamável e não explosivo. A ingestão de grandes quantidades pode causar problemas digestivos e aumentar o risco de desenvolver cálculos renais. O contato com a pele pode causar leve irritação e a inalação de poeira pode causar irritação do trato respiratório. É importante manusear o NaHCO3 com cuidado para evitar a inalação de poeira e o contato com a pele.
| Símbolos de perigo | Não aplicável |
| Descrição de segurança | S24/25 |
| Números de identificação da ONU | UN3077, SUBSTÂNCIA AMBIENTALMENTE PERIGOSA, SÓLIDA, NOS (Bicarbonato de Sódio) |
| Código SH | 2836.90.90 |
| Classe de perigo | 9 |
| Grupo de embalagem | III |
| Toxicidade | Baixa toxicidade se ingerido, inalado ou em contato com a pele |
Métodos para a síntese de bicarbonato de sódio
O bicarbonato de sódio (NaHCO3) pode ser sintetizado por vários métodos, incluindo o processo Solvay, que é o método mais comumente utilizado para produção em larga escala. O processo Solvay envolve a reação de cloreto de sódio, amônia e dióxido de carbono para produzir hidrogenocarbonato de sódio e cloreto de cálcio. O hidrogenocarbonato de sódio também pode ser sintetizado pela reação de NaHCO3 e dióxido de carbono, ou pela reação de hidróxido de sódio e dióxido de carbono. Esses métodos produzem uma forma de NaHCO3 de alta pureza, que pode ser posteriormente purificada por recristalização.
Usos do bicarbonato de sódio
O hidrogenocarbonato de sódio, comumente conhecido como bicarbonato de sódio, tem uma ampla gama de utilizações devido às suas propriedades únicas. Na culinária, é frequentemente usado como agente de saída para produtos assados, como bolos e pães. Nos cuidados pessoais, é usado como abrasivo suave em pastas de dente e como desodorante. Também é utilizado na indústria alimentícia como ajustador de pH e agente neutralizante. O hidrogenocarbonato de sódio também tem usos medicinais, como tratamento de azia, indigestão e acidez. Além disso, é utilizado na fabricação de produtos de limpeza e extintores devido às suas propriedades extintoras. O hidrogenocarbonato de sódio também tem utilizações ambientais, pois pode ser usado para neutralizar águas residuais ácidas.
