Então você já viu a imagem acima, certo?
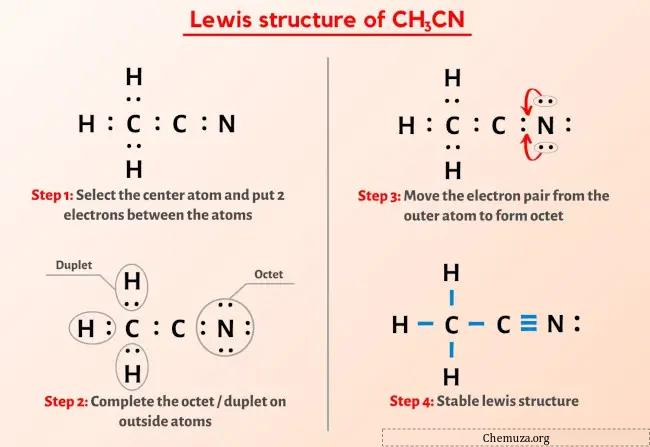
Deixe-me explicar brevemente a imagem acima.
A estrutura CH3CN Lewis tem 2 átomos de carbono (C) no centro que estão rodeados por três átomos de hidrogênio (H) e um átomo de nitrogênio (N). Existe uma ligação tripla entre o átomo de carbono (C) e o átomo de nitrogênio (N). Existe 1 dupleto livre no átomo de nitrogênio (N).
Se você não entendeu nada da imagem acima da estrutura de Lewis do CH3CN, então fique comigo e você obterá uma explicação detalhada passo a passo sobre como desenhar uma estrutura de Lewis da molécula CH3CN .
Então, vamos prosseguir para as etapas de desenho da estrutura de Lewis do CH3CN.
Etapas para desenhar a estrutura CH3CN Lewis
Etapa 1: Encontre o número total de elétrons de valência em CH3CN
Para encontrar o número total de elétrons de valência em uma molécula de CH3CN, primeiro você precisa saber os elétrons de valência presentes no átomo de carbono , no átomo de hidrogênio e também no átomo de nitrogênio.
(Elétrons de valência são os elétrons presentes na órbita mais externa de qualquer átomo.)
Aqui vou lhe dizer como encontrar facilmente os elétrons de valência do carbono, hidrogênio e também do nitrogênio usando uma tabela periódica.
Elétrons totais de valência na molécula CH3CN
→ Elétrons de valência dados pelo átomo de carbono:
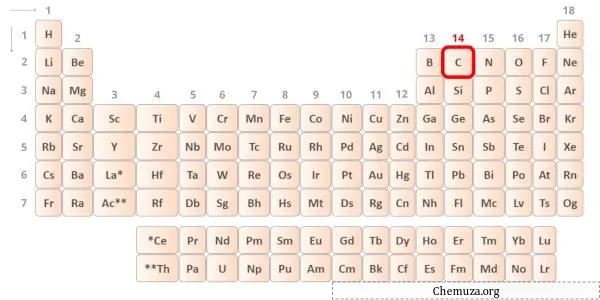
O carbono é um elemento do grupo 14 da tabela periódica. [1] Portanto, os elétrons de valência presentes no carbono são 4 .
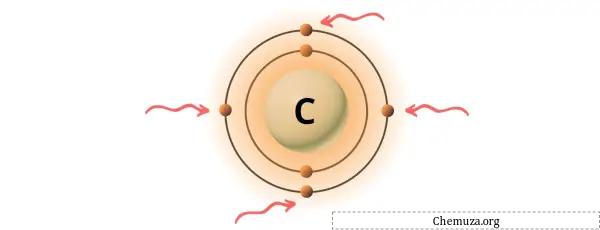
Você pode ver os 4 elétrons de valência presentes no átomo de carbono, conforme mostrado na imagem acima.
→ Elétrons de valência dados pelo átomo de hidrogênio:
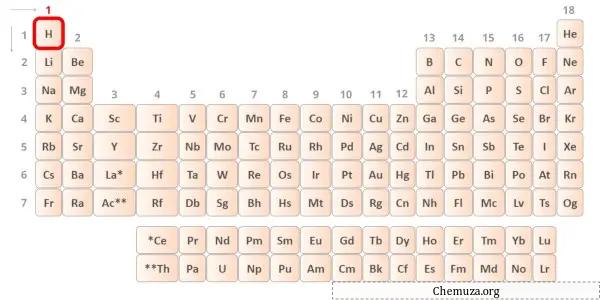
O hidrogênio é um elemento do grupo 1 da tabela periódica. [2] Portanto, o elétron de valência presente no hidrogênio é 1 .

Você pode ver que apenas um elétron de valência está presente no átomo de hidrogênio, conforme mostrado na imagem acima.
→ Elétrons de valência dados pelo átomo de nitrogênio:
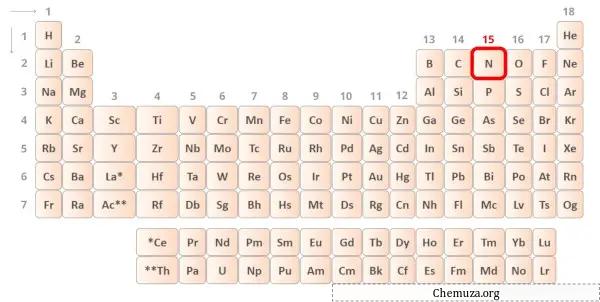
O nitrogênio é um elemento do grupo 15 da tabela periódica.[3] Portanto, os elétrons de valência presentes no nitrogênio são 5 .

Você pode ver os 5 elétrons de valência presentes no átomo de nitrogênio, conforme mostrado na imagem acima.
Então,
Total de elétrons de valência na molécula CH3CN = elétrons de valência doados por 2 átomos de carbono + elétrons de valência doados por 3 átomos de hidrogênio + elétrons de valência doados por 1 átomo de nitrogênio = 4(2) + 1(3) + 5 = 16 .
Passo 2: Selecione o átomo central
Para selecionar o átomo central, devemos lembrar que o átomo menos eletronegativo permanece no centro.
(Lembre-se: se houver hidrogênio em determinada molécula, sempre coloque hidrogênio do lado de fora.)
Agora, aqui a molécula dada é um CH3CN e contém átomos de carbono (C), átomos de hidrogênio (H) e átomos de nitrogênio (N).
Então, de acordo com a regra, temos que manter o hidrogênio fora.
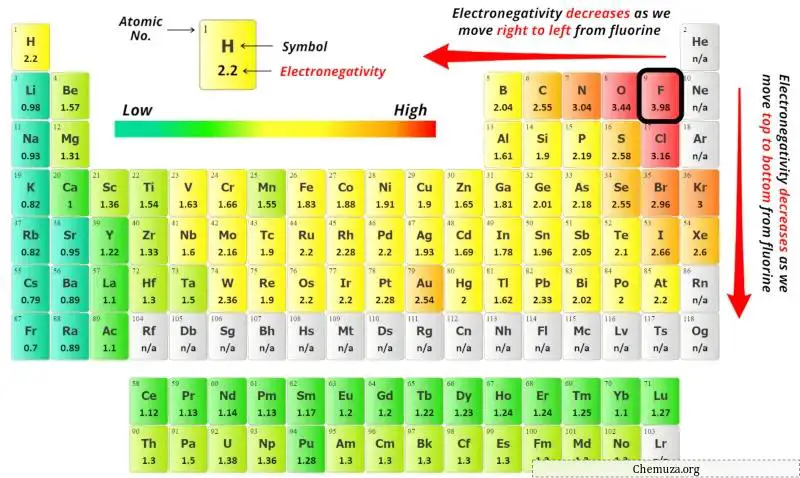
Agora você pode ver os valores de eletronegatividade do átomo de carbono (C) e do átomo de nitrogênio (N) na tabela periódica acima.
Se compararmos os valores de eletronegatividade do carbono (C) e do nitrogênio (N), então o átomo de carbono é menos eletronegativo .
Aqui, os átomos de carbono (C) são o átomo central e o átomo de nitrogênio (N) é o átomo externo.
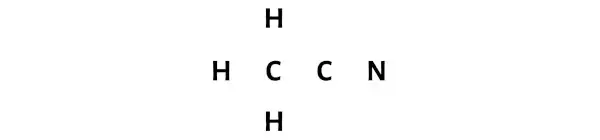
Etapa 3: Conecte cada átomo colocando um par de elétrons entre eles
Agora, na molécula CH3CN, você precisa colocar os pares de elétrons entre os átomos de carbono (C), nitrogênio (N) e hidrogênio (H).
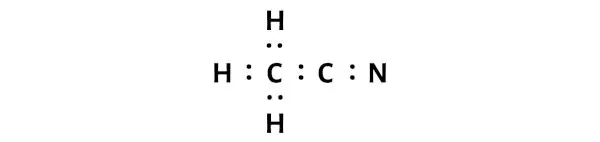
Isso indica que esses átomos estão quimicamente ligados entre si em uma molécula de CH3CN.
Etapa 4: tornar os átomos externos estáveis
Nesta etapa você precisa verificar a estabilidade dos átomos externos.
Aqui no esboço da molécula CH3CN, você pode ver que os átomos externos são átomos de hidrogênio e átomos de nitrogênio.
Esses átomos de hidrogênio e nitrogênio formam um dupleto e um octeto , respectivamente, e são, portanto, estáveis.
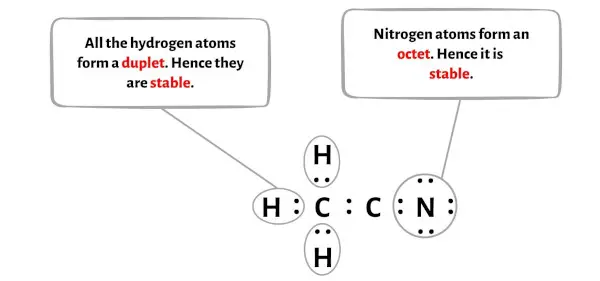
Além disso, na etapa 1, calculamos o número total de elétrons de valência presentes na molécula CH3CN.
A molécula CH3CN tem um total de 16 elétrons de valência e todos esses elétrons de valência são usados no diagrama acima.
Portanto, não há mais pares de elétrons para manter nos átomos centrais.
Então agora vamos para a próxima etapa.
Etapa 5: verifique o octeto no átomo central. Se não tiver octeto, mova o par solitário para formar uma ligação dupla ou tripla.
Nesta etapa, você precisa verificar se o átomo de carbono central (C) é estável ou não.
Para verificar a estabilidade do átomo central de carbono (C), precisamos verificar se ele forma um octeto ou não.
Infelizmente, o átomo de carbono não forma um octeto aqui. O carbono tem apenas 4 elétrons e é instável.
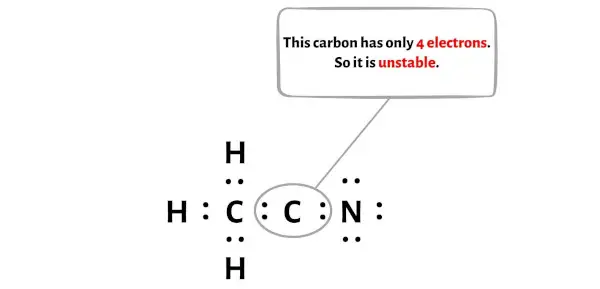
Agora, para tornar este átomo de carbono estável, você precisa deslocar o par de elétrons do átomo de nitrogênio externo para que o átomo de carbono possa ter 8 elétrons (ou seja, um octeto).
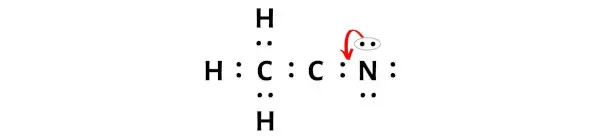
Mas depois de mover um par de elétrons, o átomo de carbono ainda não forma um octeto, pois possui apenas 6 elétrons.
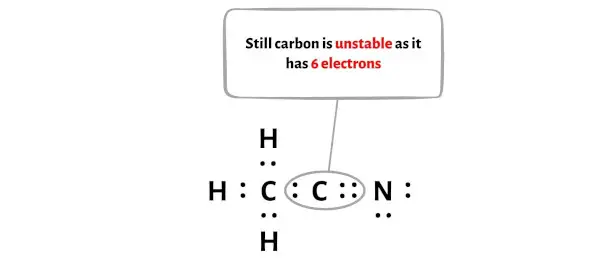
Novamente, precisamos mover um par extra de elétrons apenas do átomo de nitrogênio.
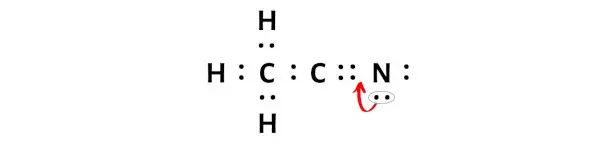
Após movimentar esse par de elétrons, o átomo de carbono central receberá mais 2 elétrons e seu total de elétrons passará a ser 8.
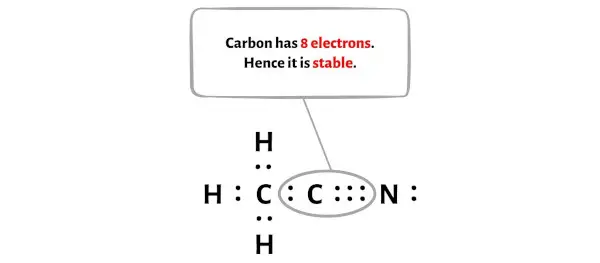
Você pode ver na imagem acima que o átomo de carbono forma um octeto.
E, portanto, o átomo de carbono é estável.
Agora vamos passar para a última etapa para verificar se a estrutura de Lewis do CH3CN é estável ou não.
Passo 6: Verifique a estabilidade da estrutura de Lewis
Agora você chegou à última etapa em que precisa verificar a estabilidade da estrutura de Lewis do CH3CN.
A estabilidade da estrutura de Lewis pode ser verificada usando um conceito formal de carga .
Resumindo, devemos agora encontrar a carga formal dos átomos de hidrogênio (H), carbono (C) e nitrogênio (N) presentes na molécula CH3CN.
Para calcular o imposto formal, deve-se utilizar a seguinte fórmula:
Carga formal = Elétrons de valência – (Elétrons ligantes)/2 – Elétrons não ligantes
Você pode ver o número de elétrons ligantes e elétrons não ligantes para cada átomo da molécula CH3CN na imagem abaixo.
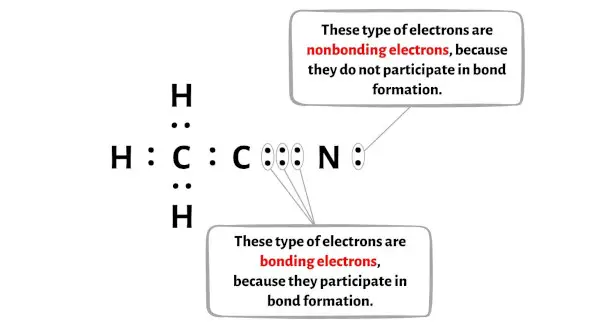
Para o átomo de hidrogênio (H):
Elétron de valência = 1 (porque o hidrogênio está no grupo 1)
Elétrons de ligação = 2
Elétrons não ligantes = 0
Para o átomo de carbono (C):
Elétrons de valência = 4 (porque o carbono está no grupo 14)
Elétrons de ligação = 8
Elétrons não ligantes = 0
Para o átomo de nitrogênio (N):
Elétrons de valência = 5 (porque o nitrogênio está no grupo 15)
Elétrons de ligação = 6
Elétrons não ligantes = 2
| Acusação formal | = | elétrons de valência | – | (Elétrons de ligação)/2 | – | Elétrons não ligantes | ||
| H | = | 1 | – | 2/2 | – | 0 | = | 0 |
| VS | = | 4 | – | 02/08 | – | 0 | = | 0 |
| NÃO | = | 5 | – | 6/2 | – | 2 | = | 0 |
A partir dos cálculos de carga formal acima, você pode ver que o átomo de hidrogênio (H), o átomo de carbono (C), bem como o átomo de nitrogênio (N) têm carga formal “zero ” .
Isto indica que a estrutura de Lewis do CH3CN acima é estável e não há mais alterações na estrutura do CH3CN acima.
Na estrutura de pontos de Lewis acima de CH3CN, você também pode representar cada par de elétrons de ligação (:) como uma ligação simples (|). Fazer isso resultará na seguinte estrutura de Lewis de CH3CN.
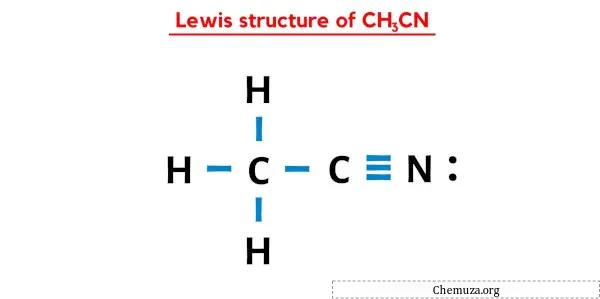
Espero que você tenha entendido completamente todas as etapas acima.
Para mais prática e melhor compreensão, você pode tentar outras estruturas de Lewis listadas abaixo.
Experimente (ou pelo menos veja) estas estruturas de Lewis para uma melhor compreensão:
