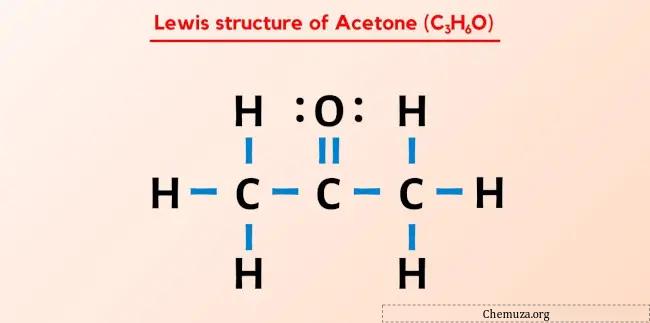
A estrutura de Lewis da acetona (também conhecida como propanona ou C3H6O) tem três átomos de carbono (C) consecutivos, que têm um átomo de oxigênio (O) duplamente ligado ao átomo central de carbono (C) e três átomos únicos de hidrogênio (H) ligados para cada átomo de carbono externo (C). Existem 2 pares solitários no átomo de oxigênio (O).
Vamos entender a estrutura de Lewis da acetona em etapas simples.
Etapas para desenhar a estrutura de Lewis da acetona (C3H6O)
Etapa 1: Encontre o número total de elétrons de valência na molécula C3H6O
Para encontrar o número total de elétrons de valência em uma molécula de C3H6O, primeiro você precisa saber os elétrons de valência presentes no átomo de carbono , no átomo de hidrogênio e também no átomo de oxigênio.
(Elétrons de valência são os elétrons presentes na órbita mais externa de qualquer átomo.)
Aqui vou lhe dizer como encontrar facilmente os elétrons de valência do carbono, hidrogênio e também do oxigênio usando uma tabela periódica.
Elétrons totais de valência na molécula C3H6O
→ Elétrons de valência dados pelo átomo de carbono:
O carbono é um elemento do grupo 14 da tabela periódica. [1] Portanto, os elétrons de valência presentes no carbono são 4 .
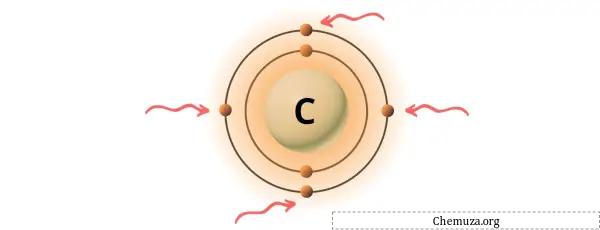
Você pode ver os 4 elétrons de valência presentes no átomo de carbono, conforme mostrado na imagem acima.
→ Elétrons de valência dados pelo átomo de hidrogênio:
O hidrogênio é um elemento do grupo 1 da tabela periódica.[2] Portanto, o elétron de valência presente no hidrogênio é 1 .

Você pode ver que apenas um elétron de valência está presente no átomo de hidrogênio, conforme mostrado na imagem acima.
→ Elétrons de valência dados pelo átomo de oxigênio:

O oxigênio é um elemento do grupo 16 da tabela periódica. [3] Portanto, os elétrons de valência presentes no oxigênio são 6 .
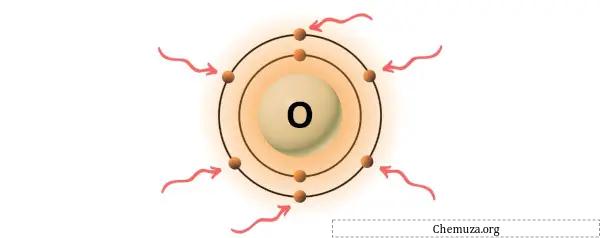
Você pode ver os 6 elétrons de valência presentes no átomo de oxigênio, conforme mostrado na imagem acima.
Então,
Total de elétrons de valência na molécula C3H6O = elétrons de valência doados por 3 átomos de carbono + elétrons de valência doados por 6 átomos de hidrogênio + elétrons de valência doados por 1 átomo de oxigênio = 4(3) + 1(6) + 6 = 24 .
Passo 2: Prepare o esboço
A estrutura de Lewis da acetona possui três átomos de carbono consecutivos com um átomo de oxigênio ligado ao átomo de carbono central. Os átomos de hidrogênio estão ligados aos dois átomos de carbono externos. O átomo de oxigênio está duplamente ligado ao átomo de carbono, enquanto os átomos de hidrogênio estão ligados de forma simples aos átomos de carbono.
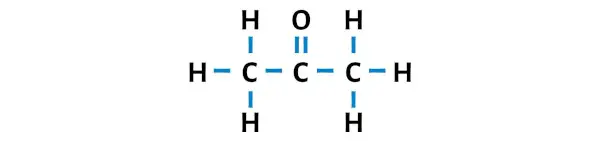
Etapa 3: tornar os átomos externos estáveis
Aqui no esboço da molécula C3H6O, você pode ver que os átomos externos são átomos de hidrogênio e átomos de oxigênio.
Os átomos de hidrogênio são estáveis porque têm 2 elétrons (porque o hidrogênio só precisa de 2 elétrons para formar um dupleto estável).
Então agora vamos tornar o átomo de oxigênio estável formando um octeto nele.
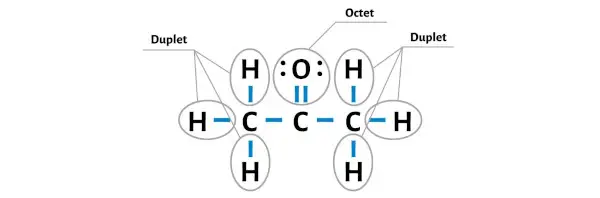
Agora você pode ver que todos os átomos externos são estáveis.
Além disso, na etapa 1, calculamos o número total de elétrons de valência presentes na molécula C3H6O.
A molécula C3H6O tem um total de 24 elétrons de valência e todos esses elétrons de valência são usados no diagrama de C3H6O acima.
Portanto, a estrutura de Lewis de C3H6O (ou acetona) acima é uma estrutura estável.
Espero que você tenha entendido as etapas acima.
Para mais prática e melhor compreensão, você pode tentar outras estruturas de Lewis listadas abaixo.
Experimente (ou pelo menos veja) estas estruturas de Lewis para uma melhor compreensão:
