O nitrato de chumbo (Pb(NO₃)₂) é um sólido cristalino branco. É solúvel em água e comumente utilizado em laboratório para diversas aplicações, como fabricação de outros compostos de chumbo e fogos de artifício.
| Nome IUPAC | Nitrato de chumbo (II) |
| Fórmula molecular | Pb(NO₃)₂ |
| Número CAS | 10099-74-8 |
| Sinônimos | Nitrato de chumbo, dinitrato de chumbo, nitrato de chumbo (II), nitrato de chumbo (IV) |
| InChI | InChI=1S/2NO3.Pb/c2 2-1(3)4;/q2 -1;+2 |
Propriedades do nitrato de chumbo
Fórmula de nitrato de chumbo
A fórmula química do dinitrato de chumbo é Pb(NO₃)₂. Isto indica que cada molécula de dinitrato de chumbo contém um átomo de chumbo (Pb) ligado a dois íons NO₃. Esta fórmula é essencial para a compreensão da composição e propriedades do composto.
Massa molar de nitrato de chumbo
A massa molar do dinitrato de chumbo pode ser calculada somando as massas atômicas de seus elementos constituintes. Para o chumbo (Pb), a massa atômica é de aproximadamente 207,2 g/mol, e para o NO₃, é de aproximadamente 62,0 g/mol. A soma desses valores dá uma massa molar de aproximadamente 331,2 g/mol para o dinitrato de chumbo.
Ponto de ebulição do nitrato de chumbo
O ponto de ebulição do dinitrato de chumbo é a temperatura na qual ele muda de líquido para gás sob pressão atmosférica padrão. O ponto de ebulição do dinitrato de chumbo é relativamente alto, em torno de 470°C (878°F), tornando-o adequado para algumas aplicações industriais.
Ponto de fusão do nitrato de chumbo
O ponto de fusão do dinitrato de chumbo é a temperatura na qual ele muda de sólido para líquido. O dinitrato de chumbo tem um ponto de fusão de aproximadamente 470°C (878°F). Esta característica ajuda a determinar suas condições adequadas de armazenamento e manuseio.
Densidade de nitrato de chumbo g/mL
A densidade do nitrato de chumbo é uma medida de sua massa por unidade de volume. A densidade do dinitrato de chumbo é de aproximadamente 4,53 g/mL. Essa alta densidade a torna uma substância pesada e é considerada em diversos processos industriais e laboratoriais.
Peso molecular do nitrato de chumbo
O peso molecular do dinitrato de chumbo, também chamado de massa molar, é de aproximadamente 331,2 g/mol. Este valor é crucial em cálculos estequiométricos e para determinar a quantidade de substância numa determinada amostra.
Estrutura do nitrato de chumbo
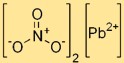
O dinitrato de chumbo possui estrutura cristalina em sua forma sólida. Os cátions Pb²⁺ são cercados por ânions NO₃⁻ em um arranjo tridimensional. Esta estrutura cristalina confere ao nitrato de chumbo sua estabilidade e propriedades características.
Solubilidade do nitrato de chumbo
O nitrato de chumbo é muito solúvel em água. Dissolve-se facilmente em água para formar uma solução límpida e incolor. A solubilidade do dinitrato de chumbo é essencial em diversas aplicações, como em reações químicas e como precursor na síntese de outros compostos de chumbo. O manuseio e descarte adequados são cruciais devido à sua solubilidade e aos potenciais impactos ambientais.
| Aparência | Sólido cristalino branco |
| Gravidade Específica | 4,53g/ml |
| Cor | Incolor |
| Cheiro | Inodoro |
| Massa molar | 331,2 g/mol |
| Densidade | 4,53g/ml |
| Ponto de fusão | 470°C (878°F) |
| Ponto de ebulição | ~470°C (~878°F) |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Muito solúvel |
| Solubilidade | Solúvel em água, ligeiramente solúvel em álcool etílico |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não disponível |
| pH | Neutro (cerca de 7) |
Segurança e perigos do nitrato de chumbo
O dinitrato de chumbo apresenta vários riscos de segurança. O contato direto com o composto pode irritar a pele e os olhos. A inalação de poeira ou vapores de dinitrato de chumbo pode causar problemas respiratórios. Devido à sua solubilidade em água, pode contaminar os mananciais e prejudicar a vida aquática. Além disso, os compostos de chumbo são tóxicos quando ingeridos e a exposição ao chumbo pode levar ao envenenamento por chumbo. Para minimizar os riscos, devem ser tomadas medidas de segurança adequadas ao manusear nitrato de chumbo, tais como utilizar equipamento de proteção, trabalhar numa área bem ventilada e seguir as diretrizes estabelecidas para armazenamento. manuseio e descarte. É essencial ter cuidado para evitar efeitos adversos à saúde e contaminação ambiental.
| Símbolos de perigo | Perigoso para a saúde, corrosivo, irritante |
| Descrição de segurança | Irritante. Evite contato direto. Use EPI. |
| Números de identificação da ONU | Nº ONU 1469 (nitrato de chumbo) |
| Código SH | 2834.29.1000 |
| Classe de perigo | 5.1 (Agente oxidante) |
| Grupo de embalagem | II |
| Toxicidade | Tóxico se ingerido ou inalado. |
Métodos de síntese de nitrato de chumbo
Existem vários métodos para sintetizar dinitrato de chumbo, todos envolvendo a reação de compostos de chumbo com ácido nítrico.
Uma abordagem comum é misturar óxido de chumbo (PbO) ou carbonato de chumbo (PbCO₃) com ácido nítrico concentrado (HNO₃). A reação produz dinitrato de chumbo e água. Outro método envolve a dissolução de chumbo metálico ou óxido de chumbo em ácido nítrico diluído, levando à formação de dinitrato de chumbo.
O segundo método envolve a reação entre Pb(OAc)₂ e nitrato de sódio . Nesta abordagem, dissolva o Pb(OAc)₂ em água e, em seguida, adicione nitrato de sódio à solução. A reação entre esses dois compostos leva à formação de dinitrato de chumbo e acetato de sódio.
O químico deve dissolver o chumbo metálico ou o óxido de chumbo em ácido nítrico diluído a quente para sintetizar o dinitrato de chumbo no laboratório. Eles devem controlar cuidadosamente a reação para evitar a geração excessiva de calor e fumaça. Uma vez concluída a reação, a solução de dinitrato de chumbo é geralmente purificada por filtração ou cristalização.
É crucial gerenciar cuidadosamente o processo de síntese devido à toxicidade dos compostos de chumbo. Para garantir sua segurança, eles devem usar ventilação adequada e usar equipamentos de proteção individual (EPI) adequados. Além disso, devem descartar todos os resíduos de maneira adequada para evitar a contaminação do meio ambiente.
Usos do nitrato de chumbo
O dinitrato de chumbo encontra diversas aplicações em diferentes indústrias devido às suas propriedades únicas. Alguns dos principais usos do dinitrato de chumbo incluem:
- Produtos pirotécnicos: Os fabricantes costumam usar dinitrato de chumbo para aumentar o brilho e as cores dos displays pirotécnicos porque atua como um agente oxidante.
- Indústria de corantes e pigmentos: A produção de alguns pigmentos e corantes à base de chumbo, como os pigmentos amarelo cromo e laranja, envolve o uso de dinitrato de chumbo como matéria-prima.
- Estabilizador térmico: A indústria de plásticos utiliza dinitrato de chumbo como estabilizador térmico para PVC (cloreto de polivinila) para evitar a degradação térmica durante o processamento e uso.
- Fósforos: As cabeças dos fósforos contêm nitrato de chumbo para promover inflamação quando atingidas contra uma superfície áspera.
- Galvanoplastia: Os banhos de galvanoplastia incorporam dinitrato de chumbo como componente essencial para facilitar a deposição de revestimentos de chumbo em diversas superfícies.
- Química Analítica: Os laboratórios utilizam dinitrato de chumbo como reagente para realizar testes e análises químicas específicas.
- Inibidor de corrosão: Algumas formulações utilizam dinitrato de chumbo como inibidor de corrosão de metais, protegendo-os da oxidação e degradação.
- Produtos farmacêuticos: A indústria farmacêutica utiliza ocasionalmente dinitrato de chumbo como reagente em processos de síntese específicos.
Questões:
P: O nitrato de chumbo é solúvel?
R: Sim, o nitrato de chumbo é solúvel em água.
Q: Prata metálica é adicionada a uma solução de nitrato de chumbo (ii). O que é uma reação química equilibrada?
A: Reação química balanceada: 2Ag + Pb(NO₃)₂ → 2AgNO₃ + Pb.
P: O nitrato de chumbo ii é um eletrólito?
R: Sim, o dinitrato de chumbo (II) é um eletrólito.
P: Qual é a porcentagem em massa de chumbo no nitrato de chumbo(ii) (pb(no3)2) arredondada para três algarismos significativos?
R: A % em massa de chumbo no Pb(NO₃)₂ é de aproximadamente 73,5%.
P: O que acontece quando o nitrato de chumbo é aquecido?
R: Quando o nitrato de chumbo é aquecido, ele se decompõe para produzir óxido de chumbo, dióxido de nitrogênio e gás oxigênio.
P: O nitrato de chumbo é solúvel em água?
R: Sim, o nitrato de chumbo é altamente solúvel em água.
P: Quais são os dois gases liberados quando o nitrato de chumbo é aquecido?
R: Os dois gases liberados são dióxido de nitrogênio (NO₂) e oxigênio (O₂).
P: O que você observa quando o nitrato de chumbo é aquecido?
R: Quando o dinitrato de chumbo é aquecido, ele se decompõe, liberando vapores marrons de dióxido de nitrogênio e permanece um resíduo amarelo de óxido de chumbo.
P: Que gás é liberado quando o nitrato de chumbo é aquecido?
R: O gás dióxido de nitrogênio (NO₂) é liberado quando o nitrato de chumbo é aquecido.
P: O que acontecerá se combinarmos solução de iodeto de sódio e solução de nitrato de chumbo(ii)?
R: Quando soluções de iodeto de sódio e dinitrato de chumbo (II) são combinadas, forma-se um precipitado amarelo de iodeto de chumbo (PbI₂).
