O borato de sódio é um composto utilizado em diversas indústrias. Possui múltiplas aplicações, como agente de limpeza, fundente em metalurgia e componente em cosméticos e detergentes.
| Nome IUPAC | Borato de sódio |
| Fórmula molecular | Na2B4O7 |
| Número CAS | 1330-96-4 |
| Sinônimos | Bórax, tetraborato de sódio, tetraborato dissódico, biborato de sódio |
| InChI | InChI=1S/B4O7.2Na/c5-1-7-3-9-2-8-4-10-3;;/q-2;2*+1 |
Propriedades do borato de sódio
Fórmula de Borato de Sódio
A fórmula química do borato de sódio é Na2B4H20O17. Consiste em dois átomos de sódio (Na), quatro átomos de boro (B) e sete átomos de oxigênio (O). A fórmula representa a proporção de cada elemento no composto.
Massa molar de borato de sódio
A massa molar do bórax é calculada somando as massas atômicas de todos os átomos do composto. A massa molar do bórax é de aproximadamente 381,37 gramas por mol (g/mol). É útil para determinar a quantidade de substância presente em uma determinada amostra.
Ponto de ebulição do borato de sódio
O bórax tem um ponto de ebulição relativamente alto. À pressão atmosférica padrão, ferve a aproximadamente 1,575 graus Celsius (C). Este alto ponto de ebulição o torna adequado para diversas aplicações industriais que envolvem processos de alta temperatura.
Borato de sódio Ponto de fusão
O bórax tem um ponto de fusão de cerca de 741 graus Celsius (C). Ele sofre uma transição de fase do estado sólido para o líquido nesta temperatura. O ponto de fusão relativamente baixo permite que o bórax derreta facilmente e seja usado em vários processos de fabricação.
Densidade de borato de sódio g/ml
A densidade do bórax é de aproximadamente 1,73 gramas por mililitro (g/mL). A densidade é uma medida da quantidade de massa contida em um determinado volume. A densidade relativamente alta do bórax torna-o um composto útil em aplicações onde o seu peso ou concentração é importante.
Peso molecular do borato de sódio
O peso molecular do bórax é de aproximadamente 381,37 gramas por mol (g/mol). Representa a soma dos pesos atômicos de todos os átomos de uma molécula de bórax. O peso molecular é essencial para vários cálculos, como determinar o número de moles ou a massa de uma substância.
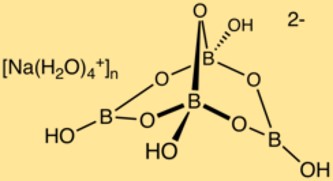
Estrutura do borato de sódio
O bórax possui uma estrutura cristalina complexa composta de poliedros boro-oxigênio e íons sódio. Os átomos de boro formam uma rede com os átomos de oxigênio, criando uma estrutura tridimensional. Os íons sódio estão localizados nesta estrutura, garantindo a estabilidade do composto.
Solubilidade do borato de sódio
O bórax é moderadamente solúvel em água. Dissolve-se facilmente em água quente e sua solubilidade aumenta com a temperatura. Contudo, a sua solubilidade em solventes orgânicos é limitada. A solubilidade do bórax o torna útil para uma variedade de aplicações, inclusive como agente de limpeza e na formulação de soluções e misturas.
| Aparência | Pó cristalino branco |
| Gravidade Específica | 1,73g/ml |
| Cor | Branco |
| Cheiro | Inodoro |
| Massa molar | 381,37 g/mol |
| Densidade | 1,73g/ml |
| Ponto de fusão | 741°C |
| Ponto de ebulição | 1575°C |
| Ponto flash | Não aplicável |
| Solubilidade em Água | Solúvel |
| Solubilidade | Solúvel em água, solubilidade limitada em solventes orgânicos |
| Pressão de vapor | Não disponível |
| Densidade do vapor | Não disponível |
| pKa | Não aplicável |
| pH | Por volta das 9h às 10h |
Segurança e perigos do borato de sódio
O bórax deve ser manuseado com cautela devido aos seus potenciais riscos de segurança. Pode causar irritação na pele, olhos e sistema respiratório por contato direto ou inalação. A ingestão de grandes quantidades pode causar distúrbios gastrointestinais. Medidas de proteção, como luvas e óculos de proteção, devem ser utilizadas ao trabalhar com bórax para evitar a exposição. É importante armazená-lo em local seguro e bem ventilado, longe de substâncias incompatíveis. Se ocorrer ingestão ou exposição acidental, deve-se procurar atendimento médico imediato. As Fichas de Dados de Segurança de Materiais apropriadas e as instruções de manuseio devem ser consultadas para obter informações detalhadas sobre os perigos do bórax e as precauções de segurança.
| Símbolos de perigo | Tóxico |
| Descrição de segurança | Perigoso se ingerido. Causa irritação na pele e nos olhos. |
| Números de identificação da ONU | ONU 1458 |
| Código SH | 2840.19.20 |
| Classe de perigo | 6.1 (Substâncias tóxicas) |
| Grupo de embalagem | III |
| Toxicidade | Toxicidade moderada por ingestão ou contato com a pele/olhos. |
Métodos para a síntese de borato de sódio
Existem vários métodos para sintetizar bórax. Um método comum é a reação entre bórax (tetraborato deca-hidratado de sódio) e carbonato de sódio . Neste processo, dissolva o bórax em água e adicione carbonato de sódio à solução. A reação ocorre, formando bórax e precipitando um sólido. Separe e seque o sólido para obter bórax.
Outro método é dissolver o ácido bórico em água e adicionar gradualmente hidróxido de sódio à solução. A reação ocorre e forma bórax. Evapore a solução para remover o excesso de água e obter cristais de bórax.
Além disso, misture óxido de boro com hidróxido de sódio em um solvente adequado e aqueça a mistura. A reação ocorre e forma bórax. Filtre a mistura para separar as impurezas e deixe o filtrado esfriar e cristalizar, produzindo bórax.
Esses métodos sintéticos fornecem rotas para obter bórax de maneira controlada. No entanto, é importante seguir as precauções de segurança adequadas e manusear os produtos químicos de forma responsável durante o processo de síntese.
Usos do borato de sódio
O bórax, também conhecido como bórax, tem uma ampla gama de utilizações em diversas indústrias devido às suas propriedades versáteis. Aqui estão algumas de suas aplicações comuns:
- Fluxo na Metalurgia: Serve como fluxo em aplicações de soldagem e brasagem, ajudando a reduzir o ponto de fusão dos metais e facilitando o fluxo do metal fundido.
- Retardador de Chama: Encontra aplicação como retardador de chama em vários materiais, incluindo isolamento de celulose, têxteis e produtos de madeira.
- Vidro e cerâmica: O bórax é um componente essencial na fabricação de vidro e cerâmica. Ajuda a diminuir o ponto de fusão, melhorar a durabilidade e melhorar as propriedades ópticas destes materiais.
- Tampão de pH: Funciona como tampão de pH em laboratórios e experimentos científicos.
- Agente de limpeza: Produtos domésticos, como detergentes para a roupa, saboneteiras e produtos de limpeza multiuso, usam o bórax de maneira eficaz como agente de limpeza.
- Cosméticos: Cosméticos e produtos de higiene pessoal usam bórax como agente tamponante, ajustador de pH e emulsificante.
- Conservante: Os produtos de madeira contêm bórax como conservante para prevenir infestações por fungos e insetos.
- Agricultura: O bórax atua como fertilizante de micronutrientes para corrigir deficiências de boro nas culturas, promovendo assim o crescimento saudável das plantas.
- Aplicações Médicas: As formulações medicinais incorporam bórax por suas propriedades anti-sépticas e adstringentes.
- Tratamento de Água: Os processos de tratamento de água utilizam bórax para inibir o crescimento de algas e controlar os níveis de pH.
Essas diversas aplicações destacam a importância do bórax em diversas indústrias, tornando-o um composto valioso e versátil.
Questões:
P: Para que é usado o borato de sódio?
R: O bórax é usado como agente de limpeza, fluxo na metalurgia, componente em cosméticos, retardador de chama, na fabricação de vidro/cerâmica, como preservativo de madeira, etc.
P: Onde comprar borato de sódio?
R: O bórax pode ser adquirido em vários fornecedores de produtos químicos, lojas de ferragens, mercados online e alguns supermercados.
P: Qual será o cátion quando o borato de sódio se dissolver?
R: O cátion liberado quando o bórax se dissolve é o sódio (Na+).
P: Borato de sódio é o mesmo que ácido bórico?
R: Não, o bórax e o ácido bórico são compostos diferentes, embora ambos contenham boro.
P: Borato de sódio é o mesmo que bórax?
R: Sim, o bórax é comumente chamado de bórax.
P: O borato de sódio é baseado?
R: O bórax atua como uma base fraca em soluções aquosas.
P: O borato de sódio é seguro para beber?
R: O bórax não deve ser ingerido, pois pode ser tóxico. Não se destina ao consumo.
P: O borato de sódio neutraliza o ácido sulfúrico?
R: Não, o bórax não neutraliza o ácido sulfúrico. Ele pode reagir, mas não o neutralizará completamente.
P: Qual é a função do borato de sódio no tampão de eluição pH 10?
R: O bórax em tampão de eluição com pH 10 facilita a eluição de biomoléculas carregadas negativamente de colunas de cromatografia.
P: O que é bórax?
R: O bórax, também conhecido como borato de sódio, é um composto mineral natural composto de moléculas de sódio, boro, oxigênio e água.
P: O que acontece quando o bórax é fortemente aquecido?
R: Quando o bórax é fortemente aquecido, ele desidrata e perde suas moléculas de água, resultando na formação de bórax anidro.
P: Bórax é o mesmo que ácido bórico?
R: Não, o bórax e o ácido bórico são compostos diferentes. O bórax é borato de sódio, enquanto o ácido bórico é uma forma ácida de boro.
P: O que é bórax em pó?
R: O pó de bórax refere-se à forma em pó do bórax, que é usado para diversos fins, como limpeza, lavanderia e artesanato.
