Le phénol (C6H5OH) est un composé chimique utilisé dans diverses industries. Il possède des propriétés antiseptiques et est également utilisé dans la production de plastiques, de colorants et de produits pharmaceutiques.
| Nom UICPA | Phénol |
| Formule moléculaire | C6H6O |
| Numero CAS | 108-95-2 |
| Synonymes | Acide carbolique, hydroxybenzène, monohydroxybenzène |
| InChI | InChI=1S/C6H6O/c7-6-4-2-1-3-5-6/h1-5,7H |
Propriétés du phénol
Formule phénol
La formule du phénol est C6H6O. Il se compose de six atomes de carbone, six atomes d’hydrogène et un atome d’oxygène. La disposition de ces atomes confère au phénol ses propriétés chimiques uniques.
Phénol Masse molaire
La masse molaire de C6H5OH est calculée en additionnant les masses atomiques de ses éléments constitutifs. C6H5OH a une masse molaire d’environ 94,11 grammes par mole (g/mol). Cette valeur est utile pour déterminer la quantité de C6H5OH dans un échantillon donné.
Point d’ébullition du phénol
C6H5OH a un point d’ébullition d’environ 181,7 degrés Celsius (358,1 degrés Fahrenheit). Ce point d’ébullition relativement élevé indique que C6H5OH existe sous forme liquide à température ambiante et nécessite une chaleur importante pour se transformer en état gazeux.
Phénol Point de fusion
Le point de fusion du C6H5OH est d’environ 40,5 degrés Celsius (104,9 degrés Fahrenheit). Cette température marque la transition du C6H5OH de l’état solide à l’état liquide. Le faible point de fusion permet au C6H5OH de se dissoudre facilement dans divers solvants.
Densité du phénol g/mL
C6H5OH a une densité d’environ 1,07 grammes par millilitre (g/mL). Cette valeur de densité indique que C6H5OH est plus dense que l’eau, qui a une densité de 1 g/mL. Cela signifie que C6H5OH coule dans l’eau.
Phénol Poids moléculaire
Le poids moléculaire de C6H5OH est calculé en additionnant les poids atomiques de ses atomes constitutifs. C6H5OH a un poids moléculaire d’environ 94,11 grammes par mole (g/mol). Cette valeur est cruciale pour déterminer la stœchiométrie et les réactions impliquant C6H5OH.
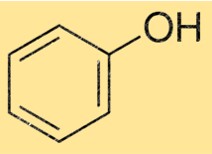
Structure du phénol
La structure de C6H5OH est constituée d’un cycle benzénique avec un groupe hydroxyle (-OH) attaché à l’un des atomes de carbone. Ce groupe hydroxyle confère à C6H5OH ses propriétés caractéristiques, ce qui en fait un composé important dans diverses applications industrielles.
Solubilité du phénol
C6H5OH présente une solubilité modérée dans l’eau. Il peut se dissoudre dans l’eau pour former une solution claire en raison de la formation de liaisons hydrogène entre les molécules C6H5OH et les molécules d’eau. Cependant, la solubilité du C6H5OH diminue avec la présence d’autres composés organiques non polaires.
| Apparence | Liquide clair et incolore |
| Gravité spécifique | 1,07 g/ml |
| Couleur | Incolore |
| Odeur | Odeur caractéristique |
| Masse molaire | 94,11 g/mole |
| Densité | 1,07 g/ml |
| Point de fusion | 40,5 °C (104,9 °F) |
| Point d’ébullition | 181,7 °C (358,1 °F) |
| Point d’éclair | 79 °C (174 °F) |
| Solubilité dans l’eau | Soluble |
| Solubilité | Soluble dans les solvants organiques |
| La pression de vapeur | 0,7 mmHg (20 °C) |
| Densité de vapeur | 3,2 (air = 1) |
| pKa | 9.95 |
| pH | Environ 6 |
Sécurité et dangers du phénol
Le C6H5OH présente des risques potentiels pour la sécurité et doit être manipulé avec prudence. Il est corrosif et peut provoquer de graves brûlures de la peau et des lésions oculaires au contact. L’inhalation de vapeurs de C6H5OH peut irriter le système respiratoire et entraîner une détresse respiratoire. L’exposition à des concentrations élevées peut être nocive pour les organes internes, notamment le foie, les reins et le système nerveux. Le C6H5OH est également inflammable et peut s’enflammer s’il est exposé à une flamme nue ou à une source de chaleur. Il est important d’utiliser des mesures de protection appropriées telles que des gants, des lunettes et une protection respiratoire lorsque vous travaillez avec du C6H5OH afin de minimiser les risques associés à sa manipulation et à son utilisation.
| Symboles de danger | Crâne et os croisés, corrosif |
| Description de la sécurité | Provoque de graves brûlures, toxique en cas d’inhalation |
| Numéros d’identification de l’ONU | UN 1671 (liquide), UN 2312 (solide) |
| Code SH | 2907.11.00 |
| Classe de danger | Classe 6.1 (Substances toxiques) |
| Groupe d’emballage | PG II (pour liquide), PG III (pour solide) |
| Toxicité | Très toxique et corrosif |
Méthodes de synthèse du phénol
Le C6H5OH peut être synthétisé par diverses méthodes. Une méthode courante est le processus au cumène. Dans ce processus, le benzène et le propylène réagissent en présence d’un catalyseur acide, généralement de l’acide phosphorique, pour produire du cumène. L’air ou l’oxygène oxyde le cumène pour produire de l’hydroperoxyde de cumène, qui subit un clivage pour donner du C6H5OH et de l’acétone comme sous-produits.
Une autre méthode est le procédé Dow, qui implique l’oxydation directe du benzène à l’aide d’air et d’un catalyseur d’oxydes métalliques, comme le cuivre ou le manganèse. Ce processus produit du C6H5OH et de l’eau comme principaux produits.
Le procédé Raschig-Hooker est une autre voie de synthèse du C6H5OH. Il s’agit de la réaction du chlorobenzène avec l’hydroxyde de sodium à des températures et des pressions élevées. Ce processus produit du C6H5OH et du chlorure de sodium.
L’hydrolyse des sels de diazonium dérivés de l’aniline permet d’obtenir du C6H5OH. Ce processus implique la réaction de l’aniline avec l’acide nitreux pour former le sel de diazonium, qui subit ensuite une hydrolyse pour générer du C6H5OH.
De plus, il existe des méthodes alternatives, notamment l’oxydation du toluène ou du benzène avec de l’acide nitrique, ainsi que l’hydrolyse du chlorobenzène à l’aide de vapeur.
Ces différentes méthodes de synthèse offrent différentes voies de production de C6H5OH, permettant sa disponibilité dans l’industrie et son application dans de nombreux secteurs tels que la pharmacie, les plastiques et les colorants.
Utilisations du phénol
Le C6H5OH trouve diverses applications dans plusieurs secteurs en raison de ses propriétés uniques. Voici quelques-unes de ses utilisations courantes :
- Il est utilisé comme antiseptique dans divers produits de santé et désinfectants pour prévenir les infections et favoriser la cicatrisation des plaies.
- Il sert de précurseur dans la production de divers plastiques, notamment les polycarbonates, les résines époxy et les résines phénoliques, largement utilisées par les industries de la construction, de l’automobile et de l’électricité.
- Le C6H5OH joue un rôle essentiel dans la synthèse de médicaments pharmaceutiques, tels que les analgésiques, les antipyrétiques et les antiseptiques, contribuant ainsi au domaine médical.
- Les fabricants l’utilisent dans la fabrication de colorants, de pigments et de parfums synthétiques pour ajouter de la couleur et du parfum à divers produits de consommation.
- Les dérivés du C6H5OH sont utilisés comme herbicides pour contrôler la croissance des mauvaises herbes dans les pratiques agricoles et horticoles.
- Les résines phénoliques dérivées du C6H5OH sont utilisées dans la production d’adhésifs, offrant de fortes propriétés de liaison dans diverses applications, notamment le travail du bois et les stratifiés.
- Les produits cosmétiques tels que les crèmes, les lotions et les teintures capillaires contiennent du C6H5OH en raison de ses propriétés conservatrices et antioxydantes.
- Dans des industries telles que la transformation alimentaire et la fabrication pharmaceutique, le C6H5OH agit comme un solvant pour extraire divers composés, notamment les graisses, les huiles et les alcaloïdes.
- Il sert d’intermédiaire polyvalent dans la synthèse de nombreux produits chimiques, notamment le bisphénol-A, le caprolactame et le nylon.
- Les chercheurs utilisent le phénol comme réactif de laboratoire dans des expériences, notamment dans les études biochimiques et de biologie moléculaire.
Le large éventail d’applications met en évidence l’importance du phénol dans différents secteurs, ce qui en fait un composé précieux dans divers processus industriels et produits de consommation.
Des questions
Q : Qu’est-ce qu’un phénol ?
R : C6H5OH est un composé chimique constitué d’un groupe hydroxyle (-OH) attaché à un cycle benzénique.
Q : Quel est le groupe fonctionnel de l’alcool et d’un phénol ?
R : Le groupe fonctionnel d’un alcool est le groupe hydroxyle (-OH), tandis que dans C6H5OH, le groupe hydroxyle est spécifiquement attaché à un cycle benzénique.
Q : À quoi sert le phénol ?
R : C6H5OH est utilisé dans diverses industries pour des applications telles que les antiseptiques, la production de plastiques, la synthèse pharmaceutique, les colorants, les parfums et comme solvant.
Q : Qu’est-ce que le phénol pKa ?
R : Le pKa de C6H5OH est d’environ 9,95, ce qui indique sa faible nature acide.
Q : Le phénol est-il un alcool ?
R : Oui, C6H5OH est considéré comme un alcool en raison de la présence du groupe fonctionnel hydroxyle (-OH).
Q : Que sont les composés phénoliques ?
R : Les composés phénoliques constituent une large classe de composés chimiques qui contiennent un ou plusieurs cycles phénol et présentent diverses activités biologiques et propriétés antioxydantes.
Q : Comment calculer la teneur phénolique totale ?
R : La teneur totale en composés phénoliques peut être déterminée à l’aide de diverses méthodes spectrophotométriques, telles que le test Folin-Ciocalteu, en mesurant l’absorbance des composés phénoliques à des longueurs d’onde spécifiques.
Q : Le phénol est-il soluble dans l’eau ?
R : Oui, C6H5OH est modérément soluble dans l’eau, formant une solution claire en raison de la formation de liaisons hydrogène avec les molécules d’eau.
Q : Qu’est-ce qui est le plus acide, le phénol ou l’alcool ?
R : C6H5OH est plus acide que l’alcool en raison de la présence d’un ion phénoxe plus stable résultant de la stabilisation par résonance dans la molécule C6H5OH.
