Tetrahydrofuran (THF) is een kleurloze organische verbinding. Het wordt vaak gebruikt als oplosmiddel in verschillende industrieën vanwege het vermogen om een breed scala aan stoffen op te lossen.
| IUPAC-naam | Oxolaan |
| Moleculaire formule | C4H8O |
| CAS-nummer | 109-99-9 |
| Synoniemen | THF, oxacyclopentaan, butyleenoxide, diethyleenoxide, cyclotetramethyleenoxide |
| InChi | InChI=1S/C4H8O/c1-2-4-5-3-1/h1-4H2 |
Eigenschappen van tetrahydrofuran
Tetrahydrofuran-formule
Tetrahydrofuran (THF) heeft de chemische formule C4H8O. Het is een cyclische ether met een vijfring die vier koolstofatomen en één zuurstofatoom bevat. THF heeft een laag kookpunt en wordt in diverse industrieën veel gebruikt als oplosmiddel.
Tetrahydrofuran molaire massa
De molaire massa van THF is ongeveer 72,11 g/mol. Deze waarde wordt berekend door de atoommassa’s van de samenstellende atomen in de molecuulformule op te tellen. De relatief lage molaire massa van THF draagt bij aan het lage kookpunt en de lage vluchtigheid, waardoor het een effectief oplosmiddel is voor een breed scala aan organische verbindingen.
Kookpunt van tetrahydrofuran
Het kookpunt van THF is 66°C (151°F) bij standaard atmosferische druk. Het lage kookpunt van THF maakt het bruikbaar als oplosmiddel voor chemische reacties die hoge temperaturen vereisen, zoals Grignard-reacties. Het lage kookpunt betekent echter ook dat THF zeer vluchtig is, dus wees voorzichtig bij het hanteren ervan.
Tetrahydrofuran Smeltpunt
Het smeltpunt van THF is ongeveer −108,5 °C (−163,3 °F). THF is vloeibaar bij kamertemperatuur, maar kan bij lage temperaturen stollen. Het lage smeltpunt van THF maakt het bruikbaar als cryogeen oplosmiddel voor toepassingen bij lage temperaturen.
Dichtheid van tetrahydrofuran g/ml
De dichtheid van THF is ongeveer 0,889 g/ml bij 20°C (68°F). Deze waarde is relatief laag vergeleken met andere gangbare oplosmiddelen. De lage dichtheid van THF maakt het bruikbaar als oplosmiddel voor dichtheidsgevoelige reacties, omdat het de totale dichtheid van het reactiemengsel kan verlagen.
Tetrahydrofuran Molecuulgewicht
Het molecuulgewicht van THF is ongeveer 72,11 g/mol. Deze waarde wordt berekend door de atoommassa’s van de samenstellende atomen in de molecuulformule op te tellen. Het relatief lage molecuulgewicht van THF draagt bij aan het lage kookpunt en de vluchtigheid ervan.
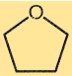
Structuur van tetrahydrofuran
THF heeft een vijfledige ringstructuur met vier koolstofatomen en één zuurstofatoom. De koolstofatomen zijn gerangschikt in een tetraëdrische geometrie, waarbij elk koolstofatoom gebonden is aan twee andere koolstofatomen en één waterstofatoom. Het zuurstofatoom is gebonden aan een koolstofatoom en een waterstofatoom.
Oplosbaarheid van tetrahydrofuran
THF is een polair aprotisch oplosmiddel dat een breed scala aan organische verbindingen kan oplossen. THF is mengbaar met water en wordt vaak gebruikt als co-oplosmiddel bij verschillende chemische reacties. THF is echter mogelijk niet compatibel met sommige materialen, dus het is belangrijk om de compatibiliteit ervan te controleren voordat u het gebruikt.
| Verschijning | Kleurloze vloeistof |
| Specifieke dichtheid | 0,889 |
| Kleur | Kleurloos |
| Geur | geur van ether |
| Molaire massa | 72,11 g/mol |
| Dikte | 0,889 g/ml |
| Fusie punt | −108,5°C (−163,3°F) |
| Kookpunt | 66°C (151°F) |
| Flitspunt | −14°C (7°F) |
| oplosbaarheid in water | Mengbaar |
| Oplosbaarheid | Oplosbaar in ethanol, ether, aceton, benzeen |
| Dampdruk | 200 mmHg bij 20°C |
| Dampdichtheid | 2,5 (lucht = 1) |
| pKa | 25.3 |
| pH | Neutraal (7) |
Veiligheid en gevaren van tetrahydrofuran
Tetrahydrofuran (THF) brengt verschillende veiligheids- en gezondheidsrisico’s met zich mee. THF is licht ontvlambaar en kan ontbranden bij kamertemperatuur. Bij verhitting of verbranding kunnen er ook giftige dampen vrijkomen. Blootstelling aan THF kan huid- en oogirritatie veroorzaken, en langdurige blootstelling kan leiden tot lever- en nierschade. Het is ook bekend dat THF duizeligheid en hoofdpijn veroorzaakt, en herhaalde inhalatie kan tot ademhalingsproblemen leiden. Voorzichtigheid is geboden bij het hanteren van THF en er moet beschermende uitrusting zoals handschoenen en een veiligheidsbril worden gedragen. THF moet worden bewaard in een koele, goed geventileerde ruimte, uit de buurt van warmtebronnen en onverenigbare materialen.
| Gevarensymbolen | Ontvlambaar, giftig |
| Beveiligingsbeschrijving | Licht ontvlambare vloeistof en damp. Veroorzaakt ernstige oogirritatie. Kan slaperigheid of duizeligheid veroorzaken. Kan schadelijk zijn bij inslikken of inademen. |
| VN-identificatienummers | VN2056 |
| HS-code | 29321100 |
| Gevarenklasse | 3 (Ontvlambare vloeistoffen) |
| Verpakkingsgroep | II |
| Toxiciteit | LD50 (oraal, rat) – 5.410 mg/kg |
Methoden voor de synthese van tetrahydrofuran
Er kunnen verschillende methoden worden gebruikt om Tetrahydrofuran (THF) te synthetiseren.
Een gebruikelijke methode omvat de katalytische hydrogenering van furaan. Hierbij wordt furaandamp over een nikkel- of palladiumkatalysator geleid in aanwezigheid van waterstofgas. De resulterende reactie produceert THF en water als bijproducten.
Een andere methode omvat de reactie van 1,4-butaandiol met zwavelzuur , gevolgd door destillatie om THF te produceren. De gevaren van geconcentreerd zwavelzuur maken deze methode minder gebruikelijk.
Zuurgekatalyseerde dehydratatie van 1,4-butaandiol is een andere manier om THF te synthetiseren. Deze methode omvat het verwarmen van 1,4-butaandiol met een sterk zuur, zoals zwavelzuur , om water te verwijderen en THF te produceren.
Bovendien kan THF worden verkregen door katalytische hydrogenolyse van cellulose of andere uit biomassa afkomstige suikers. Deze methode staat steeds meer in de belangstelling vanwege het potentieel voor hernieuwbare bronnen van THF-productie.
Elke methode heeft zijn voor- en nadelen, en de specifieke gekozen methode zal afhangen van factoren zoals de kosten, beschikbaarheid van grondstoffen en de gewenste zuiverheid van het eindproduct.
Gebruik van tetrahydrofuran
Tetrahydrofuran (THF) heeft verschillende industriële en laboratoriumtoepassingen, waaronder:
- Oplosmiddel: Vaak gebruikt als oplosmiddel voor verschillende organische verbindingen vanwege het hoge oplosmiddelvermogen en het lage kookpunt.
- Polymerisatie: Gebruikt als co-oplosmiddel bij de polymerisatie van polystyreen en polyvinylchloride, evenals bij de productie van polyurethaanschuimen.
- Chemische synthese: gebruikt als reactieoplosmiddel bij organische chemische synthese, zoals bij de bereiding van Grignard-reagentia.
- Extractie: Gebruikt als extractiemiddel voor diverse natuurlijke producten, zoals alkaloïden en steroïden.
- Kleefstoffen: Gebruikt als component in lijmformuleringen, zoals die gebruikt worden bij de productie van schoenen en leer.
- Coatings: Gebruikt bij de productie van coatings en vernissen, maar ook bij de formulering van verven en lakken.
- Analytische chemie: Gebruikt als oplosmiddel in de mobiele fase bij analyses met hoge prestatie vloeistofchromatografie (HPLC) en gaschromatografie (GC).
Vragen:
Vraag: Wat is het belangrijkste organische product dat wordt gevormd wanneer tetrahydrofuran wordt behandeld met een overmaat aan HBr?
A: Wanneer THF wordt behandeld met een overmaat aan HBr, is het belangrijkste organische product dat wordt gevormd 3-broom-1,4-dioxaan.
Vraag: Is tetrahydrofuran mengbaar met water?
A: Ja, THF is mengbaar met water. Het heeft een hoge oplosbaarheid in polaire oplosmiddelen, vooral water.
Vraag: Zal tetrahydrofuran rubber beschadigen?
A: Ja, THF kan rubber beschadigen. Dit kan zwelling, verzachting en barsten van rubbermaterialen veroorzaken.
Vraag: Is tetrahydrofuran polair of niet-polair?
A: THF is een polair oplosmiddel. Het heeft een dipoolmoment vanwege het zuurstofatoom dat aanwezig is in de ringstructuur, waardoor het een goed oplosmiddel is voor polaire verbindingen.
Vraag: Zal tetrahydrofuran ontploffen in water?
A: Nee, THF explodeert niet in water. Bij langdurige blootstelling aan lucht kan het echter een explosief peroxide vormen. Een juiste opslag en hantering zijn noodzakelijk om de vorming van peroxiden te voorkomen.
Vraag: Wat is het veiligheidsinformatieblad van tetrahydrofuran?
A: Het THF SDS (veiligheidsinformatieblad) geeft informatie over de fysische en chemische eigenschappen, instructies voor hantering en opslag, gezondheids- en veiligheidsvoorzorgsmaatregelen en noodprocedures. Het is belangrijk om de informatie in het veiligheidsinformatieblad te lezen en op te volgen wanneer u met THF werkt.
